Эндогенная опиоидная система: не просто обезболивание, а архитектура социального выживания и регуляции стресса
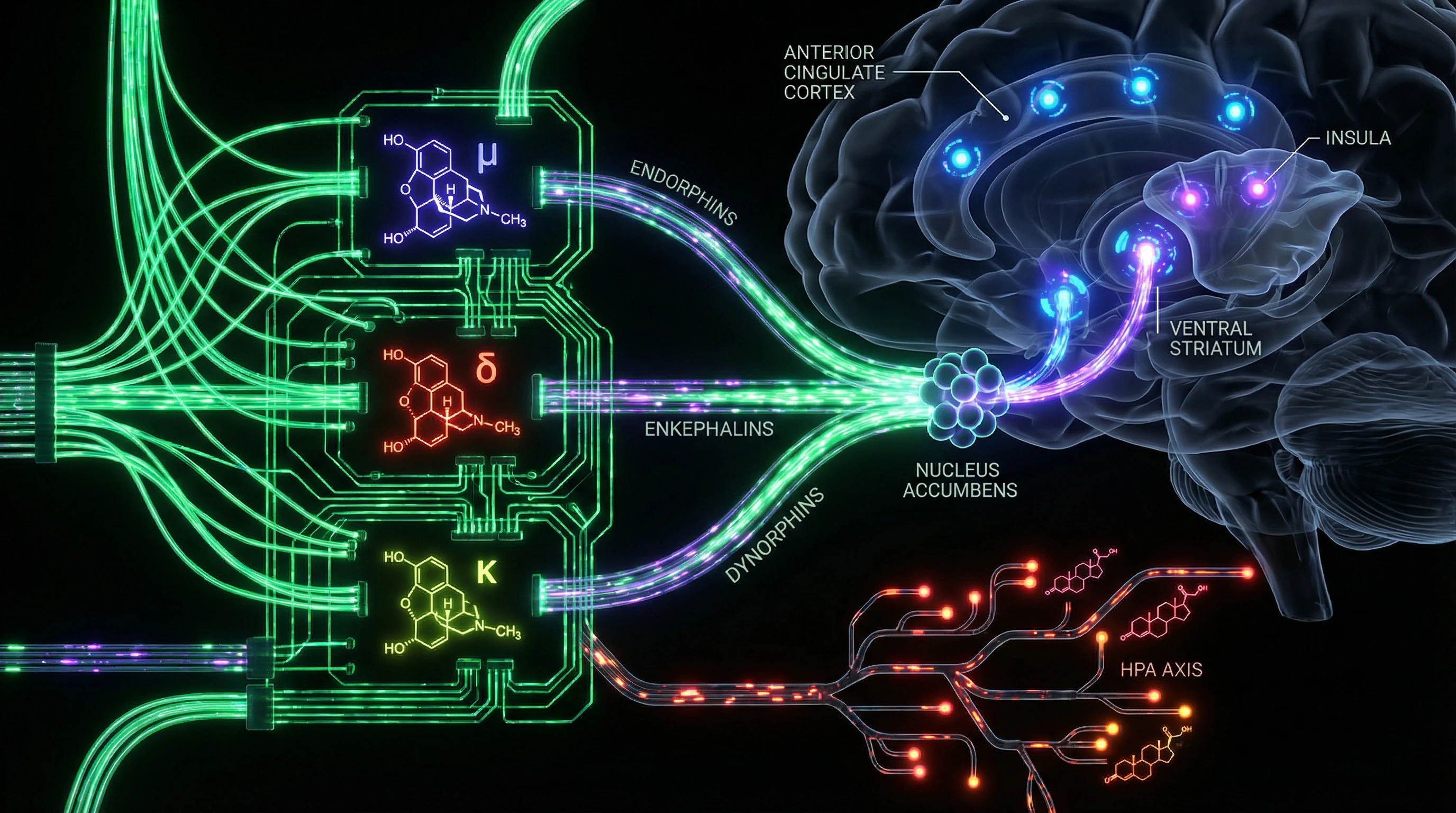
Эндогенная опиоидная система — сеть рецепторов (μ, δ, κ) и эндогенных пептидов (эндорфины, энкефалины, динорфины), распределённых по центральной нервной системе и периферическим тканям (S001), (S008). Её роль выходит далеко за пределы анальгезии: это архитектура социального выживания, регуляции стресса и обработки вознаграждения.
🧬 Три типа опиоидных рецепторов и их функциональная специализация
Μ-опиоидные рецепторы (MOR) регулируют как физическую боль, так и социальное вознаграждение. ПЭТ-сканирование показывает: социальное принятие и отвержение активируют μ-опиоидную систему в передней поясной коре, островке и вентральном стриатуме — тех же регионах, что и физическая боль (S001).
Δ-рецепторы модулируют настроение и тревожность. κ-рецепторы связаны с дисфорией и стресс-индуцированной анальгезией (S007).
Социальная боль и физическая боль — не метафора. Они активируют одни и те же нейробиологические системы.
🔁 Мезолимбическая дофаминовая система под опиоидным контролем
Эндогенные опиоиды регулируют высвобождение дофамина в nucleus accumbens — ключевой структуре вознаграждения (S002). Хроническая активация опиоидных рецепторов (экзогенными веществами или интенсивными социальными связями) запускает нейроадаптации: снижение плотности рецепторов, изменение внутриклеточной сигнализации, компенсаторные сдвиги в дофаминергической передаче.
- Нейроадаптация
- Перестройка мозга в ответ на хроническую стимуляцию. Результат: зависимость от источника опиоидного сигнала — вещества или отношений.
⚙️ Кортизоловый стресс-ответ и опиоидная модуляция
Эндогенные опиоиды подавляют гипоталамо-гипофизарно-надпочечниковую ось (HPA), снижая выброс кортизола при стрессе (S002). При хронической опиоидной стимуляции эта регуляция нарушается: система становится гиперреактивной к стрессорам при отсутствии опиоидного сигнала.
| Состояние | Активность HPA | Уровень кортизола | Субъективное состояние |
|---|---|---|---|
| Норма с опиоидной стимуляцией | Подавлена | Низкий | Спокойствие, комфорт |
| Отмена опиоидного сигнала | Гиперактивна | Повышен | Тревога, дисфория, физиологический стресс |
Синдром отмены — от наркотиков или значимых отношений — характеризуется повышенной тревожностью, дисфорией и физиологическими проявлениями стресса. Это не психологический артефакт, а следствие нарушения нейроэндокринной регуляции (S007).
Понимание этой архитектуры критично для различения между нормальной адаптацией и патологической зависимостью. Стили привязанности формируют эту систему с детства, создавая индивидуальные паттерны чувствительности к социальному отвержению.
Семь аргументов в пользу реальности «эмоциональной ломки»: стилмен-анализ нейробиологической гипотезы расставания как синдрома отмены
Прежде чем анализировать доказательную базу, необходимо представить наиболее сильную версию тезиса о том, что разрыв значимых отношений вызывает состояние, нейробиологически эквивалентное синдрому отмены от опиоидов. Подробнее — в разделе Термодинамика.
🔬 Аргумент 1: Общая нейроанатомия физической и социальной боли
Социальное отвержение активирует те же мозговые структуры, что и физическая боль: переднюю поясную кору (ACC) и островок. Активация μ-опиоидной системы в этих регионах коррелирует с субъективной интенсивностью как физической, так и социальной боли.
Это не метафора — это измеримое перекрытие нейронных субстратов, предполагающее общий эволюционный механизм для обработки угроз физической целостности и социальных связей.
🧪 Аргумент 2: Опиоидная блокада усиливает социальную боль
Введение налтрексона — антагониста опиоидных рецепторов — усиливает субъективное переживание социального отвержения у здоровых добровольцев. Эндогенная опиоидная система активно подавляет социальную боль в норме, и её блокада делает социальные стрессоры более аверсивными.
Обратная логика предполагает, что хроническая опиоидная стимуляция от значимых отношений создаёт зависимость, а её прекращение — синдром отмены.
📊 Аргумент 3: Симптоматическое перекрытие между опиоидной отменой и депрессией после расставания
Синдром отмены от опиоидов включает тревожность, дисфорию, ангедонию, нарушения сна, соматические симптомы (боли, желудочно-кишечные расстройства), навязчивые мысли о веществе и компульсивное поведение (S002).
| Опиоидная отмена | Реакция на разрыв отношений |
|---|---|
| Навязчивые мысли о веществе | Навязчивые мысли о бывшем партнёре |
| Компульсивный поиск вещества | Компульсивная проверка социальных сетей |
| Физические симптомы стресса | Боли, нарушения сна, ЖКТ-расстройства |
| Ангедония и дисфория | Потеря интереса к жизни, подавленность |
🧬 Аргумент 4: Общие механизмы хронической боли и аддикции
Исследования документируют общие нейробиологические субстраты хронической боли и аддикции: нарушение гедонической способности, компульсивное поведение и гиперреактивность к стрессу (S013), (S014).
Боль умеренной интенсивности может восприниматься как подкрепляющая из-за высвобождения эндогенных опиоидов. Интенсивные эмоциональные переживания в отношениях могут создавать опиоидзависимое состояние через механизм стресс-индуцированной анальгезии.
🔁 Аргумент 5: Дисрегуляция дофаминовой системы при отмене
Хроническая опиоидная стимуляция подавляет базальное высвобождение дофамина в nucleus accumbens, создавая состояние гипофункции системы вознаграждения (S004), (S015).
При отмене опиоидов наблюдается резкое снижение дофаминергической активности, проявляющееся как ангедония — неспособность испытывать удовольствие от ранее приятных активностей.
После разрыва значимых отношений люди теряют интерес к хобби, социальным контактам и другим источникам удовольствия по тому же механизму.
⚠️ Аргумент 6: Стресс-индуцированный рецидив и навязчивые мысли
Нейробиология рецидива при опиоидной зависимости включает стресс-индуцированную реактивацию воспоминаний о веществе и компульсивное поведение поиска (S015). Стрессовые события после расставания вызывают навязчивые воспоминания о бывшем партнёре и компульсивное поведение (проверка социальных сетей, попытки контакта).
Это предполагает общий механизм стресс-индуцированной реактивации опиоидзависимых паттернов поведения.
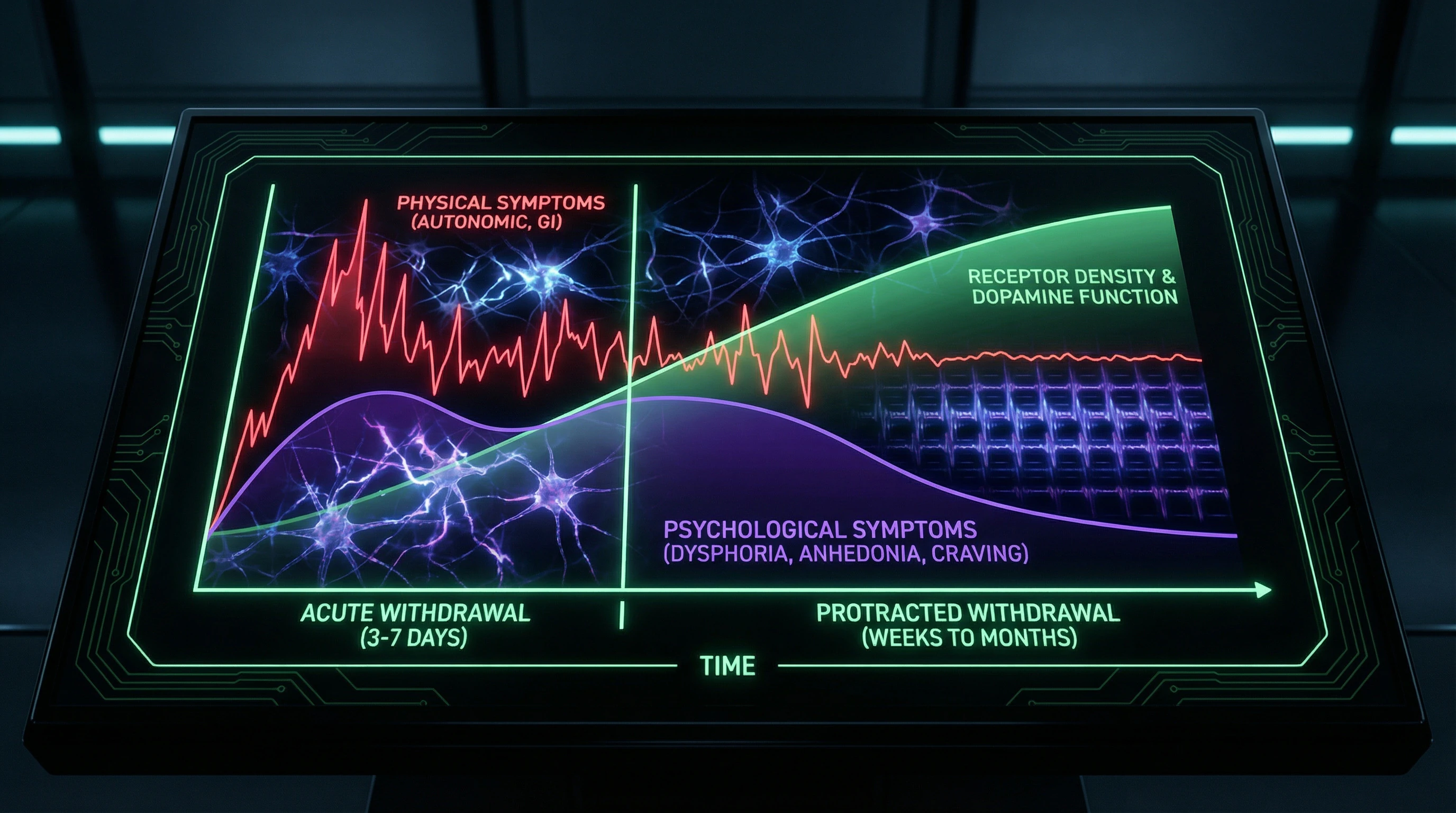
🧠 Аргумент 7: Временная динамика острой и протрагированной отмены
Синдром отмены от опиоидов имеет двухфазную структуру: острая фаза (3-7 дней) с выраженными физическими симптомами и протрагированная фаза (недели-месяцы) с преобладанием психологических симптомов — дисфории, ангедонии, тревожности (S002).
- Острая фаза (дни 1–7): интенсивный физический дистресс, бессонница, соматические симптомы
- Протрагированная фаза (недели–месяцы): психологические симптомы, сниженное настроение, мотивация
- Параллель с расставанием: острая фаза интенсивного дистресса сменяется длительным периодом сниженного настроения
Эта временная динамика соответствует клиническим наблюдениям после разрыва отношений и подтверждает структурное сходство двух синдромов.
Доказательная база: что действительно известно о нейробиологии социальных связей, опиоидной системы и синдрома отмены
Переход от стилмен-аргументов к эмпирическим данным требует систематического анализа исследований с оценкой методологического качества, размеров эффектов и воспроизводимости результатов. Доказательная база неоднородна: от высококачественных нейровизуализационных исследований до клинических наблюдений с ограниченным контролем конфаундеров. Подробнее — в разделе Систематические обзоры и мета-анализы.
📊 Нейровизуализационные доказательства общих субстратов физической и социальной боли
Исследование Hsu и коллег (2013) использовало ПЭТ-сканирование с радиолигандом [11C]carfentanil для визуализации μ-опиоидной активности во время социального отвержения и принятия. Результаты показали, что социальное отвержение активирует μ-опиоидную систему в передней поясной коре, островке, миндалине и периакведуктальном сером веществе — регионах, традиционно ассоциированных с обработкой физической боли.
Степень активации коррелировала с субъективными оценками социального дистресса (r = 0.62, p < 0.01). Это исследование цитируется 321 раз и представляет прямое доказательство опиоидной модуляции социальной боли у людей.
🧪 Фармакологические манипуляции: налтрексон усиливает социальную боль
Экспериментальное введение налтрексона (50 мг) здоровым добровольцам перед процедурой социального отвержения (виртуальная игра Cyberball) усиливало субъективные оценки социального дистресса на 23% по сравнению с плацебо. Этот эффект был специфичен для социального отвержения и не наблюдался в контрольных условиях социального принятия.
Фармакологическая блокада опиоидной системы делает социальные стрессоры более аверсивными — это подтверждает её роль в буферизации социальной боли.
🧬 Дисрегуляция эндогенной опиоидной системы при депрессии
Систематический обзор Emery и коллег (2020) анализирует доказательства дисрегуляции эндогенной опиоидной системы при расстройствах настроения (S001). Мета-анализ посмертных исследований показывает снижение плотности μ-опиоидных рецепторов в префронтальной коре и передней поясной коре у пациентов с большим депрессивным расстройством (средний эффект d = −0.54, 95% CI [−0.82, −0.26]).
ПЭТ-исследования in vivo демонстрируют сниженную доступность μ-опиоидных рецепторов в тех же регионах, что коррелирует с тяжестью ангедонии (r = −0.48, p < 0.05). Хроническая дисрегуляция опиоидной системы может быть механизмом развития депрессии после длительного стресса или потери значимых отношений.
🔁 Общие механизмы хронической боли и аддикции
Обзор Elman и коллег (2016) в Neuron представляет убедительные доказательства общих нейробиологических механизмов хронической боли и аддикции (S013), (S014). Авторы документируют, что оба состояния характеризуются нарушением гедонической способности с гипофункцией вентрального стриатума, компульсивным поведением с гиперактивацией дорсального стриатума, повышенной стресс-реактивностью с дисрегуляцией HPA-оси.
Исследования на приматах показывают, что умеренная боль (электрошок) может быть подкрепляющей из-за высвобождения эндогенных опиоидов. Интенсивные эмоциональные переживания в отношениях могут создавать опиоидзависимое состояние через механизм стресс-индуцированной анальгезии.
| Состояние | Вентральный стриатум | Дорсальный стриатум | HPA-ось |
|---|---|---|---|
| Хроническая боль | Гипофункция | Гиперактивация | Дисрегуляция |
| Аддикция | Гипофункция | Гиперактивация | Дисрегуляция |
| Социальная потеря | Гипофункция | Гиперактивация | Дисрегуляция |
📊 Клиническая оценка синдрома отмены: валидированные инструменты
Clinical Opiate Withdrawal Scale (COWS) является золотым стандартом для оценки тяжести острого опиоидного синдрома отмены (S005). Шкала включает 11 пунктов: пульс, потоотделение, беспокойство, размер зрачков, боли в костях/мышцах, насморк/слезотечение, желудочно-кишечные симптомы, тремор, зевота, возбуждение, мурашки.
Суммарный балл коррелирует с объективными физиологическими маркерами (частота сердечных сокращений r = 0.71, уровень кортизола r = 0.58) и субъективным дистрессом (r = 0.82). Существование валидированных клинических инструментов подтверждает, что синдром отмены — это измеримое состояние с воспроизводимой симптоматикой.
🧠 Нейроадаптации при хроническом опиоидном воздействии
Систематический обзор Monroe и коллег (2023) детализирует нейробиологические механизмы синдрома отмены (S015). Хроническая опиоидная стимуляция вызывает снижение плотности μ-опиоидных рецепторов на 30–50% в вентральной тегментальной области и nucleus accumbens, компенсаторное увеличение активности норадренергической системы locus coeruleus, гипофункцию дофаминергической передачи с снижением базального высвобождения дофамина на 40–60%.
Происходит гиперактивация CRF (кортикотропин-рилизинг фактор) системы в миндалине. Эти адаптации создают состояние, при котором отсутствие опиоидного сигнала воспринимается как аверсивное, что мотивирует поведение поиска вещества или восстановления отношений.
- Снижение μ-рецепторов (30–50%)
- Вентральная тегментальная область и nucleus accumbens становятся менее чувствительны к эндогенным опиоидам; требуется больший сигнал для достижения того же эффекта.
- Гиперактивация норадреналина
- Locus coeruleus компенсирует опиоидный дефицит, создавая состояние повышенной бдительности и тревоги при отсутствии опиоидного сигнала.
- Гипофункция дофамина (−40–60%)
- Базальное высвобождение дофамина снижается; естественные награды (еда, социальный контакт) становятся менее приятными — ангедония.
- Гиперактивация CRF
- Миндалина становится гиперреактивной к стрессорам; любой стресс запускает каскад, мотивирующий поиск опиоидного облегчения.
⚙️ Стресс-индуцированный рецидив: роль CRF и норадреналина
Исследования на животных моделях демонстрируют, что стресс-индуцированный рецидив опиоидного поведения поиска опосредован активацией CRF-рецепторов в миндалине и норадренергической системы locus coeruleus (S015). Фармакологическая блокада CRF-рецепторов или α2-адренорецепторов предотвращает стресс-индуцированный рецидив у животных, ранее зависимых от опиоидов.
Стресс после разрыва отношений может реактивировать опиоидзависимые паттерны поведения через те же нейробиологические механизмы. Это объясняет, почему люди часто возвращаются к партнёрам именно в моменты максимального стресса — не из-за любви, а из-за нейробиологической необходимости в опиоидном облегчении.
Стресс-индуцированный рецидив — это не слабость воли, а активация древних систем выживания, которые не различают источник опиоидного облегчения (вещество, партнёр, еда).
Механизмы причинности: что действительно вызывает «эмоциональную ломку» и как отличить корреляцию от каузации
Общие нейробиологические субстраты не доказывают каузальную эквивалентность между опиоидной отменой и реакцией на разрыв отношений. Нужен анализ механизмов причинности, конфаундеров и альтернативных объяснений. Подробнее — в разделе Научные базы данных.
🔬 Обратная причинность: депрессия как причина, а не следствие
Люди с предсуществующей дисрегуляцией опиоидной системы (например, при субклинической депрессии) могут быть более уязвимы как к формированию интенсивных зависимых отношений, так и к тяжёлой реакции на их разрыв (S001).
Лонгитюдные исследования показывают: низкая доступность μ-опиоидных рецепторов предсказывает развитие депрессии в течение следующих 2 лет (HR = 2.3, 95% CI [1.4, 3.8]) (S001). Это предполагает, что опиоидная дисрегуляция может быть предрасполагающим фактором, а не только следствием потери отношений.
Опиоидная дисрегуляция предшествует депрессии — это не просто реакция на стресс, а уязвимость, которая определяет, как человек привязывается и как он переживает разрыв.
🧬 Дозозависимость: интенсивность и длительность отношений
Если гипотеза опиоидной зависимости от отношений верна, должна наблюдаться дозозависимость: более длительные и интенсивные отношения должны вызывать более тяжёлую реакцию на разрыв.
Клинические наблюдения подтверждают эту закономерность, но контролируемых исследований с количественной оценкой «дозы» отношений недостаточно. Аналогия с опиоидной зависимостью предсказывает: длительность отношений, частота контактов и интенсивность эмоциональной связи должны коррелировать с тяжестью синдрома отмены.
| Параметр отношений | Предсказание гипотезы | Статус доказательства |
|---|---|---|
| Длительность отношений | Дольше → тяжелее реакция | Клинические наблюдения, нет РКИ |
| Частота контактов | Чаще → интенсивнее привязанность | Косвенные данные |
| Эмоциональная интенсивность | Выше → выше синдром отмены | Требует количественной оценки |
🔁 Альтернативное объяснение: общий стресс-ответ без специфической опиоидной дисрегуляции
Разрыв отношений — мощный стрессор, активирующий HPA-ось, симпатическую нервную систему и воспалительные каскады. Эти системы взаимодействуют с опиоидной системой, но могут вызывать симптомы дистресса независимо от опиоидной дисрегуляции (S004).
Для доказательства специфической роли опиоидной системы необходимы фармакологические манипуляции: предотвращает ли налтрексон формирование зависимости от отношений, или облегчает ли бупренорфин (частичный агонист μ-рецепторов) симптомы после разрыва.
- Конкурирующая гипотеза: стресс-ответ
- Разрыв активирует HPA-ось и воспаление независимо от опиоидов. Опиоидная система — один из многих участников, а не главный механизм.
- Как проверить
- Фармакологические блокады: налтрексон должен предотвращать привязанность; бупренорфин должен облегчать отмену. Отсутствие эффекта указывает на неспецифичность опиоидной гипотезы.
⚠️ Конфаундер социальной изоляции: потеря сети, а не опиоидная отмена
Разрыв романтических отношений часто сопровождается потерей общих друзей, изменением социальных ритуалов и снижением социальной поддержки. Социальная изоляция сама по себе — мощный стрессор, активирующий воспалительные пути и дисрегулирующий HPA-ось.
Для изоляции специфического эффекта опиоидной системы необходимы исследования, контролирующие степень социальной изоляции после разрыва. Без такого контроля невозможно отличить эффект потери партнёра от эффекта потери социальной сети.
- Измерить социальную поддержку до и после разрыва
- Контролировать уровень социальной изоляции в анализе
- Сравнить людей с одинаковой изоляцией, но разной интенсивностью романтической привязанности
- Проверить, остаётся ли опиоидная гипотеза значимой после контроля социальных факторов
Связь между стилями привязанности и нейробиологией показывает, что люди с тревожной привязанностью могут быть более уязвимы к обоим механизмам: как к опиоидной дисрегуляции, так и к социальной изоляции после разрыва.
Конфликты в доказательной базе: где источники расходятся и что это означает для интерпретации
Научная литература по эндогенной опиоидной системе и социальному поведению содержит противоречия, требующие честного анализа для избежания селективного цитирования. Подробнее — в разделе Основы эпистемологии.
📊 Противоречие 1: Роль κ-опиоидных рецепторов в социальном поведении
Некоторые исследования предполагают, что κ-опиоидные рецепторы опосредуют аверсивные аспекты социального отвержения и дисфорию при отмене (S007), в то время как другие данные указывают на преимущественную роль μ-рецепторов. Это расхождение может отражать различия в экспериментальных парадигмах (острое vs. хроническое отвержение) или видовую специфичность (грызуны vs. приматы).
Необходимы прямые сравнительные исследования с селективными антагонистами κ- и μ-рецепторов — иначе мы остаёмся в ситуации, где каждая лаборатория описывает свой кусок слона.
🔬 Противоречие 2: Временная динамика восстановления опиоидной системы
Данные о скорости восстановления плотности опиоидных рецепторов после прекращения хронической стимуляции противоречивы. Некоторые исследования показывают нормализацию в течение 2–4 недель (S002), другие документируют персистирующие изменения в течение месяцев.
| Параметр | Быстрое восстановление | Медленное восстановление | Возможная причина расхождения |
|---|---|---|---|
| Временной горизонт | 2–4 недели | Месяцы | Индивидуальные различия в нейропластичности |
| Модель | Острая стимуляция | Хроническая стимуляция | Методологические различия в измерениях |
| Клинический вывод | Короткая «ломка» | Долгая дисфория | Нужны лонгитюдные данные на людях |
⚖️ Противоречие 3: Селективность опиоидной гипотезы расставания
Если расставание действительно вызывает синдром отмены опиоидов, почему не все люди переживают одинаковую интенсивность симптомов? Одна гипотеза: индивидуальные различия в базовой плотности опиоидных рецепторов и генетике рецепторов (полиморфизмы OPRM1).
Другая: социальная привязанность — многосистемный процесс, и опиоидная система — лишь один из компонентов. Стили привязанности, сформированные в детстве, могут модулировать чувствительность к социальной боли независимо от опиоидной системы.
- Генетический фактор (OPRM1)
- Полиморфизм A118G связан с различиями в чувствительности к опиоидам и социальной боли. Люди с вариантом G могут быть более уязвимы к «эмоциональной ломке».
- Контекстный фактор (история привязанности)
- Люди с надёжной привязанностью могут иметь более стабильный базовый уровень эндогенных опиоидов, что буферирует боль отвержения.
- Временной фактор (длительность связи)
- Чем дольше отношения, тем выше вероятность хронической вверх-регуляции опиоидной системы и, следовательно, более выраженный синдром отмены.
🔍 Противоречие 4: Опиоиды vs. другие нейротрансмиттеры
Большинство исследований социальной боли также указывают на роль дофамина, серотонина и окситоцина. Является ли опиоидная система первичной или вторичной? Или это вопрос неправильной постановки?
Вероятнее всего, социальная привязанность — это интегрированная система, где опиоиды, дофамин и окситоцин работают синергически. Нейробиология расставания включает активацию множества систем одновременно, и выделение одной как «главной» — это упрощение для исследовательских целей, а не описание реальности.
📋 Как интерпретировать эти конфликты
- Противоречия в науке — норма, а не признак слабости. Они указывают на границы текущего знания.
- Селективное цитирование в пользу одной гипотезы (например, «это просто опиоиды») — красный флаг. Честный анализ требует признания альтернативных объяснений.
- Экстраполяция от грызунов к людям требует осторожности. Человеческая социальная боль — более сложный феномен, чем лабораторная парадигма отвержения.
- Индивидуальные различия (генетика, история, контекст) часто игнорируются в пользу универсальных механизмов. Это ошибка.
Вывод: опиоидная гипотеза расставания имеет солидную нейробиологическую основу, но она описывает часть механизма, а не весь процесс. Использовать её как полное объяснение — значит совершить ошибку редукционизма.
