 🧠 Нейронаука
🧠 НейронаукаЗолотой стандарт синтеза научных доказательств в медицинеλ
Систематические обзоры и мета-анализы представляют высший уровень доказательности, объединяя результаты множественных исследований через прозрачные, воспроизводимые протоколы для получения надежных клинических рекомендаций.
Overview
Систематические обзоры и мета-анализы являются фундаментальными инструментами доказательной медицины, позволяющими систематически идентифицировать, отбирать, критически оценивать и синтезировать все релевантные исследования по конкретному вопросу. В отличие от нарративных обзоров, они следуют предопределенным протоколам, минимизируя систематические ошибки и обеспечивая воспроизводимость результатов. Мета-анализ как статистический метод объединяет количественные данные из независимых исследований, увеличивая статистическую мощность и разрешая противоречия между отдельными работами. Современные стандарты, такие как PRISMA 2020, обеспечивают прозрачность и полноту отчетности на всех этапах проведения обзора.
🛡️ Протокол Лапласа: Качество мета-анализа определяется качеством включенных исследований — объединение слабых работ не создает сильных доказательств. Критическая оценка методологии, анализ гетерогенности и публикационных смещений обязательны для корректной интерпретации результатов.
Reference Protocol
Научный фундамент
Доказательная база для критического анализа
Navigation Matrix
Подразделы
[abiogenesis]
Абиогенез
Научная теория о естественном происхождении жизни из простых химических соединений более 3,5 миллиардов лет назад через постепенную химическую эволюцию
Изучить
[cell-biology]
Клеточная биология
Клетка — наименьшая живая единица, содержащая все молекулы жизни. От одноклеточных организмов до триллионов клеток человеческого тела — изучаем структуру, функции и поведение основы всего живого.
Изучить
[evolution-genetics]
Эволюция и генетика
Биологическая эволюция — это процесс развития и изменения живой природы на протяжении миллионов лет, благодаря которому возникло всё разнообразие жизни на нашей планете.
Изучить
[neuroscience]
Нейронаука
Междисциплинарная наука, изучающая структуру, функции и развитие нервной системы, от молекулярных механизмов до поведения и познания человека.
Изучить
Protocol: Evaluation
Проверь себя
Квизы по этой теме скоро появятся
Sector L1
Статьи
Научно-исследовательские материалы, эссе и глубокие погружения в механизмы критического мышления.
 🧠 Нейронаука
🧠 Нейронаука 🧬 Эволюция и генетика
🧬 Эволюция и генетика 🧠 Нейронаука
🧠 Нейронаука 🧬 Эволюция и генетика
🧬 Эволюция и генетика 🧬 Эволюция и генетика
🧬 Эволюция и генетика 🧬 Эволюция и генетика
🧬 Эволюция и генетика 🧠 Нейронаука
🧠 Нейронаука 🧬 Эволюция и генетика
🧬 Эволюция и генетика 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧬 Эволюция и генетика
🧬 Эволюция и генетика⚡
Подробнее
Методология систематических обзоров: от хаоса литературы к воспроизводимому протоколу
Систематические обзоры — высшая ступень иерархии научных доказательств. Они отличаются от нарративных обзоров строгой методологией: предварительная регистрация протокола, исчерпывающий поиск по множественным базам данных, прозрачная документация каждого решения.
Ключевое отличие: минимизация систематических ошибок через явные критерии включения и исключения, установленные до начала поиска. Это предотвращает субъективный отбор источников, который неизбежен в традиционных литературных обзорах.
Протоколы и регистрация: PRISMA-P как страховка от постфактум-манипуляций
Проспективная регистрация протокола в реестрах типа PROSPERO — критический механизм предотвращения селективной отчётности. PRISMA-P 2015 предоставляет 17-пунктовый чеклист для разработки протокола до начала обзора: исследовательский вопрос, критерии отбора, стратегия поиска, методы синтеза.
Регистрация создаёт публичный след намерений исследователей, делая невозможным скрытое изменение первичных исходов или критериев включения после ознакомления с результатами.
PRISMA 2020 расширил чеклист до 27 пунктов: отдельные требования к абстрактам, диаграммам потока, поправкам протокола, оценке достоверности доказательств и прозрачности финансирования. Соблюдение PRISMA не гарантирует качество, но обеспечивает минимальную прозрачность для критической оценки методологической строгости.
Стратегии поиска: от inception до последнего байта
Комплексная стратегия поиска требует систематического охвата множественных баз данных. Типичный протокол включает CENTRAL, MEDLINE и Embase с поиском от момента создания базы до определённой даты.
- Прозрачность поисковых терминов
- Полные поисковые строки для каждой базы данных, булевы операторы, фильтры — всё должно быть опубликовано для воспроизводимости.
- Расширенный поиск
- Ручной просмотр списков литературы ключевых статей, контакты с экспертами, поиск неопубликованных данных для минимизации публикационного смещения.
Систематический поиск выходит за рамки электронных баз данных. Это комбинированный подход, где каждый источник документируется и обосновывается в протоколе.
Мета-анализ и статистический синтез: когда цифры говорят громче слов
Мета-анализ — статистическая техника объединения количественных данных из множественных независимых исследований для получения единой оценки эффекта с повышенной статистической мощностью. В отличие от систематического обзора, который может быть качественным, мета-анализ всегда количественный и требует числовых данных, пригодных для статистического пулирования.
Критическое преимущество: разрешение неопределённостей, когда отдельные исследования противоречат друг другу, и выявление эффектов, незаметных в малых выборках.
Модели фиксированных и случайных эффектов: философия вариабельности
Модель фиксированного эффекта предполагает, что все включённые исследования оценивают один истинный эффект, а различия между ними обусловлены только случайной ошибкой выборки. Модель случайных эффектов допускает, что истинный эффект варьирует между исследованиями из-за различий в популяциях, вмешательствах или дизайне.
| Модель | Предположение | Доверительный интервал |
|---|---|---|
| Фиксированный эффект | Один истинный эффект; вариация = случайная ошибка | Уже при гетерогенности |
| Случайные эффекты | Истинный эффект варьирует между исследованиями | Шире; отражает дополнительную неопределённость |
Мета-анализ связи ИМТ с риском рака молочной железы выявил противоположные эффекты при стратификации по менопаузальному статусу: повышение риска у постменопаузальных женщин и снижение у пременопаузальных. Исследование нейронаучного обучения боли показало, что продолжительность вмешательства значимо влияет на размер эффекта, объясняя часть гетерогенности между исследованиями.
Гетерогенность и публикационные смещения: детективная работа с данными
Статистика I² количественно оценивает долю вариабельности между исследованиями, обусловленную истинной гетерогенностью: значения 25%, 50% и 75% интерпретируются как низкая, умеренная и высокая гетерогенность соответственно. Высокая гетерогенность не дисквалифицирует мета-анализ, но требует исследования через подгрупповой и модераторный анализ.
- Идентифицировать источники вариабельности между исследованиями
- Провести анализ чувствительности, исключив работы с высоким риском систематических ошибок
- Проверить робастность выводов к методологическому качеству
Публикационное смещение возникает, когда исследования с положительными результатами публикуются чаще, чем с отрицательными, искажая пулированную оценку эффекта в сторону преувеличения. Воронкообразные графики визуализируют асимметрию распределения размеров эффекта, а статистические тесты Эггера и Бегга формально проверяют наличие смещения.
Включение неопубликованных данных через контакты с исследователями и поиск в реестрах клинических испытаний частично смягчает публикационное смещение, но полностью устранить его невозможно.
Сетевой мета-анализ: многомерная шахматная партия вмешательств
Сетевой мета-анализ расширяет традиционный парный мета-анализ, позволяя одновременно сравнивать множественные вмешательства даже при отсутствии прямых head-to-head сравнений между всеми парами. Методология использует как прямые доказательства из исследований, напрямую сравнивающих два вмешательства, так и непрямые доказательства через общий компаратор, создавая связную сеть сравнений.
Критическое преимущество — возможность ранжирования всех доступных вмешательств по эффективности и безопасности, информируя клинические решения в условиях множественных терапевтических опций.
Непрямые сравнения и транзитивность: логика переходных умозаключений
Непрямое сравнение вмешательств A и C через общий компаратор B основывается на предположении транзитивности: если A превосходит B, а B превосходит C, то A должно превосходить C. Валидность непрямых сравнений критически зависит от сходства исследований по модификаторам эффекта — характеристикам, которые могут влиять на относительную эффективность вмешательств.
Нарушение транзитивности происходит, когда исследования, сравнивающие A с B, систематически отличаются от исследований, сравнивающих B с C, по популяции, дозировке или сопутствующим вмешательствам.
- Статистика несогласованности
- Проверяет предположение транзитивности через оценку согласованности между прямыми и непрямыми доказательствами. Значимое расхождение сигнализирует о потенциальных нарушениях.
- Анализ чувствительности
- Исключает узлы сети с высоким риском нарушения транзитивности, проверяя робастность ранжирования вмешательств.
Протокол RAIN (systematic Review and Artificial Intelligence Network meta-analysis) для COVID-19 демонстрирует применение сетевого мета-анализа к быстро эволюционирующей доказательной базе с множественными терапевтическими кандидатами.
Ранжирование вмешательств: от вероятностей к клиническим решениям
Сетевой мета-анализ генерирует вероятностное ранжирование вмешательств через SUCRA (Surface Under the Cumulative Ranking curve) — метрику, где значение 100% указывает на наивысшую вероятность быть лучшим вмешательством, а 0% — худшим. Ранжирование учитывает не только точечные оценки эффекта, но и неопределённость: вмешательство с умеренным эффектом и узким доверительным интервалом может ранжироваться выше, чем с большим эффектом, но широким интервалом.
Вмешательство, оптимальное в среднем по сети, может быть неоптимальным для конкретной подгруппы пациентов. Стратификация по клиническим характеристикам критична для перевода ранжирования в действие.
Мета-анализ анти-VEGF терапий для макулярной дегенерации иллюстрирует клиническую ценность: ранжирование по эффективности и безопасности одновременно информирует выбор между афлиберцептом, ранибизумабом и бевацизумабом.
Интеграция искусственного интеллекта в сетевой мета-анализ, как предложено в протоколе RAIN, автоматизирует извлечение данных и оценку риска систематических ошибок, ускоряя синтез доказательств в условиях пандемии. Исследование инозитола при СПКЯ демонстрирует важность стратификации: мио-инозитол показал превосходство над D-хиро-инозитолом для репродуктивных исходов, но комбинация оказалась оптимальной для метаболических параметров.
Стандарты отчетности PRISMA 2020: от чеклиста к прозрачности синтеза
PRISMA 2020 — обновленный набор рекомендаций, заменивший версию 2009 года. 27-пунктовый чеклист охватывает все этапы: от формулировки вопроса по структуре PICO до интерпретации результатов с учетом ограничений.
Ключевое отличие: расширенные требования к описанию методов поиска, оценке достоверности доказательств и отчетности о синтезе данных. Это повышает воспроизводимость и позволяет читателю проверить каждый шаг логики авторов.
27-пунктовый чеклист и диаграммы потока данных
Чеклист структурирован по разделам: название, аннотация, введение, методы, результаты, обсуждение, финансирование. Каждый раздел содержит конкретные требования к отчетности.
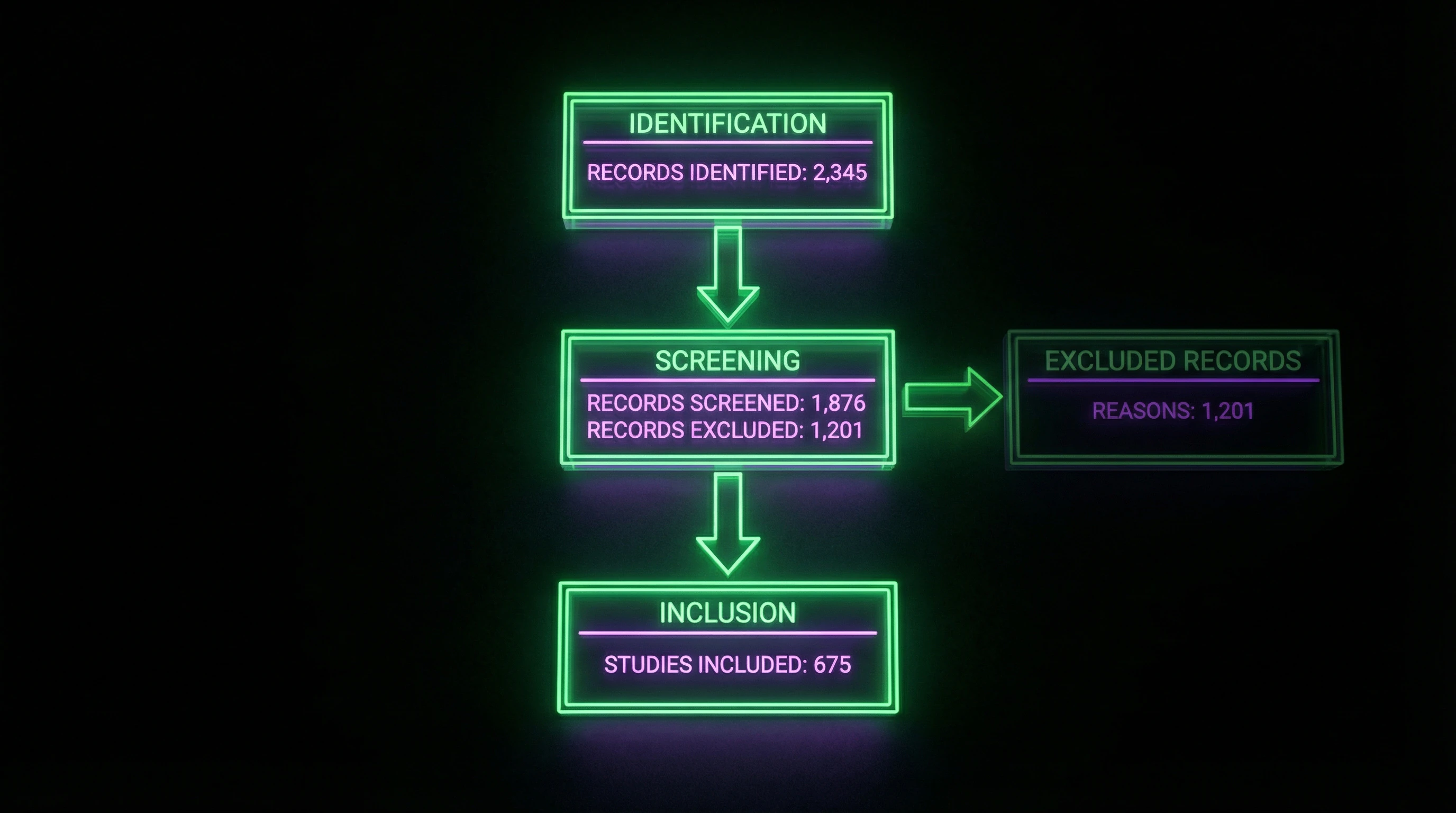
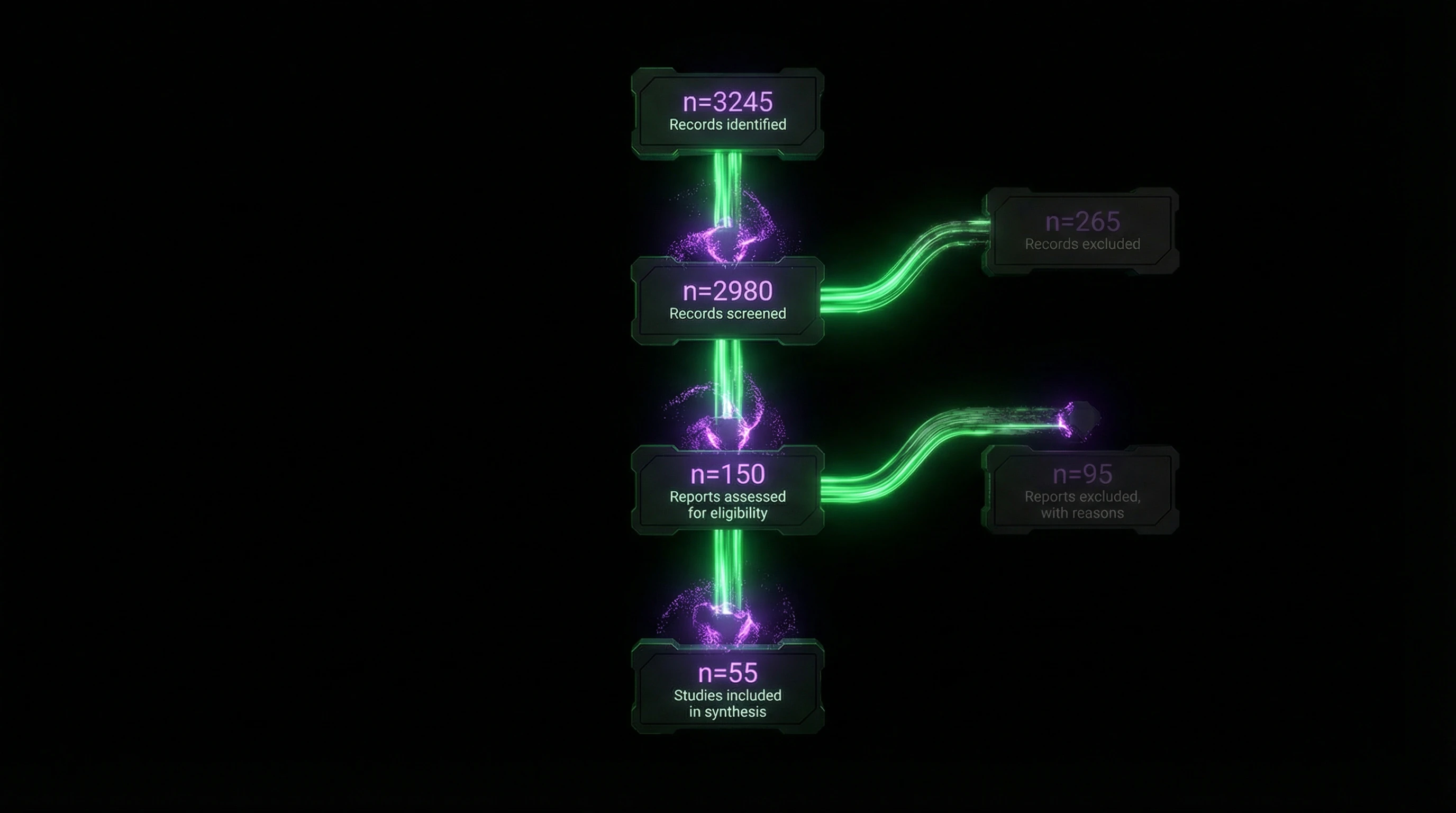
Диаграмма потока визуализирует процесс отбора: количество записей, идентифицированных через базы данных → исключенные на скрининге → оцененные на соответствие → окончательно включенные в синтез. Пример: обзор по нейронауке боли начался с 6850 записей, но только 37 исследований соответствовали критериям включения.
Диаграмма потока — не украшение. Это протокол проверки: читатель видит, где и почему исследования отсеялись, и может оценить, не потеряны ли релевантные работы.
Отдельный чеклист для аннотаций обеспечивает краткое, но полное представление ключевых элементов обзора в структурированном формате — критично для быстрого скрининга читателем.
Отличия от PRISMA 2009 и расширенные требования
PRISMA 2020 требует полные поисковые запросы для всех баз данных и дату последнего поиска — этого не было в 2009 году. Это позволяет другому исследователю воспроизвести поиск или обновить обзор.
- Оценка риска систематических ошибок
- Теперь обязательно указывать инструменты и методы, использованные для критической оценки, с представлением результатов для каждого включенного исследования. В 2009 году это часто описывалось размыто.
- Достоверность доказательств (GRADE)
- Новая версия требует явного указания системы оценки (например, GRADE) и обсуждения ограничений на уровне отдельных исследований и обзора в целом.
- PRISMA-P 2015
- Дополняет основной чеклист 17-пунктовым руководством для протоколов. Подчеркивает важность предварительной регистрации методологии в базах типа PROSPERO — это предотвращает p-hacking и селективную отчетность.
Регистрация протокола до начала обзора — это не бюрократия. Это гарантия, что авторы не переписали методы задним числом под результаты.
Оценка риска систематических ошибок: от инструментов к интерпретации
Объединение низкокачественных данных не производит высококачественных доказательств. Риск систематических ошибок оценивается по множественным доменам: рандомизация, сокрытие распределения, ослепление участников и оценщиков исходов, полнота данных и селективная отчетность.
В обзоре по образованию о нейронауке боли 78% исследований имели высокий риск систематических ошибок из-за невозможности ослепления при образовательных вмешательствах. Систематическая документация оценки для каждого исследования позволяет читателям судить о надежности выводов.
Инструменты критической оценки и домены риска
Cochrane Risk of Bias (RoB 2) структурирует оценку рандомизированных контролируемых исследований по пяти доменам: процесс рандомизации, отклонения от запланированных вмешательств, отсутствующие данные исходов, измерение исходов и селективная отчетность.
| Инструмент | Тип исследований | Ключевые домены |
|---|---|---|
| RoB 2 | Рандомизированные контролируемые | Рандомизация, ослепление, полнота данных, селективная отчетность |
| ROBINS-I | Нерандомизированные | Искажение конфаундеров, отбор участников, классификация вмешательств |
Каждый домен оценивается как низкий, некоторый или высокий риск на основе сигнальных вопросов, с общей оценкой, отражающей наихудший домен. Для нерандомизированных исследований ROBINS-I учитывает дополнительные источники систематических ошибок.
Интерпретация результатов с учетом методологического качества
Высокая гетерогенность между исследованиями часто объясняется различиями в методологическом качестве. Анализ чувствительности с исключением исследований высокого риска выявляет, переоценены ли эффекты.
В мета-анализе образования о нейронауке боли эффект на интенсивность боли сохранялся только при включении исследований низкого риска систематических ошибок — указание на переоценку эффекта в низкокачественных исследованиях.
Система GRADE (Grading of Recommendations Assessment, Development and Evaluation) интегрирует оценку риска систематических ошибок с непоследовательностью, косвенностью, неточностью и систематическими ошибками публикации для определения общей достоверности доказательств.
- Оценить риск систематических ошибок по доменам (рандомизация, ослепление, полнота данных)
- Провести анализ чувствительности, исключив исследования высокого риска
- Применить GRADE для интеграции качества с другими факторами неопределенности
- Документировать ограничения для клиницистов и разработчиков рекомендаций
Практическое применение и ограничения: от статистики к клинике
Статистическая значимость в мета-анализе не всегда соответствует клинической значимости. Объединение больших выборок может выявлять минимальные эффекты, не имеющие практической ценности.
В обзоре по образованию о нейронауке боли стандартизированная разница средних −0,26 для интенсивности боли была статистически значимой, но не достигала порога минимально клинически важного различия в 1,5 балла по 10-балльной шкале.
Продолжительность вмешательства значимо влияла на размер эффекта: программы длительностью более 30 минут показывали клинически значимое снижение боли, тогда как короткие вмешательства — нет.
Это подчеркивает необходимость интерпретации результатов в контексте минимальных клинически важных различий, специфичных для каждого исхода и популяции.
Клиническая значимость против статистической значимости
Доверительные интервалы объединенных оценок эффекта информируют о точности и клинической интерпретации. Широкие интервалы, пересекающие порог клинической значимости, указывают на неопределенность практической ценности вмешательства.
В сетевом мета-анализе инозитола при синдроме поликистозных яичников мио-инозитол показал отношение шансов 2,38 (95% ДИ 1,43–3,95) для восстановления овуляции по сравнению с плацебо — как статистически, так и клинически значимое улучшение.
| Исход | Вмешательство | Эффект | Интерпретация |
|---|---|---|---|
| Восстановление овуляции | Мио-инозитол vs плацебо | ОШ 2,38 (95% ДИ 1,43–3,95) | Статистически и клинически значимо |
| Метаболические исходы | Мио- + D-хиро-инозитол (40:1) | Превосходство подтверждено | Требует стратификации по типам исходов |
Гетерогенность эффектов между подгруппами (I² > 50%) требует осторожности в обобщении результатов и может указывать на необходимость индивидуализированного подхода к лечению.
Роль искусственного интеллекта в автоматизации синтеза доказательств
Интеграция искусственного интеллекта в систематические обзоры автоматизирует трудоемкие этапы: скрининг названий и аннотаций, извлечение данных и оценку риска систематических ошибок. Машинное обучение может сократить время скрининга на 30–70% при сохранении чувствительности выше 95%.
Автоматизация требует валидации: алгоритмы обучаются на существующих данных и могут воспроизводить систематические ошибки обучающих наборов или пропускать исследования с нестандартной терминологией.
В диагностическом мета-анализе ИИ-ассистированной идентификации паращитовидных желез объединенная чувствительность составила 93,8%, но гетерогенность между исследованиями (I² = 89%) указывала на вариабельность алгоритмов и необходимость стандартизации.
- Живые систематические обзоры, непрерывно обновляемые с помощью ИИ-мониторинга новых публикаций, представляют будущее синтеза доказательств в быстро развивающихся областях.
- Требуется прозрачная отчетность о роли автоматизации в каждом этапе процесса.
- Критично для быстрого синтеза доказательств в условиях пандемии и других кризисных ситуаций.

Knowledge Access Protocol
FAQ
Часто задаваемые вопросы
Систематический обзор — это исследование, использующее строгие предопределённые методы для поиска, отбора и анализа всех релевантных исследований по конкретному вопросу. В отличие от нарративных обзоров, он следует чётким протоколам (например, PRISMA), минимизирует субъективность и обеспечивает воспроизводимость результатов. Это делает систематические обзоры высшим уровнем доказательности в медицине.
Мета-анализ — это статистический метод объединения количественных данных из нескольких независимых исследований для получения единой оценки эффекта. Он увеличивает статистическую мощность и помогает разрешить противоречия между отдельными исследованиями. Применяется в клинической медицине, эпидемиологии и нейронауках для получения более точных выводов.
PRISMA 2020 — это обновлённый стандарт отчётности для систематических обзоров, включающий 27-пунктовый чеклист, чеклист для аннотаций и диаграммы потока. Он заменил версию 2009 года и обеспечивает прозрачность, полноту и воспроизводимость публикаций. Соблюдение PRISMA повышает качество и доверие к результатам обзоров.
Нет, систематические обзоры могут содержать систематические ошибки, несмотря на строгую методологию. Публикационные смещения, низкое качество включённых исследований и неполный поиск литературы могут исказить выводы. Поэтому критическая оценка риска ошибок и анализ чувствительности обязательны для правильной интерпретации.
Высокая гетерогенность между исследованиями требует осторожной интерпретации. Модераторный и подгрупповой анализы помогают выявить источники различий (например, дозировка, длительность, характеристики популяции). Если гетерогенность необъяснима, объединение данных может быть некорректным, и следует ограничиться качественным синтезом.
Проспективная регистрация протокола (например, в PROSPERO) предотвращает выборочную публикацию результатов и постфактум изменения методологии. Это повышает прозрачность и снижает риск манипуляций данными. PRISMA-P 2015 подчёркивает необходимость разработки протокола до начала обзора для обеспечения научной строгости.
Необходимо систематически искать в нескольких базах данных (MEDLINE, Embase, CENTRAL) от начала их существования до определённой даты. Поисковые запросы должны быть прозрачно задокументированы, включая ключевые слова и фильтры. Дополнительно проверяются списки литературы найденных статей и серая литература для полноты охвата.
Сетевой мета-анализ позволяет одновременно сравнивать несколько вмешательств, даже при отсутствии прямых сравнений между ними. Он использует непрямые сравнения через общий компаратор и позволяет ранжировать методы лечения. Применяется для оптимизации выбора терапии при множестве доступных опций.
Используются стандартизированные инструменты критической оценки для выявления методологических ограничений (рандомизация, ослепление, полнота данных). Оценка риска ошибок информирует интерпретацию результатов и помогает определить надёжность выводов. Исследования с высоким риском могут быть исключены в анализе чувствительности.
Модель фиксированных эффектов предполагает единый истинный эффект во всех исследованиях, а модель случайных эффектов допускает вариабельность эффектов между исследованиями. При наличии гетерогенности модель случайных эффектов более консервативна и даёт более широкие доверительные интервалы. Выбор модели зависит от статистических тестов гетерогенности.
Нет, мета-анализ не всегда эквивалентен крупному РКИ. Он объединяет данные с разными протоколами, популяциями и качеством, что может вносить систематические ошибки. Хорошо спланированное крупное исследование часто предпочтительнее, особенно при высокой гетерогенности или низком качестве доступных данных.
Нет, статистическая значимость не гарантирует клиническую значимость. Большой размер выборки в мета-анализе может выявить минимальные эффекты, не имеющие практического значения. Необходимо оценивать величину эффекта, доверительные интервалы и клинический контекст для определения реальной пользы.
ИИ автоматизирует трудоёмкие этапы: скрининг заголовков, извлечение данных, оценку риска ошибок. Это ускоряет процесс и снижает человеческие ошибки, но требует валидации. Примеры включают ИИ-ассистированную идентификацию паращитовидных желёз и автоматический анализ диагностической точности.
Модераторный анализ исследует, как величина эффекта зависит от характеристик исследований (дозировка, длительность, популяция). Например, эффект обучения нейронауке боли может различаться в зависимости от продолжительности вмешательства. Это помогает оптимизировать клинические рекомендации и понять источники гетерогенности.
Технически возможно, но требует осторожности из-за различий в риске ошибок между дизайнами (РКИ vs наблюдательные). Обычно предпочтительно объединять исследования одного типа, а разные дизайны анализировать отдельно или в подгруппах. Смешивание может увеличить гетерогенность и затруднить интерпретацию.
Публикационное смещение (предпочтительная публикация положительных результатов) может завышать оценки эффекта. Используются воронкообразные графики, тесты Эггера и методы коррекции (trim-and-fill). При значительном смещении выводы следует формулировать осторожно, указывая на возможную переоценку эффекта.
