 🧠 Нейронаука
🧠 НейронаукаНейронаука: Исследование Мозга и Нервной Системыλ
Междисциплинарная наука, изучающая структуру, функции и развитие нервной системы, от молекулярных механизмов до поведения и познания человека.
Overview
Нейронаука объединяет биологию, физику, химию и информатику, чтобы расшифровать 🧠 работу мозга — от молекулярных механизмов до сознания. Современные технологии (фМРТ, ПЭТ-сканирование) позволяют наблюдать активность нейронных сетей в реальном времени и понимать, как формируются память, эмоции, решения. Результаты применяются в медицине, образовании, разработке ИИ и когнитивной терапии.
🛡️
Протокол Лапласа: Нейронаука основывается на строгих экспериментальных методах и воспроизводимых результатах, отделяя научно обоснованные знания о мозге от популярных мифов и псевдонаучных утверждений о его работе.
Reference Protocol
Научный фундамент
Доказательная база для критического анализа
Protocol: Evaluation
Проверь себя
Квизы по этой теме скоро появятся
Sector L1
Статьи
Научно-исследовательские материалы, эссе и глубокие погружения в механизмы критического мышления.
 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука 🧠 Нейронаука
🧠 Нейронаука⚡
Подробнее
Архитектура нервной системы: от молекулярных машин до глобальных сетей
Нервная система — иерархическая структура, где миллиарды специализированных клеток координируют все процессы организма от автоматических рефлексов до абстрактного мышления. Нейроны передают информацию на расстояния от микрометров до метров со скоростью до 120 м/с благодаря уникальной морфологии и электрохимическим свойствам.
Человеческий мозг содержит приблизительно 86 миллиардов нейронов, каждый формирует в среднем 7000 синаптических контактов. Эта сеть создаёт основу для всех когнитивных процессов.
Нейроны и синаптическая передача: молекулярная логика коммуникации
Нейрон состоит из сомы (тело клетки), дендритов (приём сигналов) и аксона (передача). Информация кодируется потенциалами действия — стереотипными электрическими импульсами амплитудой около 100 мВ и длительностью 1–2 мс, возникающими при деполяризации мембраны выше порога −55 мВ.
Генерация потенциала действия обеспечивается каскадным открытием потенциал-зависимых натриевых каналов, пропускающих до 10⁷ ионов Na⁺ в секунду через один канал. Миелиновая оболочка увеличивает скорость проведения в 5–50 раз благодаря сальтаторному механизму — прыжкообразному распространению возбуждения между перехватами Ранвье.
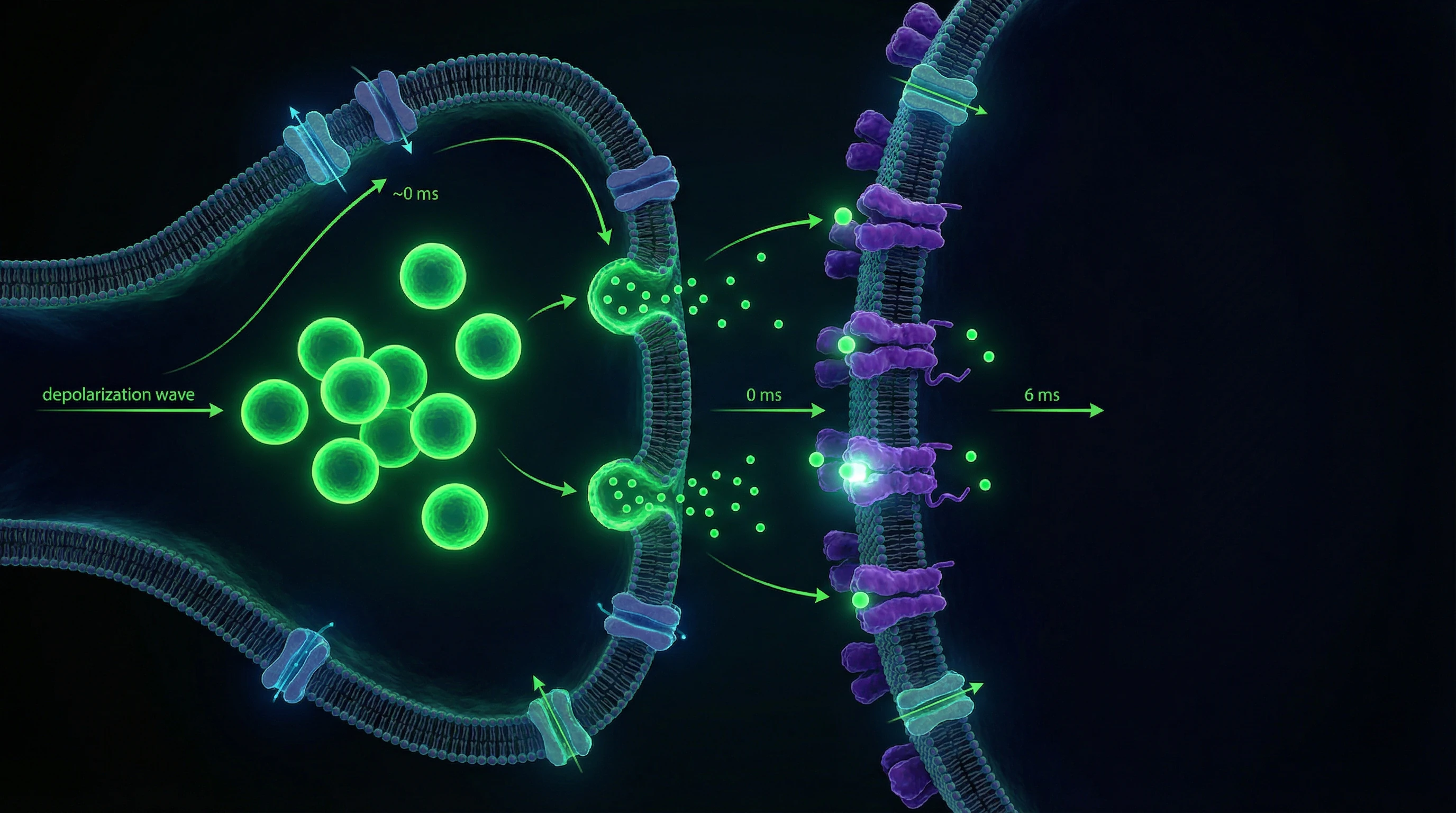
Синаптическая передача осуществляется преимущественно химическим путём через высвобождение нейромедиаторов в синаптическую щель шириной 20–40 нм. Прибытие потенциала действия в пресинаптическое окончание открывает потенциал-зависимые кальциевые каналы; вход Ca²⁺ запускает экзоцитоз синаптических везикул за 0,2–0,5 мс.
- Квант медиатора
- Содержимое одной синаптической везикулы; типичный синапс высвобождает 1–5 квантов на импульс с вероятностью 0,1–0,9.
- Глутамат
- Основной возбуждающий медиатор (80–90% синапсов ЦНС); его баланс с ГАМК определяет возбудимость нейронных сетей.
- ГАМК
- Основной тормозной медиатор (10–20% синапсов); критична для предотвращения гипервозбудимости.
Центральная и периферическая нервная система: функциональное разделение труда
ЦНС включает головной мозг (масса 1300–1400 г) и спинной мозг (длина 40–45 см, 31 сегмент), защищённые костными структурами и тремя мозговыми оболочками. Кора больших полушарий содержит 16–20 миллиардов нейронов, организованных в шесть слоёв толщиной 1,5–4,5 мм; общая площадь коры при разглаживании составляет 1800–2300 см².
| Структура | Функция | Механизм |
|---|---|---|
| Базальные ганглии | Контроль движений | Отбор и инициация моторных программ |
| Гиппокамп | Консолидация памяти | Кодирование эпизодических событий |
| Миндалина | Эмоциональные реакции | Оценка угрозы и награды |
| Спинной мозг | Рефлексы и моторика | Латентность 30–50 мс через 31 пару нервов |
ПНС состоит из 12 пар черепных и 31 пары спинномозговых нервов, разделяясь на соматическую систему (произвольный контроль скелетных мышц) и автономную систему (непроизвольная регуляция внутренних органов).
- Симпатический отдел (норадреналин): реакция «бей или беги» — увеличивает ЧСС с 60–80 до 120–180 уд/мин, перераспределяет кровоток к мышцам (до 80% сердечного выброса), мобилизует энергетические резервы.
- Парасимпатический отдел (ацетилхолин): режим «отдых и восстановление» — стимулирует пищеварение, снижает ЧСС, активирует анаболические процессы.
- Энтеральная нервная система: 200–600 миллионов нейронов кишечника функционируют автономно и двунаправленно взаимодействуют с ЦНС через блуждающий нерв.
Методы исследования мозга: от электродов до молекулярных меток
Современная нейронаука использует мультимодальный подход, комбинируя методы с различным пространственным (от нанометров до сантиметров) и временным (от микросекунд до лет) разрешением. Прорывы последних десятилетий — функциональная МРТ (1990-е), оптогенетика (2005), двухфотонная микроскопия in vivo (2000-е), коннектомика (2010-е) — позволили перейти от корреляционных наблюдений к причинно-следственному анализу нейронных механизмов.
Интеграция данных разных масштабов через вычислительное моделирование создаёт многоуровневые карты мозга от молекул до поведения.
Нейровизуализация и электрофизиология: наблюдение за живым мозгом
Функциональная МРТ (фМРТ) детектирует изменения кровотока через BOLD-сигнал (blood oxygen level dependent) с пространственным разрешением 1–3 мм и временным 1–2 с, позволяя картировать активность всего мозга неинвазивно. Активация нейронов увеличивает локальный кровоток на 20–40% с задержкой 4–6 с, превышая потребность в кислороде (нейроваскулярное сопряжение), что создаёт контраст между активными и неактивными зонами.
Позитронно-эмиссионная томография (ПЭТ) использует радиоактивные трейсеры для визуализации метаболизма глюкозы (¹⁸F-FDG), нейромедиаторных систем (¹¹C-raclopride для дофамина), амилоидных бляшек при болезни Альцгеймера с чувствительностью до пикомолярных концентраций.
| Метод | Пространственное разрешение | Временное разрешение | Преимущество |
|---|---|---|---|
| фМРТ | 1–3 мм | 1–2 с | Целый мозг, неинвазивно |
| ПЭТ | 2–4 мм | Минуты | Молекулярные маркеры (метаболизм, рецепторы) |
| МЭГ | 2–5 мм | 1 мс | Высокое временное разрешение, неинвазивно |
| ЭЭГ | 5–10 см | 1 мс | Портативность, низкая стоимость |
Магнитоэнцефалография (МЭГ) регистрирует магнитные поля 10–100 фемтотесла, генерируемые синхронной активностью 10⁴–10⁵ нейронов, с временным разрешением 1 мс и локализацией источников с точностью 2–5 мм.
Электроэнцефалография (ЭЭГ) измеряет суммарную электрическую активность через 19–256 электродов на скальпе, выявляя ритмы: дельта (0,5–4 Гц, глубокий сон), тета (4–8 Гц, медитация), альфа (8–13 Гц, расслабленное бодрствование), бета (13–30 Гц, активное мышление), гамма (30–100 Гц, когнитивная интеграция).
Patch-clamp техника достигает разрешения единичных ионных каналов (проводимость 1–100 пикосименс), позволяя анализировать синаптические токи амплитудой 5–50 пА с точностью до микросекунд — это граница между макроскопией и молекулярной физикой.
Многоканальные электродные матрицы (до 1024 каналов) регистрируют активность сотен нейронов одновременно in vivo, выявляя паттерны популяционного кодирования и нейронные ансамбли, коррелирующие с поведением.
Молекулярные и генетические подходы: манипуляция нейронными цепями
Оптогенетика использует светочувствительные белки (channelrhodopsin-2 активируется синим светом 470 нм, halorhodopsin — жёлтым 580 нм) для контроля активности генетически определённых популяций нейронов с миллисекундной точностью. Экспрессия опсинов под промоторами специфических генов (например, CaMKIIα для возбуждающих нейронов, GAD67 для тормозных) позволяет селективно активировать или ингибировать клеточные типы, доказывая их причинную роль в поведении.
Хемогенетика (DREADD — designer receptors exclusively activated by designer drugs) обеспечивает фармакологический контроль нейронной активности: синтетический лиганд клозапин-N-оксид (CNO, 1–10 мг/кг) активирует инертные рецепторы, модулируя активность целевых нейронов на часы. Вирусные векторы (AAV, lentivirus) доставляют генетические конструкции с эффективностью трансдукции 60–90% в целевую область объёмом 0,5–2 мм³.
- Оптогенетика: свет → опсин → ионный канал → нейрон активен/неактивен (миллисекунды)
- Хемогенетика: CNO → синтетический рецептор → модуляция активности (часы)
- CRISPR/Cas9: редактирование генома → нокаут гена → моделирование болезни (постоянно)
- Вирусные векторы: доставка конструкции в целевую область (60–90% эффективность)
CRISPR/Cas9 редактирование генома позволяет создавать нокауты специфических генов в нейронах с эффективностью 40–80%, моделируя генетические варианты, ассоциированные с неврологическими заболеваниями.
Транскриптомика единичных клеток (scRNA-seq) выявила более 100 молекулярно различных типов нейронов в коре, каждый с уникальным профилем экспрессии 15000–20000 генов, переопределяя классификацию клеток мозга.
Коннектомика реконструирует полные карты синаптических связей: коннектом C. elegans (302 нейрона, 7000 синапсов) завершён в 1986, мышиный кортикальный кубик 1 мм³ (100000 нейронов, 10⁹ синапсов) — в 2021 с использованием серийной электронной микроскопии и машинного обучения. Это переход от описания к полной топографии.
Кальциевая визуализация с индикаторами GCaMP6 (ΔF/F до 1000% при активности) позволяет регистрировать активность 1000–10000 нейронов одновременно in vivo через имплантированные микроскопы (1–2 г) или двухфотонную микроскопию через черепное окно.
Когнитивная нейронаука: нейронные коды разума
Когнитивная нейронаука изучает нейронные механизмы высших психических функций — восприятия, внимания, памяти, языка, принятия решений, сознания. Ключевая концепция — нейронное кодирование: информация представлена паттернами активности популяций нейронов, где значение определяется не отдельными клетками, а распределённой активностью ансамблей из 10²-10⁴ нейронов.
Временная динамика не менее важна, чем частота импульсации: информация кодируется в точном тайминге спайков относительно тета-ритма (4-8 Гц) гиппокампа с точностью до 10-20 мс.
Механизмы памяти и обучения: от синапсов до систем
Долговременная потенциация (LTP) — устойчивое усиление синаптической передачи на 100-400% после высокочастотной стимуляции (100 Гц, 1 с) — считается клеточным механизмом памяти. LTP в гиппокампе требует активации NMDA-рецепторов, пропускающих Ca²⁺ только при одновременной деполяризации и связывании глутамата (детектор совпадения Хебба).
Каскад активации: CaMKII → фосфорилирование AMPA-рецепторов → увеличение их числа в синапсе (с 20 до 80 рецепторов за 15-30 мин). Поздняя фаза LTP (L-LTP, >3 ч) требует синтеза белков de novo через активацию CREB-зависимой транскрипции, увеличивая размер дендритных шипиков на 30-60% и стабилизируя изменения на дни-месяцы.
| Процесс | Стимуляция | Эффект | Функция |
|---|---|---|---|
| LTP | 100 Гц, 1 с | Усиление на 100-400% | Обучение, запоминание |
| LTD | 1 Гц, 15 мин | Ослабление на 30-50% | Забывание, рефинирование |
Долговременная депрессия (LTD) — противоположный процесс ослабления синапсов при низкочастотной стимуляции — обеспечивает забывание и рефинирование нейронных цепей.
Консолидация памяти переносит информацию из гиппокампа в неокортекс за недели-месяцы через реактивацию нейронных паттернов во время сна. Во время медленноволнового сна гиппокампальные «replay» воспроизводят дневные последовательности активности в сжатом времени (компрессия в 6-20 раз), синхронизируясь с кортикальными веретёнами (12-15 Гц, 0,5-2 с) для переноса информации.
Нарушение сна в первые 6 ч после обучения снижает консолидацию на 30-50%, а оптогенетическое усиление реактивации улучшает память на 20-40%.
Рабочая память удерживает 4±1 элемент в префронтальной коре через устойчивую активность нейронов (10-30 Гц) в течение секунд-минут задержки, модулируемую дофамином (оптимум при умеренных уровнях, инвертированная U-кривая). Эпизодическая память кодируется «клетками места» гиппокампа (активны в специфических локациях, поле 20-50 см) и «клетками времени» (кодируют временные интервалы 1-30 с), формируя когнитивную карту пространства-времени.
Нейронные основы сознания: интеграция и глобальное рабочее пространство
Теория глобального нейронного рабочего пространства (Dehaene, Changeux) постулирует, что сознательное восприятие возникает при «воспламенении» распределённой сети префронтальных, париетальных и височных областей, транслирующих информацию через дальние кортико-кортикальные связи. Сознательные стимулы вызывают позднюю активность (>300 мс) с глобальной синхронизацией в гамма-диапазоне (30-80 Гц).
Подпороговые стимулы генерируют только локальную раннюю активность (<200 мс) без распространения. Повреждение префронтальной коры или таламических ядер (интраламинарные ядра) нарушает сознание, подтверждая их роль в глобальной интеграции.
- Сознательный стимул → позднее глобальное воспламенение (>300 мс)
- Подпороговый стимул → локальная ранняя активность (<200 мс)
- Повреждение префронтальной коры → нарушение интеграции
- Повреждение таламических ядер → потеря сознания
Теория интегрированной информации (Tononi) количественно определяет сознание через Φ (phi) — меру причинно-следственной интеграции системы: высокое Φ требует баланса между функциональной специализацией модулей и их интеграцией, максимизируясь в таламо-кортикальной системе.
Нейронные корреляты сознания (NCC) — минимальные нейронные механизмы, достаточные для специфического сознательного опыта — локализованы в задних кортикальных «горячих зонах»: экстрастриарная зрительная кора (V2-V4) для зрительного осознания, височно-париетальная кора для телесного самосознания.
Бинокулярное соперничество показывает, что активность V1 коррелирует с физическим стимулом, а V4 и нижневисочной коры — с субъективным восприятием, указывая на V4 как критическую зону для визуального сознания.
Анестетики (пропофол, севофлуран) подавляют сознание, нарушая таламо-кортикальную связность и снижая сложность ЭЭГ (индекс пертурбационной сложности PCI с 0,5 в бодрствовании до 0,2 под анестезией), не затрагивая локальную активность.
Вегетативное состояние характеризуется сохранной метаболической активностью (50-60% нормы по ПЭТ), но фрагментированной функциональной связностью, тогда как состояние минимального сознания показывает частичное восстановление дальних связей и реакции на команды в 20-40% случаев.
Нейропластичность и Развитие — Как Мозг Перестраивается на Протяжении Жизни
Формирование нейронных связей через синаптогенез и прунинг
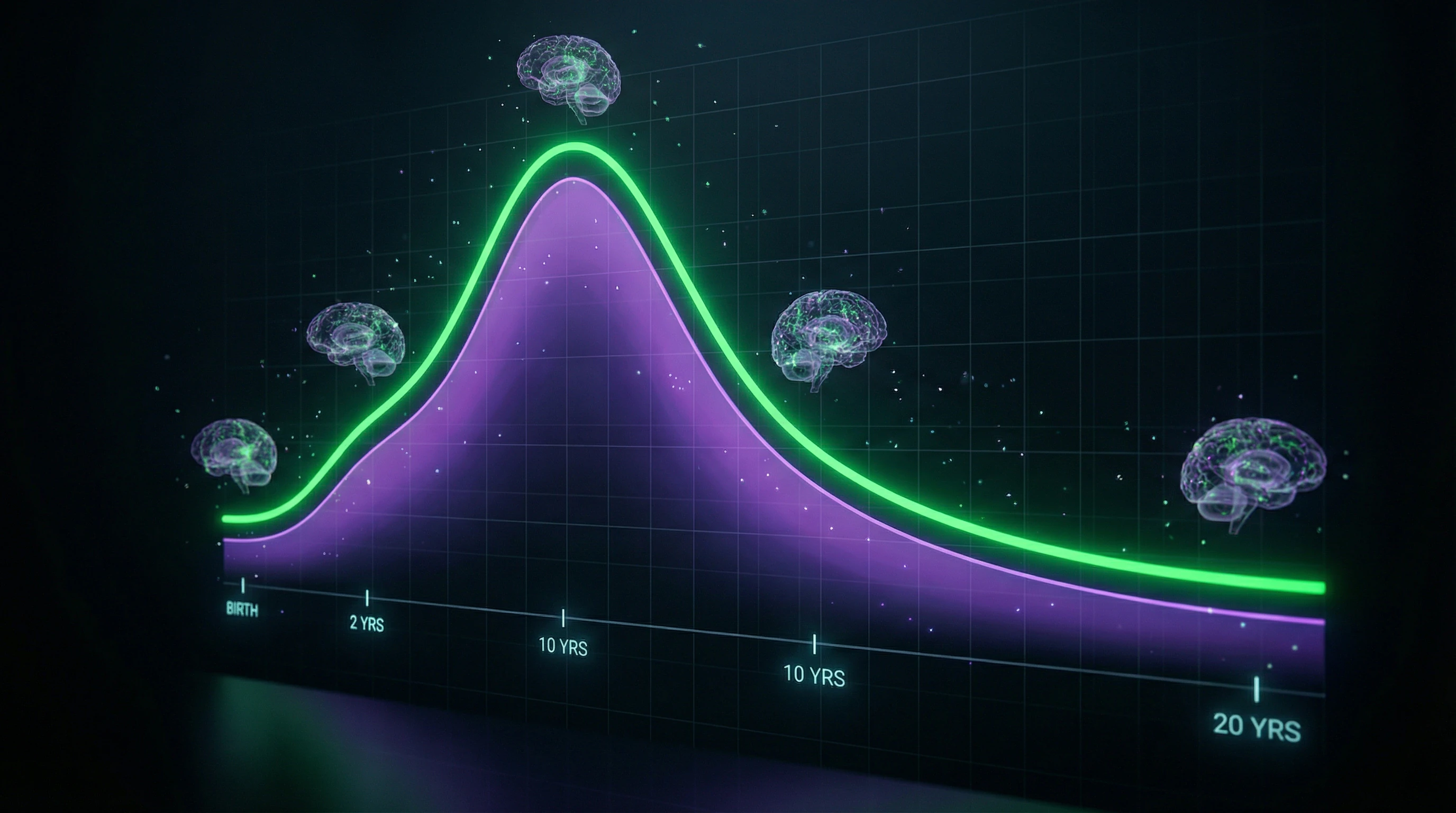
Синаптогенез достигает пика в разные периоды для различных областей: зрительная кора — 3–4 месяца (плотность синапсов до 150% взрослого уровня), префронтальная кора — 1–2 года, с последующим прунингом, удаляющим до 40% синапсов к подростковому возрасту.
Механизм зависит от активности: часто используемые синапсы стабилизируются через экспрессию BDNF и TrkB-рецепторов, неактивные помечаются комплементом C1q и элиминируются микроглией.
- Долговременная потенциация (LTP)
- Требует активации NMDA-рецепторов, входа Ca²⁺ и фосфорилирования AMPA-рецепторов, увеличивая синаптическую силу на 200–400% в течение минут с консолидацией через синтез белка в течение 1–3 часов.
- Обогащённая среда
- У грызунов увеличивает плотность дендритных шипиков на 25%, объём гиппокампа на 15% и нейрогенез в зубчатой извилине на 50% по сравнению со стандартными условиями.
Критические периоды развития мозга и их молекулярные механизмы
Критический период для бинокулярного зрения у человека — 3–8 лет, когда монокулярная депривация (косоглазие, катаракта) вызывает необратимую амблиопию из-за доминирования открытого глаза в зрительной коре.
Открытие и закрытие критических периодов регулируется балансом возбуждения/торможения: созревание парвальбумин-позитивных интернейронов и перинейрональных сетей завершает пластичность, а их деградация хондроитиназой ABC у взрослых крыс восстанавливает юношескую пластичность.
Языковое развитие показывает критический период до 7 лет для фонологии (различение звуков родного языка) и до 15 лет для синтаксиса, с прогрессивным снижением способности к акцентно-свободному усвоению второго языка на 0,7 балла по шкале владения за каждый год задержки после 7 лет.
Взрослый нейрогенез сохраняется в субгранулярной зоне гиппокампа (700 новых нейронов/день у молодых людей, снижаясь до 200/день к 70 годам) и субвентрикулярной зоне, с интеграцией новых нейронов в существующие сети за 4–6 недель.
Клиническая Нейронаука — Патологии Мозга и Их Нейробиологические Основы
Нейродегенеративные заболевания и механизмы белковой агрегации
Болезнь Альцгеймера строится на двух патологических столпах: внеклеточные бляшки β-амилоида (Aβ42, олигомеризуются при концентрации >100 нМ) и внутриклеточные нейрофибриллярные клубки гиперфосфорилированного тау-белка (фосфорилирование по 40+ сайтам вместо 2-3 в норме). На стадии деменции теряется 30-40% нейронов гиппокампа и энторинальной коры.
Патология распространяется по схеме Braak: стадии I-II (энторинальная кора, без симптомов) → III-IV (гиппокамп, лёгкие когнитивные нарушения) → V-VI (неокортекс, тяжёлая деменция). Корреляция тау-патологии с когнитивным снижением (r=0,7-0,8) значительно сильнее, чем для амилоида (r=0,3-0,4).
| Заболевание | Первичный механизм | Ключевой белок | Потеря нейронов |
|---|---|---|---|
| Болезнь Паркинсона | Гибель дофаминергических нейронов чёрной субстанции | α-синуклеин (тельца Леви) | 60-80% к появлению моторных симптомов |
| БАС | Селективная дегенерация моторных нейронов | TDP-43 (97%) или SOD1 (20% семейных) | 2-3% моторных единиц в месяц; выживаемость 3-5 лет |
Болезнь Паркинсона распространяется по гипотезе Braak: от обонятельной луковицы и дорсального ядра блуждающего нерва к среднему мозгу и коре. Боковой амиотрофический склероз (БАС) прогрессирует со скоростью потери 2-3% моторных единиц в месяц, медианная выживаемость 3-5 лет от начала симптомов.
Психические расстройства и их нейробиология на уровне цепей
Большое депрессивное расстройство — это дисбаланс активности в префронтально-лимбической сети. Дорсолатеральная префронтальная кора гипоактивна (снижение метаболизма на 15-25% по ПЭТ), субгенуальная передняя поясная кора гиперактивна (область 25 Бродмана, +30-40%), гиппокамп уменьшается на 8-10% при хронической депрессии из-за глюкокортикоид-индуцированной атрофии.
Моноаминовая гипотеза объясняет эффект СИОЗС: они повышают синаптический серотонин в 3-5 раз, но терапевтический эффект проявляется через 2-4 недели, так как требуются нейропластические изменения (увеличение BDNF, нейрогенез).
Шизофрения демонстрирует дофаминовый дисбаланс: мезолимбический путь гиперактивен (D2-рецепторы, +40-60% высвобождения дофамина → позитивные симптомы), мезокортикальный путь гипоактивен (префронтальная кора → негативные симптомы и когнитивный дефицит). Серое вещество уменьшается на 2-3%, желудочки расширяются на 20-30%.
Обсессивно-компульсивное расстройство (ОКР) характеризуется гиперактивностью орбитофронтально-стриато-таламо-кортикальной петли: метаболизм в орбитофронтальной коре +25-35%, в хвостатом ядре +15-20%. После успешной терапии (СИОЗС или когнитивно-поведенческая терапия) активность нормализуется.
Нейротехнологии и Будущее — Интерфейсы и Модуляция Мозговой Активности
Интерфейсы мозг-компьютер и декодирование нейронной активности
Инвазивные BCI с микроэлектродными матрицами (Utah array, 96–128 электродов) регистрируют потенциалы действия отдельных нейронов моторной коры с разрешением 30 кГц. Это позволяет декодировать намерение движения с точностью 90–95% и управлять роботизированными конечностями с 7–10 степенями свободы в реальном времени (задержка <100 мс).
Алгоритмы машинного обучения (рекуррентные нейросети, фильтры Калмана) преобразуют паттерны активности 50–200 нейронов в траектории движения. Ко-адаптивные декодеры обучаются через подкрепление, подстраиваясь к изменениям сигнала.
- Неинвазивные BCI на основе ЭЭГ используют P300 (потенциал через 300 мс после целевого стимула, амплитуда 5–10 мкВ) или моторные образы (десинхронизация μ-ритма 8–12 Гц в контралатеральной моторной коре).
- Управление курсором или спеллером достигает скорости 5–25 символов/минуту с точностью 70–90%.
- Электрокортикография (ECoG) с субдуральными электродами обеспечивает промежуточное разрешение (1–2 см, 1 кГц), декодируя речь с точностью 75–90% для ограниченного словаря и 40–60% для свободной речи.
Нейромодуляция и терапевтические применения стимуляции мозга
Глубокая стимуляция мозга (DBS) субталамического ядра при болезни Паркинсона (130–185 Гц, 2–4 В, 60–90 мкс) улучшает моторные симптомы на 40–70% по шкале UPDRS и снижает потребность в леводопе на 50–60%. Эффективность сохраняется >10 лет у 70% пациентов.
Механизм: подавление патологической β-осцилляции (13–30 Гц) в базальных ганглиях и нормализация таламо-кортикальной активности. Адаптивная DBS, регулирующая стимуляцию по локальным потенциалам поля (LFP), повышает эффективность на 20–30%.
Транскраниальная магнитная стимуляция (TMS) дорсолатеральной префронтальной коры (10 Гц, 3000 импульсов/сессию, 20–30 сессий) показывает ремиссию депрессии у 30–40% пациентов, резистентных к антидепрессантам. Механизм включает LTP-подобную пластичность и увеличение BDNF на 20–35%.
| Метод | Параметры | Эффект |
|---|---|---|
| tDCS (анодная) | 1–2 мА, 20–30 мин | Увеличивает возбудимость коры на 30–40% |
| tDCS (катодная) | 1–2 мА, 20–30 мин | Снижает возбудимость на 20–30% |
| tDCS + рабочая память | Стимуляция соответствующих областей | Улучшение на 10–20% |
| tDCS + моторное обучение | Стимуляция соответствующих областей | Ускорение на 15–25% |

Knowledge Access Protocol
FAQ
Часто задаваемые вопросы
Нейронаука — междисциплинарная область, изучающая структуру, функции и развитие нервной системы. Она объединяет биологию, психологию, химию и физику для понимания работы мозга, механизмов поведения и когнитивных процессов. Исследования охватывают уровни от молекул до целых нейронных сетей.
Нейроны передают информацию через электрические импульсы и химические сигналы в синапсах. Когда импульс достигает окончания нейрона, выделяются нейромедиаторы, которые связываются с рецепторами следующей клетки. Этот процесс занимает миллисекунды и лежит в основе всех функций мозга.
Нейропластичность — способность мозга изменять свою структуру и функции в ответ на опыт и обучение. Нейронные связи могут усиливаться, ослабевать или формироваться заново на протяжении всей жизни. Это свойство позволяет мозгу восстанавливаться после повреждений и адаптироваться к новым условиям.
Нет, это распространённый миф, опровергнутый нейровизуализацией. Исследования показывают, что все области мозга активны и выполняют определённые функции, даже в состоянии покоя. Различные задачи активируют разные зоны, но в течение дня задействуется весь мозг.
МРТ показывает активность областей мозга, но не «читает» конкретные мысли. Функциональная МРТ регистрирует изменения кровотока, связанные с нейронной активностью, позволяя определить, какие зоны работают при выполнении задач. Расшифровка сложных мыслей остаётся за пределами современных технологий.
Хроническое злоупотребление алкоголем может вызвать необратимые повреждения нейронов, особенно в гиппокампе и префронтальной коре. Однако при умеренном употреблении и прекращении приёма мозг способен частично восстановиться благодаря нейропластичности. Степень восстановления зависит от длительности и тяжести употребления.
Эффективны регулярные физические упражнения, качественный сон и интервальное повторение информации. Аэробные нагрузки стимулируют нейрогенез в гиппокампе, а сон консолидирует воспоминания. Также помогают мнемотехники, социальная активность и обучение новым навыкам, укрепляющие нейронные связи.
Нейромедиаторы — химические вещества, передающие сигналы между нейронами через синапсы. Дофамин регулирует мотивацию и удовольствие, серотонин — настроение, ГАМК — торможение нервной активности. Дисбаланс нейромедиаторов связан с депрессией, тревожностью и другими расстройствами.
Интерфейсы регистрируют электрическую активность мозга через электроды и преобразуют её в команды для устройств. Технология использует ЭЭГ или имплантированные сенсоры для декодирования намерений пользователя. Применяется для управления протезами, коммуникации парализованных пациентов и реабилитации после инсульта.
Да, критические периоды — это временные окна максимальной чувствительности мозга к определённым стимулам. Например, развитие зрения наиболее активно в первые годы жизни, а языковые навыки лучше усваиваются до подросткового возраста. После закрытия этих окон обучение возможно, но менее эффективно.
Это упрощение, не отражающее реальность. Оба полушария участвуют в большинстве когнитивных процессов, хотя имеют некоторую специализацию. Например, левое чаще связано с речью, но творчество требует взаимодействия обоих полушарий. Нейровизуализация показывает комплексную активность при любых задачах.
Болезнь Альцгеймера характеризуется накоплением бета-амилоидных бляшек и тау-белка в мозге, что приводит к гибели нейронов. Поражаются области, отвечающие за память и мышление, особенно гиппокамп и кора. Процесс начинается за десятилетия до появления симптомов и пока необратим.
Эффективность большинства «тренажёров мозга» ограничена и не переносится на повседневные задачи. Исследования показывают, что улучшения специфичны для тренируемых заданий. Более полезны разнообразная интеллектуальная деятельность, изучение языков, музыкальные инструменты и физическая активность.
Хронический стресс вызывает атрофию гиппокампа, ухудшая память, и увеличивает миндалевидное тело, усиливая тревожность. Повышенный кортизол повреждает нейроны и подавляет нейрогенез. Однако эти изменения частично обратимы при снижении стресса, медитации и терапии.
Сознание — интегрированная обработка информации распределёнными нейронными сетями, особенно в коре и таламусе. Теории включают глобальное рабочее пространство и интегрированную информацию, но полного понимания нет. Исследования изучают нейронные корреляты сознания при восприятии, внимании и самосознании.
Это теоретическая концепция, далёкая от реализации из-за сложности мозга и непонимания природы сознания. Требуется полное картирование 86 миллиардов нейронов и триллионов синапсов, а также воспроизведение их динамики. Философские вопросы о тождестве личности и субъективном опыте остаются нерешёнными.
