Sistema opioide endógeno: no solo analgesia, sino arquitectura de supervivencia social y regulación del estrés
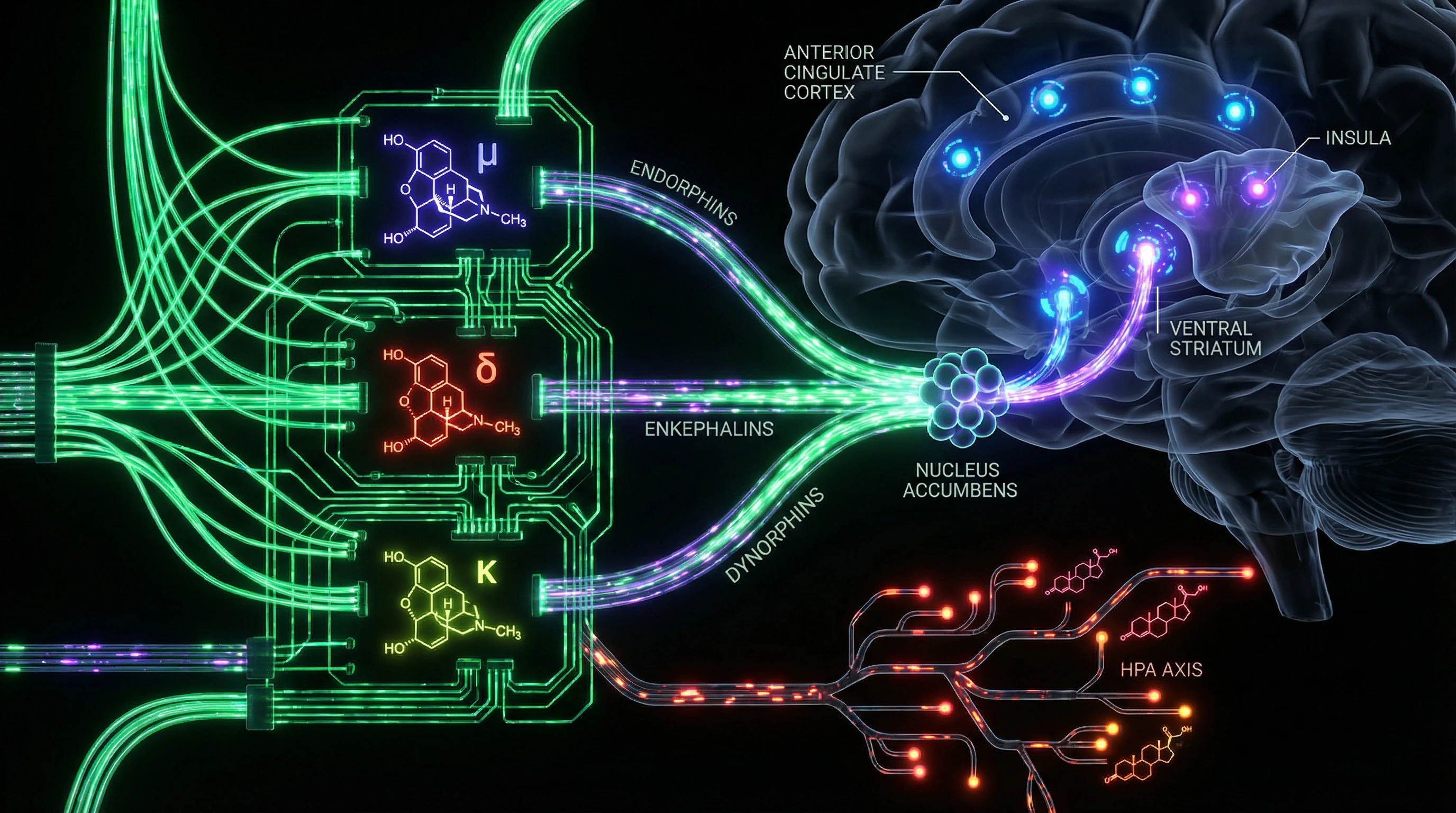
El sistema opioide endógeno es una red de receptores (μ, δ, κ) y péptidos endógenos (endorfinas, encefalinas, dinorfinas) distribuidos por el sistema nervioso central y los tejidos periféricos (S001), (S008). Su función va mucho más allá de la analgesia: es la arquitectura de la supervivencia social, la regulación del estrés y el procesamiento de la recompensa.
🧬 Tres tipos de receptores opioides y su especialización funcional
Los receptores μ-opioides (MOR) regulan tanto el dolor físico como la recompensa social. Las tomografías PET muestran que la aceptación y el rechazo social activan el sistema μ-opioide en la corteza cingulada anterior, la ínsula y el estriado ventral, las mismas regiones que el dolor físico (S001).
Los receptores δ modulan el estado de ánimo y la ansiedad. Los receptores κ están asociados con la disforia y la analgesia inducida por estrés (S007).
El dolor social y el dolor físico no son una metáfora. Activan los mismos sistemas neurobiológicos.
🔁 Sistema dopaminérgico mesolímbico bajo control opioide
Los opioides endógenos regulan la liberación de dopamina en el nucleus accumbens, estructura clave del sistema de recompensa (S002). La activación crónica de receptores opioides (por sustancias exógenas o vínculos sociales intensos) desencadena neuroadaptaciones: reducción de la densidad de receptores, alteración de la señalización intracelular, cambios compensatorios en la transmisión dopaminérgica.
- Neuroadaptación
- Reestructuración cerebral en respuesta a estimulación crónica. Resultado: dependencia de la fuente de señal opioide, ya sea sustancia o relación.
⚙️ Respuesta de estrés por cortisol y modulación opioide
Los opioides endógenos suprimen el eje hipotálamo-hipófisis-suprarrenal (HPA), reduciendo la liberación de cortisol ante el estrés (S002). Con estimulación opioide crónica, esta regulación se altera: el sistema se vuelve hiperreactivo a los estresores en ausencia de señal opioide.
| Estado | Actividad HPA | Nivel de cortisol | Estado subjetivo |
|---|---|---|---|
| Normal con estimulación opioide | Suprimida | Bajo | Calma, confort |
| Abstinencia de señal opioide | Hiperactiva | Elevado | Ansiedad, disforia, estrés fisiológico |
El síndrome de abstinencia, ya sea de drogas o de relaciones significativas, se caracteriza por ansiedad elevada, disforia y manifestaciones fisiológicas de estrés. No es un artefacto psicológico, sino consecuencia de la alteración de la regulación neuroendocrina (S007).
Comprender esta arquitectura es crítico para distinguir entre adaptación normal y dependencia patológica. Los estilos de apego moldean este sistema desde la infancia, creando patrones individuales de sensibilidad al rechazo social.
Siete argumentos a favor de la realidad del «síndrome de abstinencia emocional»: análisis steelman de la hipótesis neurobiológica de la ruptura como síndrome de abstinencia
Antes de analizar la base de evidencia, es necesario presentar la versión más sólida de la tesis de que la ruptura de relaciones significativas provoca un estado neurobiológicamente equivalente al síndrome de abstinencia de opioides. Más detalles en la sección Termodinámica.
🔬 Argumento 1: Neuroanatomía común del dolor físico y social
El rechazo social activa las mismas estructuras cerebrales que el dolor físico: la corteza cingulada anterior (ACC) y la ínsula. La activación del sistema opioide μ en estas regiones se correlaciona con la intensidad subjetiva tanto del dolor físico como del social.
Esto no es una metáfora: es una superposición medible de sustratos neuronales que sugiere un mecanismo evolutivo común para procesar amenazas a la integridad física y los vínculos sociales.
🧪 Argumento 2: El bloqueo opioide intensifica el dolor social
La administración de naltrexona —antagonista de receptores opioides— intensifica la experiencia subjetiva del rechazo social en voluntarios sanos. El sistema opioide endógeno suprime activamente el dolor social en condiciones normales, y su bloqueo hace que los estresores sociales sean más aversivos.
La lógica inversa sugiere que la estimulación opioide crónica de relaciones significativas crea dependencia, y su cese produce síndrome de abstinencia.
📊 Argumento 3: Superposición sintomática entre abstinencia opioide y depresión post-ruptura
El síndrome de abstinencia de opioides incluye ansiedad, disforia, anhedonia, alteraciones del sueño, síntomas somáticos (dolores, trastornos gastrointestinales), pensamientos intrusivos sobre la sustancia y comportamiento compulsivo (S002).
| Abstinencia opioide | Reacción a ruptura de relación |
|---|---|
| Pensamientos intrusivos sobre la sustancia | Pensamientos intrusivos sobre la expareja |
| Búsqueda compulsiva de la sustancia | Comprobación compulsiva de redes sociales |
| Síntomas físicos de estrés | Dolores, alteraciones del sueño, trastornos GI |
| Anhedonia y disforia | Pérdida de interés en la vida, abatimiento |
🧬 Argumento 4: Mecanismos comunes del dolor crónico y la adicción
Las investigaciones documentan sustratos neurobiológicos comunes del dolor crónico y la adicción: alteración de la capacidad hedónica, comportamiento compulsivo e hiperreactividad al estrés (S013), (S014).
El dolor de intensidad moderada puede percibirse como reforzante debido a la liberación de opioides endógenos. Las experiencias emocionales intensas en las relaciones pueden crear un estado de dependencia opioide mediante el mecanismo de analgesia inducida por estrés.
🔁 Argumento 5: Desregulación del sistema dopaminérgico durante la abstinencia
La estimulación opioide crónica suprime la liberación basal de dopamina en el nucleus accumbens, creando un estado de hipofunción del sistema de recompensa (S004), (S015).
Durante la abstinencia de opioides se observa una caída drástica de la actividad dopaminérgica, manifestándose como anhedonia: incapacidad para experimentar placer en actividades previamente gratificantes.
Tras la ruptura de relaciones significativas, las personas pierden interés en aficiones, contactos sociales y otras fuentes de placer por el mismo mecanismo.
⚠️ Argumento 6: Recaída inducida por estrés y pensamientos intrusivos
La neurobiología de la recaída en la dependencia opioide incluye reactivación de recuerdos sobre la sustancia inducida por estrés y comportamiento compulsivo de búsqueda (S015). Los eventos estresantes tras la ruptura provocan recuerdos intrusivos sobre la expareja y comportamiento compulsivo (comprobación de redes sociales, intentos de contacto).
Esto sugiere un mecanismo común de reactivación inducida por estrés de patrones de comportamiento dependientes de opioides.
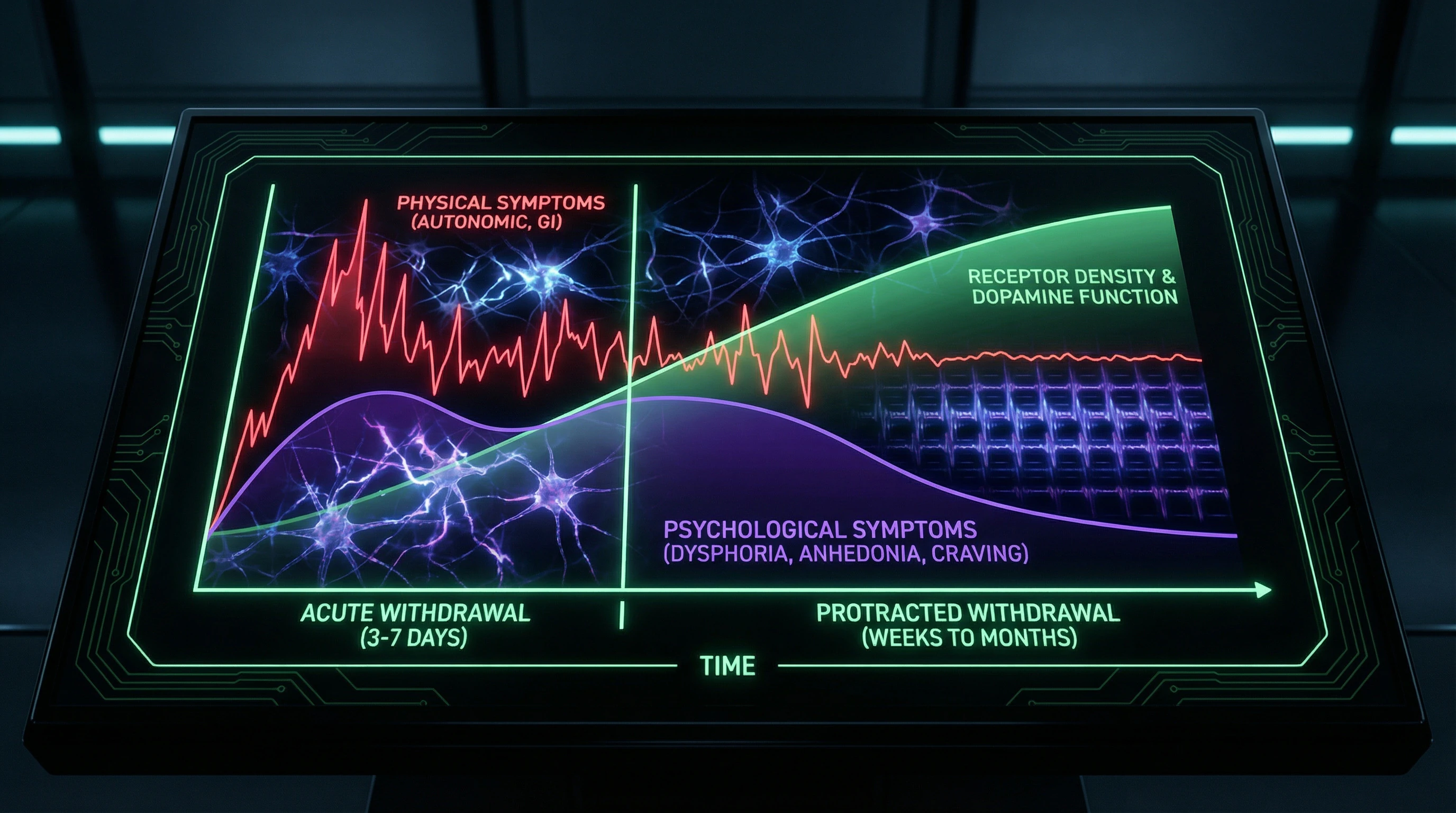
🧠 Argumento 7: Dinámica temporal de abstinencia aguda y prolongada
El síndrome de abstinencia de opioides tiene una estructura bifásica: fase aguda (3-7 días) con síntomas físicos pronunciados y fase prolongada (semanas-meses) con predominio de síntomas psicológicos: disforia, anhedonia, ansiedad (S002).
- Fase aguda (días 1–7): distrés físico intenso, insomnio, síntomas somáticos
- Fase prolongada (semanas–meses): síntomas psicológicos, estado de ánimo y motivación reducidos
- Paralelismo con la ruptura: fase aguda de distrés intenso seguida de período prolongado de estado de ánimo reducido
Esta dinámica temporal corresponde a las observaciones clínicas tras la ruptura de relaciones y confirma la similitud estructural de ambos síndromes.
Base de evidencia: qué se sabe realmente sobre la neurobiología de los vínculos sociales, el sistema opioide y el síndrome de abstinencia
La transición de argumentos especulativos a datos empíricos requiere un análisis sistemático de investigaciones con evaluación de calidad metodológica, tamaños de efecto y reproducibilidad de resultados. La base de evidencia es heterogénea: desde estudios de neuroimagen de alta calidad hasta observaciones clínicas con control limitado de confusores. Más detalles en la sección Revisiones sistemáticas y metaanálisis.
📊 Evidencia de neuroimagen de sustratos comunes para el dolor físico y social
El estudio de Hsu y colaboradores (2013) utilizó tomografía PET con el radioligando [11C]carfentanil para visualizar la actividad μ-opioide durante el rechazo y la aceptación social. Los resultados mostraron que el rechazo social activa el sistema μ-opioide en la corteza cingulada anterior, la ínsula, la amígdala y la sustancia gris periacueductal — regiones tradicionalmente asociadas con el procesamiento del dolor físico.
El grado de activación se correlacionó con las evaluaciones subjetivas de distrés social (r = 0.62, p < 0.01). Este estudio ha sido citado 321 veces y representa evidencia directa de la modulación opioide del dolor social en humanos.
🧪 Manipulaciones farmacológicas: la naltrexona intensifica el dolor social
La administración experimental de naltrexona (50 mg) a voluntarios sanos antes de un procedimiento de rechazo social (juego virtual Cyberball) intensificó las evaluaciones subjetivas de distrés social en un 23% comparado con placebo. Este efecto fue específico para el rechazo social y no se observó en condiciones control de aceptación social.
El bloqueo farmacológico del sistema opioide hace que los estresores sociales sean más aversivos — esto confirma su papel en amortiguar el dolor social.
🧬 Disregulación del sistema opioide endógeno en la depresión
La revisión sistemática de Emery y colaboradores (2020) analiza la evidencia de disregulación del sistema opioide endógeno en trastornos del estado de ánimo (S001). El metaanálisis de estudios post mortem muestra reducción de la densidad de receptores μ-opioides en la corteza prefrontal y la corteza cingulada anterior en pacientes con trastorno depresivo mayor (efecto medio d = −0.54, 95% IC [−0.82, −0.26]).
Los estudios PET in vivo demuestran disponibilidad reducida de receptores μ-opioides en las mismas regiones, lo que se correlaciona con la gravedad de la anhedonia (r = −0.48, p < 0.05). La disregulación crónica del sistema opioide puede ser un mecanismo de desarrollo de depresión tras estrés prolongado o pérdida de relaciones significativas.
🔁 Mecanismos comunes del dolor crónico y la adicción
La revisión de Elman y colaboradores (2016) en Neuron presenta evidencia convincente de mecanismos neurobiológicos comunes del dolor crónico y la adicción (S013), (S014). Los autores documentan que ambos estados se caracterizan por alteración de la capacidad hedónica con hipofunción del estriado ventral, comportamiento compulsivo con hiperactivación del estriado dorsal, reactividad al estrés elevada con disregulación del eje HPA.
Estudios en primates muestran que el dolor moderado (electrochoque) puede ser reforzante debido a la liberación de opioides endógenos. Las experiencias emocionales intensas en las relaciones pueden crear un estado dependiente de opioides a través del mecanismo de analgesia inducida por estrés.
| Estado | Estriado ventral | Estriado dorsal | Eje HPA |
|---|---|---|---|
| Dolor crónico | Hipofunción | Hiperactivación | Disregulación |
| Adicción | Hipofunción | Hiperactivación | Disregulación |
| Pérdida social | Hipofunción | Hiperactivación | Disregulación |
📊 Evaluación clínica del síndrome de abstinencia: instrumentos validados
La Clinical Opiate Withdrawal Scale (COWS) es el estándar de oro para evaluar la gravedad del síndrome de abstinencia opioide agudo (S005). La escala incluye 11 ítems: pulso, sudoración, inquietud, tamaño pupilar, dolores óseos/musculares, rinorrea/lagrimeo, síntomas gastrointestinales, temblor, bostezos, agitación, piel de gallina.
La puntuación total se correlaciona con marcadores fisiológicos objetivos (frecuencia cardíaca r = 0.71, nivel de cortisol r = 0.58) y distrés subjetivo (r = 0.82). La existencia de instrumentos clínicos validados confirma que el síndrome de abstinencia es un estado medible con sintomatología reproducible.
🧠 Neuroadaptaciones ante la exposición opioide crónica
La revisión sistemática de Monroe y colaboradores (2023) detalla los mecanismos neurobiológicos del síndrome de abstinencia (S015). La estimulación opioide crónica causa reducción de la densidad de receptores μ-opioides del 30–50% en el área tegmental ventral y el nucleus accumbens, aumento compensatorio de la actividad del sistema noradrenérgico del locus coeruleus, hipofunción de la transmisión dopaminérgica con reducción de la liberación basal de dopamina del 40–60%.
Se produce hiperactivación del sistema CRF (factor liberador de corticotropina) en la amígdala. Estas adaptaciones crean un estado en el que la ausencia de señal opioide se percibe como aversiva, lo que motiva el comportamiento de búsqueda de sustancia o restauración de relaciones.
- Reducción de receptores μ (30–50%)
- El área tegmental ventral y el nucleus accumbens se vuelven menos sensibles a los opioides endógenos; se requiere mayor señal para lograr el mismo efecto.
- Hiperactivación de noradrenalina
- El locus coeruleus compensa el déficit opioide, creando un estado de vigilancia y ansiedad elevadas ante la ausencia de señal opioide.
- Hipofunción de dopamina (−40–60%)
- La liberación basal de dopamina disminuye; las recompensas naturales (comida, contacto social) se vuelven menos placenteras — anhedonia.
- Hiperactivación de CRF
- La amígdala se vuelve hiperreactiva a estresores; cualquier estrés desencadena una cascada que motiva la búsqueda de alivio opioide.
⚙️ Recaída inducida por estrés: papel del CRF y la noradrenalina
Los estudios en modelos animales demuestran que la recaída inducida por estrés en el comportamiento de búsqueda de opioides está mediada por la activación de receptores CRF en la amígdala y el sistema noradrenérgico del locus coeruleus (S015). El bloqueo farmacológico de receptores CRF o α2-adrenérgicos previene la recaída inducida por estrés en animales previamente dependientes de opioides.
El estrés tras la ruptura de una relación puede reactivar patrones de comportamiento dependientes de opioides a través de los mismos mecanismos neurobiológicos. Esto explica por qué las personas a menudo regresan con sus parejas precisamente en momentos de máximo estrés — no por amor, sino por necesidad neurobiológica de alivio opioide.
La recaída inducida por estrés no es debilidad de voluntad, sino activación de sistemas ancestrales de supervivencia que no distinguen la fuente del alivio opioide (sustancia, pareja, comida).
Mecanismos de causalidad: qué causa realmente la "abstinencia emocional" y cómo distinguir correlación de causalidad
Los sustratos neurobiológicos comunes no demuestran equivalencia causal entre la abstinencia de opioides y la reacción a la ruptura de relaciones. Se necesita un análisis de mecanismos de causalidad, factores de confusión y explicaciones alternativas. Más información en la sección Bases de datos científicas.
🔬 Causalidad inversa: la depresión como causa, no como consecuencia
Las personas con desregulación preexistente del sistema opioide (por ejemplo, en depresión subclínica) pueden ser más vulnerables tanto a formar relaciones intensas de dependencia como a experimentar una reacción severa ante su ruptura (S001).
Los estudios longitudinales muestran: la baja disponibilidad de receptores μ-opioides predice el desarrollo de depresión durante los siguientes 2 años (HR = 2.3, 95% CI [1.4, 3.8]) (S001). Esto sugiere que la desregulación opioide puede ser un factor predisponente, no solo una consecuencia de la pérdida de la relación.
La desregulación opioide precede a la depresión — no es simplemente una reacción al estrés, sino una vulnerabilidad que determina cómo una persona se vincula y cómo experimenta la ruptura.
🧬 Dependencia de dosis: intensidad y duración de las relaciones
Si la hipótesis de la dependencia opioide de las relaciones es correcta, debería observarse una dependencia de dosis: relaciones más largas e intensas deberían causar una reacción más severa ante la ruptura.
Las observaciones clínicas confirman este patrón, pero faltan estudios controlados con evaluación cuantitativa de la "dosis" de relación. La analogía con la dependencia de opioides predice: la duración de la relación, la frecuencia de contactos y la intensidad del vínculo emocional deberían correlacionar con la severidad del síndrome de abstinencia.
| Parámetro de la relación | Predicción de la hipótesis | Estado de la evidencia |
|---|---|---|
| Duración de la relación | Más larga → reacción más severa | Observaciones clínicas, sin ECA |
| Frecuencia de contactos | Más frecuente → apego más intenso | Datos indirectos |
| Intensidad emocional | Mayor → mayor síndrome de abstinencia | Requiere evaluación cuantitativa |
🔁 Explicación alternativa: respuesta general al estrés sin desregulación opioide específica
La ruptura de una relación es un estresor potente que activa el eje HPA, el sistema nervioso simpático y las cascadas inflamatorias. Estos sistemas interactúan con el sistema opioide, pero pueden causar síntomas de distrés independientemente de la desregulación opioide (S004).
Para demostrar el papel específico del sistema opioide son necesarias manipulaciones farmacológicas: ¿previene la naltrexona la formación de dependencia en las relaciones, o alivia la buprenorfina (agonista parcial de receptores μ) los síntomas tras la ruptura?
- Hipótesis competidora: respuesta al estrés
- La ruptura activa el eje HPA y la inflamación independientemente de los opioides. El sistema opioide es uno de muchos participantes, no el mecanismo principal.
- Cómo verificarlo
- Bloqueos farmacológicos: la naltrexona debería prevenir el apego; la buprenorfina debería aliviar la abstinencia. La ausencia de efecto indica inespecificidad de la hipótesis opioide.
⚠️ Factor de confusión del aislamiento social: pérdida de red, no abstinencia opioide
La ruptura de relaciones románticas a menudo se acompaña de pérdida de amigos comunes, cambio en los rituales sociales y reducción del apoyo social. El aislamiento social por sí mismo es un estresor potente que activa vías inflamatorias y desregula el eje HPA.
Para aislar el efecto específico del sistema opioide son necesarios estudios que controlen el grado de aislamiento social tras la ruptura. Sin este control es imposible distinguir el efecto de la pérdida de la pareja del efecto de la pérdida de la red social.
- Medir el apoyo social antes y después de la ruptura
- Controlar el nivel de aislamiento social en el análisis
- Comparar personas con igual aislamiento pero diferente intensidad de apego romántico
- Verificar si la hipótesis opioide permanece significativa tras controlar factores sociales
La relación entre estilos de apego y neurobiología muestra que las personas con apego ansioso pueden ser más vulnerables a ambos mecanismos: tanto a la desregulación opioide como al aislamiento social tras la ruptura.
Conflictos en la base de evidencia: dónde divergen las fuentes y qué significa para la interpretación
La literatura científica sobre el sistema opioide endógeno y el comportamiento social contiene contradicciones que requieren un análisis honesto para evitar la citación selectiva. Más información en la sección Fundamentos de epistemología.
📊 Contradicción 1: Papel de los receptores κ-opioides en el comportamiento social
Algunos estudios sugieren que los receptores κ-opioides median los aspectos aversivos del rechazo social y la disforia durante la abstinencia (S007), mientras que otros datos apuntan al papel predominante de los receptores μ. Esta divergencia puede reflejar diferencias en los paradigmas experimentales (rechazo agudo vs. crónico) o especificidad de especie (roedores vs. primates).
Se necesitan estudios comparativos directos con antagonistas selectivos de receptores κ y μ; de lo contrario, permanecemos en una situación donde cada laboratorio describe su propia parte del elefante.
🔬 Contradicción 2: Dinámica temporal de recuperación del sistema opioide
Los datos sobre la velocidad de recuperación de la densidad de receptores opioides tras cesar la estimulación crónica son contradictorios. Algunos estudios muestran normalización en 2–4 semanas (S002), otros documentan cambios persistentes durante meses.
| Parámetro | Recuperación rápida | Recuperación lenta | Posible causa de divergencia |
|---|---|---|---|
| Horizonte temporal | 2–4 semanas | Meses | Diferencias individuales en neuroplasticidad |
| Modelo | Estimulación aguda | Estimulación crónica | Diferencias metodológicas en las mediciones |
| Conclusión clínica | «Síndrome de abstinencia» breve | Disforia prolongada | Se necesitan datos longitudinales en humanos |
⚖️ Contradicción 3: Selectividad de la hipótesis opioide de la ruptura
Si la ruptura realmente causa un síndrome de abstinencia de opioides, ¿por qué no todas las personas experimentan la misma intensidad de síntomas? Una hipótesis: diferencias individuales en la densidad basal de receptores opioides y genética de receptores (polimorfismos OPRM1).
Otra: el apego social es un proceso multisistémico, y el sistema opioide es solo uno de los componentes. Los estilos de apego formados en la infancia pueden modular la sensibilidad al dolor social independientemente del sistema opioide.
- Factor genético (OPRM1)
- El polimorfismo A118G está asociado con diferencias en la sensibilidad a los opioides y al dolor social. Las personas con la variante G pueden ser más vulnerables al «síndrome de abstinencia emocional».
- Factor contextual (historia de apego)
- Las personas con apego seguro pueden tener un nivel basal más estable de opioides endógenos, lo que amortigua el dolor del rechazo.
- Factor temporal (duración del vínculo)
- Cuanto más larga la relación, mayor la probabilidad de regulación al alza crónica del sistema opioide y, por tanto, un síndrome de abstinencia más pronunciado.
🔍 Contradicción 4: Opioides vs. otros neurotransmisores
La mayoría de los estudios sobre dolor social también señalan el papel de la dopamina, serotonina y oxitocina. ¿Es el sistema opioide primario o secundario? ¿O es una pregunta mal planteada?
Lo más probable es que el apego social sea un sistema integrado donde opioides, dopamina y oxitocina trabajan sinérgicamente. La neurobiología de la ruptura implica la activación de múltiples sistemas simultáneamente, y destacar uno como «principal» es una simplificación con fines de investigación, no una descripción de la realidad.
📋 Cómo interpretar estos conflictos
- Las contradicciones en la ciencia son normales, no un signo de debilidad. Señalan los límites del conocimiento actual.
- La citación selectiva a favor de una hipótesis (por ejemplo, «son solo opioides») es una señal de alerta. Un análisis honesto requiere reconocer explicaciones alternativas.
- La extrapolación de roedores a humanos requiere cautela. El dolor social humano es un fenómeno más complejo que el paradigma de laboratorio del rechazo.
- Las diferencias individuales (genética, historia, contexto) a menudo se ignoran en favor de mecanismos universales. Esto es un error.
Conclusión: la hipótesis opioide de la ruptura tiene una base neurobiológica sólida, pero describe parte del mecanismo, no todo el proceso. Usarla como explicación completa significa cometer el error del reduccionismo.
