 🧠 Neurociencia
🧠 NeurocienciaNeurociencia: Investigación del Cerebro y el Sistema Nerviosoλ
Ciencia interdisciplinaria que estudia la estructura, funciones y desarrollo del sistema nervioso, desde los mecanismos moleculares hasta el comportamiento y la cognición humana.
Overview
La neurociencia integra biología, física, química e informática para descifrar 🧠 el funcionamiento del cerebro — desde mecanismos moleculares hasta la consciencia. Las tecnologías modernas (fMRI, escáneres PET) permiten observar la actividad de las redes neuronales en tiempo real y comprender cómo se forman la memoria, las emociones y las decisiones. Los resultados se aplican en medicina, educación, desarrollo de IA y terapia cognitiva.
🛡️
Protocolo Laplace: La neurociencia se fundamenta en métodos experimentales rigurosos y resultados reproducibles, separando el conocimiento científicamente validado sobre el cerebro de los mitos populares y afirmaciones pseudocientíficas sobre su funcionamiento.
Reference Protocol
Base Científica
Marco basado en evidencia para análisis crítico
Protocol: Evaluation
Ponte a Prueba
Cuestionarios sobre este tema próximamente
Sector L1
Artículos
Materiales de investigación, ensayos y profundizaciones en los mecanismos del pensamiento crítico.
 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia 🧠 Neurociencia
🧠 Neurociencia⚡
Más Información
Arquitectura del sistema nervioso: de las máquinas moleculares a las redes globales
El sistema nervioso es una estructura jerárquica donde miles de millones de células especializadas coordinan todos los procesos del organismo, desde reflejos automáticos hasta el pensamiento abstracto. Las neuronas transmiten información a distancias desde micrómetros hasta metros a velocidades de hasta 120 m/s gracias a su morfología única y propiedades electroquímicas.
El cerebro humano contiene aproximadamente 86 mil millones de neuronas, cada una forma en promedio 7000 contactos sinápticos. Esta red crea la base para todos los procesos cognitivos.
Neuronas y transmisión sináptica: lógica molecular de la comunicación
La neurona consta de soma (cuerpo celular), dendritas (recepción de señales) y axón (transmisión). La información se codifica mediante potenciales de acción: impulsos eléctricos estereotipados de amplitud aproximada de 100 mV y duración de 1–2 ms, que surgen cuando la despolarización de la membrana supera el umbral de −55 mV.
La generación del potencial de acción se asegura mediante la apertura en cascada de canales de sodio dependientes de voltaje, que permiten el paso de hasta 10⁷ iones Na⁺ por segundo a través de un solo canal. La vaina de mielina aumenta la velocidad de conducción entre 5 y 50 veces gracias al mecanismo saltatorio: propagación por saltos de la excitación entre los nódulos de Ranvier.
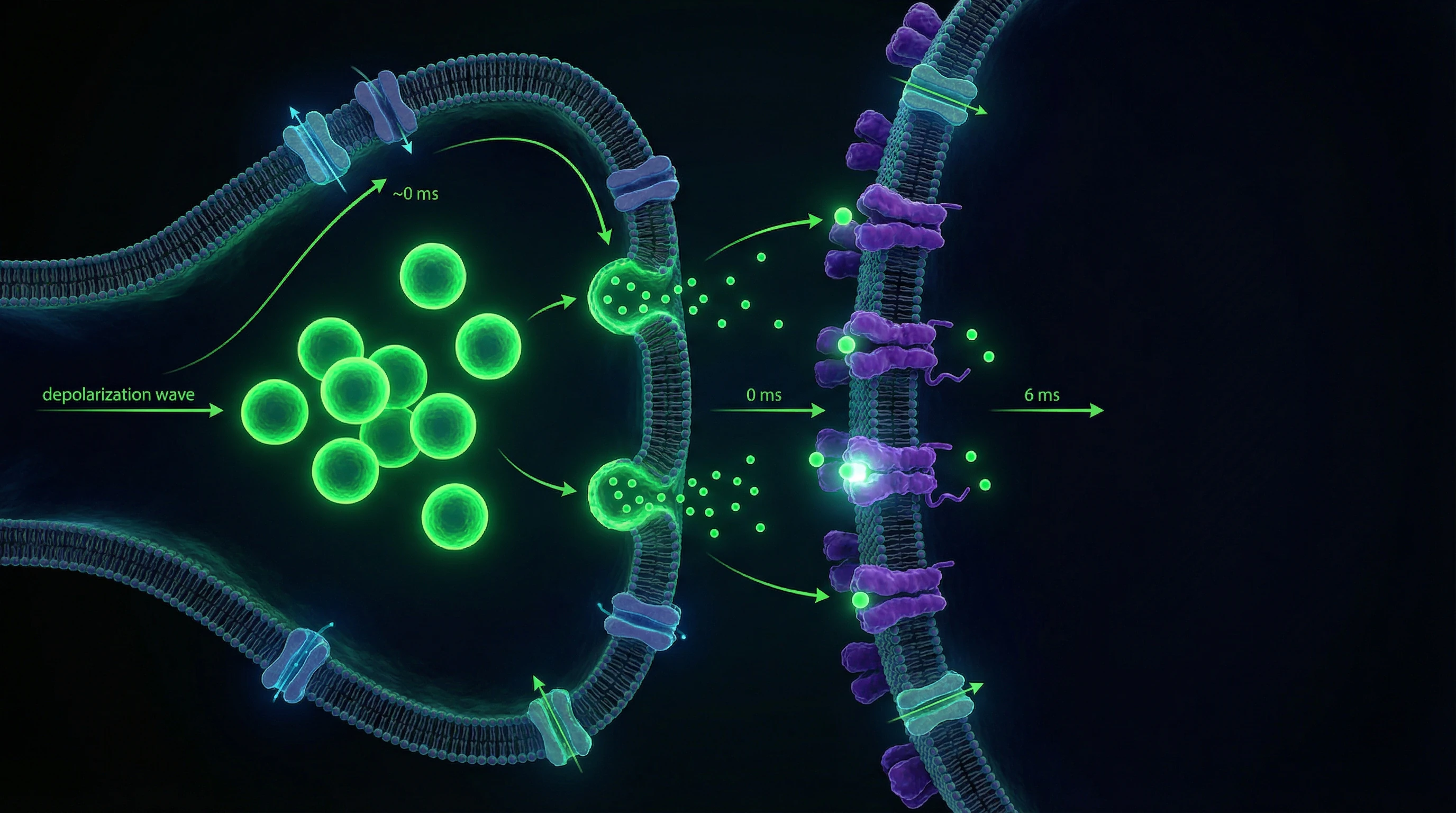
La transmisión sináptica se realiza predominantemente por vía química mediante la liberación de neurotransmisores en la hendidura sináptica de 20–40 nm de ancho. La llegada del potencial de acción al terminal presináptico abre canales de calcio dependientes de voltaje; la entrada de Ca²⁺ desencadena la exocitosis de vesículas sinápticas en 0,2–0,5 ms.
- Cuanto de mediador
- Contenido de una vesícula sináptica; una sinapsis típica libera 1–5 cuantos por impulso con probabilidad de 0,1–0,9.
- Glutamato
- Principal mediador excitatorio (80–90% de sinapsis del SNC); su equilibrio con GABA determina la excitabilidad de las redes neuronales.
- GABA
- Principal mediador inhibitorio (10–20% de sinapsis); crítico para prevenir la hiperexcitabilidad.
Sistema nervioso central y periférico: división funcional del trabajo
El SNC incluye el encéfalo (masa 1300–1400 g) y la médula espinal (longitud 40–45 cm, 31 segmentos), protegidos por estructuras óseas y tres meninges. La corteza cerebral contiene 16–20 mil millones de neuronas, organizadas en seis capas de 1,5–4,5 mm de grosor; el área total de la corteza al alisarse es de 1800–2300 cm².
| Estructura | Función | Mecanismo |
|---|---|---|
| Ganglios basales | Control de movimientos | Selección e iniciación de programas motores |
| Hipocampo | Consolidación de memoria | Codificación de eventos episódicos |
| Amígdala | Reacciones emocionales | Evaluación de amenaza y recompensa |
| Médula espinal | Reflejos y motricidad | Latencia 30–50 ms a través de 31 pares de nervios |
El SNP consta de 12 pares de nervios craneales y 31 pares de nervios espinales, dividiéndose en sistema somático (control voluntario de músculos esqueléticos) y sistema autónomo (regulación involuntaria de órganos internos).
- División simpática (noradrenalina): reacción de «lucha o huida»: aumenta la FC de 60–80 a 120–180 lpm, redistribuye el flujo sanguíneo hacia los músculos (hasta 80% del gasto cardíaco), moviliza reservas energéticas.
- División parasimpática (acetilcolina): modo «descanso y recuperación»: estimula la digestión, reduce la FC, activa procesos anabólicos.
- Sistema nervioso entérico: 200–600 millones de neuronas intestinales funcionan de forma autónoma e interactúan bidireccionalmente con el SNC a través del nervio vago.
Métodos de investigación cerebral: de electrodos a marcadores moleculares
La neurociencia moderna utiliza un enfoque multimodal, combinando métodos con diferentes resoluciones espaciales (desde nanómetros hasta centímetros) y temporales (desde microsegundos hasta años). Los avances de las últimas décadas —resonancia magnética funcional (años 90), optogenética (2005), microscopía de dos fotones in vivo (años 2000), conectómica (años 2010)— han permitido pasar de observaciones correlacionales al análisis causal de mecanismos neuronales.
La integración de datos de diferentes escalas mediante modelado computacional crea mapas multinivel del cerebro desde moléculas hasta comportamiento.
Neuroimagen y electrofisiología: observando el cerebro vivo
La resonancia magnética funcional (fMRI) detecta cambios en el flujo sanguíneo mediante señal BOLD (blood oxygen level dependent) con resolución espacial de 1–3 mm y temporal de 1–2 s, permitiendo mapear la actividad de todo el cerebro de forma no invasiva. La activación neuronal aumenta el flujo sanguíneo local en 20–40% con un retraso de 4–6 s, superando la demanda de oxígeno (acoplamiento neurovascular), lo que crea contraste entre zonas activas e inactivas.
La tomografía por emisión de positrones (PET) utiliza trazadores radiactivos para visualizar el metabolismo de glucosa (¹⁸F-FDG), sistemas de neurotransmisores (¹¹C-raclopride para dopamina), placas amiloides en enfermedad de Alzheimer con sensibilidad hasta concentraciones picomolares.
| Método | Resolución espacial | Resolución temporal | Ventaja |
|---|---|---|---|
| fMRI | 1–3 mm | 1–2 s | Cerebro completo, no invasivo |
| PET | 2–4 mm | Minutos | Marcadores moleculares (metabolismo, receptores) |
| MEG | 2–5 mm | 1 ms | Alta resolución temporal, no invasivo |
| EEG | 5–10 cm | 1 ms | Portabilidad, bajo coste |
La magnetoencefalografía (MEG) registra campos magnéticos de 10–100 femtoteslas, generados por actividad sincrónica de 10⁴–10⁵ neuronas, con resolución temporal de 1 ms y localización de fuentes con precisión de 2–5 mm.
La electroencefalografía (EEG) mide la actividad eléctrica sumada mediante 19–256 electrodos en el cuero cabelludo, revelando ritmos: delta (0,5–4 Hz, sueño profundo), theta (4–8 Hz, meditación), alfa (8–13 Hz, vigilia relajada), beta (13–30 Hz, pensamiento activo), gamma (30–100 Hz, integración cognitiva).
La técnica de patch-clamp alcanza resolución de canales iónicos individuales (conductancia 1–100 picosiemens), permitiendo analizar corrientes sinápticas de amplitud 5–50 pA con precisión de microsegundos — es el límite entre macroscopía y física molecular.
Las matrices de electrodos multicanal (hasta 1024 canales) registran actividad de cientos de neuronas simultáneamente in vivo, revelando patrones de codificación poblacional y ensambles neuronales que correlacionan con comportamiento.
Enfoques moleculares y genéticos: manipulación de circuitos neuronales
La optogenética utiliza proteínas fotosensibles (channelrhodopsin-2 se activa con luz azul 470 nm, halorhodopsin con amarilla 580 nm) para controlar la actividad de poblaciones neuronales genéticamente definidas con precisión de milisegundos. La expresión de opsinas bajo promotores de genes específicos (por ejemplo, CaMKIIα para neuronas excitadoras, GAD67 para inhibidoras) permite activar o inhibir selectivamente tipos celulares, demostrando su rol causal en el comportamiento.
La quimiogenética (DREADD — designer receptors exclusively activated by designer drugs) proporciona control farmacológico de la actividad neuronal: el ligando sintético clozapina-N-óxido (CNO, 1–10 mg/kg) activa receptores inertes, modulando la actividad de neuronas objetivo durante horas. Los vectores virales (AAV, lentivirus) entregan construcciones genéticas con eficiencia de transducción del 60–90% en el área objetivo de volumen 0,5–2 mm³.
- Optogenética: luz → opsina → canal iónico → neurona activa/inactiva (milisegundos)
- Quimiogenética: CNO → receptor sintético → modulación de actividad (horas)
- CRISPR/Cas9: edición genómica → knockout génico → modelado de enfermedad (permanente)
- Vectores virales: entrega de construcción en área objetivo (60–90% eficiencia)
La edición genómica CRISPR/Cas9 permite crear knockouts de genes específicos en neuronas con eficiencia del 40–80%, modelando variantes genéticas asociadas con enfermedades neurológicas.
La transcriptómica de células individuales (scRNA-seq) ha revelado más de 100 tipos neuronales molecularmente distintos en la corteza, cada uno con perfil único de expresión de 15000–20000 genes, redefiniendo la clasificación de células cerebrales.
La conectómica reconstruye mapas completos de conexiones sinápticas: el conectoma de C. elegans (302 neuronas, 7000 sinapsis) se completó en 1986, el cubo cortical murino de 1 mm³ (100000 neuronas, 10⁹ sinapsis) en 2021 utilizando microscopía electrónica seriada y aprendizaje automático. Es la transición de la descripción a la topografía completa.
La imagen de calcio con indicadores GCaMP6 (ΔF/F hasta 1000% durante actividad) permite registrar actividad de 1000–10000 neuronas simultáneamente in vivo mediante microscopios implantados (1–2 g) o microscopía de dos fotones a través de ventana craneal.
Neurociencia cognitiva: códigos neuronales de la mente
La neurociencia cognitiva estudia los mecanismos neuronales de las funciones psíquicas superiores: percepción, atención, memoria, lenguaje, toma de decisiones y consciencia. El concepto clave es la codificación neuronal: la información se representa mediante patrones de actividad de poblaciones neuronales, donde el significado no lo determinan células individuales, sino la actividad distribuida de conjuntos de 10²-10⁴ neuronas.
La dinámica temporal es tan importante como la frecuencia de disparo: la información se codifica en el timing preciso de los potenciales de acción respecto al ritmo theta (4-8 Hz) del hipocampo con una precisión de 10-20 ms.
Mecanismos de memoria y aprendizaje: de las sinapsis a los sistemas
La potenciación a largo plazo (LTP) —fortalecimiento sostenido de la transmisión sináptica del 100-400% tras estimulación de alta frecuencia (100 Hz, 1 s)— se considera el mecanismo celular de la memoria. La LTP en el hipocampo requiere activación de receptores NMDA, que permiten el paso de Ca²⁺ solo con despolarización simultánea y unión de glutamato (detector de coincidencia hebbiano).
Cascada de activación: CaMKII → fosforilación de receptores AMPA → aumento de su número en la sinapsis (de 20 a 80 receptores en 15-30 min). La fase tardía de LTP (L-LTP, >3 h) requiere síntesis de proteínas de novo mediante activación de transcripción dependiente de CREB, aumentando el tamaño de las espinas dendríticas un 30-60% y estabilizando los cambios durante días-meses.
| Proceso | Estimulación | Efecto | Función |
|---|---|---|---|
| LTP | 100 Hz, 1 s | Fortalecimiento 100-400% | Aprendizaje, memorización |
| LTD | 1 Hz, 15 min | Debilitamiento 30-50% | Olvido, refinamiento |
La depresión a largo plazo (LTD) —proceso opuesto de debilitamiento sináptico con estimulación de baja frecuencia— proporciona el olvido y refinamiento de circuitos neuronales.
La consolidación de la memoria transfiere información del hipocampo al neocórtex durante semanas-meses mediante reactivación de patrones neuronales durante el sueño. Durante el sueño de ondas lentas, los «replays» hipocampales reproducen secuencias de actividad diurna en tiempo comprimido (compresión de 6-20 veces), sincronizándose con husos corticales (12-15 Hz, 0,5-2 s) para transferir información.
La interrupción del sueño en las primeras 6 h tras el aprendizaje reduce la consolidación un 30-50%, mientras que el refuerzo optogenético de la reactivación mejora la memoria un 20-40%.
La memoria de trabajo mantiene 4±1 elementos en la corteza prefrontal mediante actividad neuronal sostenida (10-30 Hz) durante segundos-minutos de demora, modulada por dopamina (óptimo en niveles moderados, curva U invertida). La memoria episódica se codifica mediante «células de lugar» del hipocampo (activas en localizaciones específicas, campo de 20-50 cm) y «células de tiempo» (codifican intervalos temporales de 1-30 s), formando un mapa cognitivo del espacio-tiempo.
Bases neuronales de la consciencia: integración y espacio de trabajo global
La teoría del espacio de trabajo neuronal global (Dehaene, Changeux) postula que la percepción consciente surge cuando se «enciende» una red distribuida de áreas prefrontales, parietales y temporales, transmitiendo información a través de conexiones cortico-corticales de largo alcance. Los estímulos conscientes provocan actividad tardía (>300 ms) con sincronización global en el rango gamma (30-80 Hz).
Los estímulos subliminales generan solo actividad temprana local (<200 ms) sin propagación. El daño en la corteza prefrontal o núcleos talámicos (núcleos intralaminares) altera la consciencia, confirmando su papel en la integración global.
- Estímulo consciente → encendido global tardío (>300 ms)
- Estímulo subliminal → actividad temprana local (<200 ms)
- Daño en corteza prefrontal → alteración de la integración
- Daño en núcleos talámicos → pérdida de consciencia
La teoría de la información integrada (Tononi) define cuantitativamente la consciencia mediante Φ (phi) —medida de integración causal del sistema: un Φ alto requiere equilibrio entre especialización funcional de módulos y su integración, maximizándose en el sistema tálamo-cortical.
Los correlatos neuronales de la consciencia (NCC) —mecanismos neuronales mínimos suficientes para una experiencia consciente específica— se localizan en «zonas calientes» corticales posteriores: corteza visual extraestriada (V2-V4) para consciencia visual, corteza temporo-parietal para autoconsciencia corporal.
La rivalidad binocular muestra que la actividad de V1 se correlaciona con el estímulo físico, mientras que V4 y la corteza temporal inferior lo hacen con la percepción subjetiva, señalando a V4 como zona crítica para la consciencia visual.
Los anestésicos (propofol, sevoflurano) suprimen la consciencia alterando la conectividad tálamo-cortical y reduciendo la complejidad del EEG (índice de complejidad perturbacional PCI de 0,5 en vigilia a 0,2 bajo anestesia), sin afectar la actividad local.
El estado vegetativo se caracteriza por actividad metabólica conservada (50-60% de la norma por PET), pero conectividad funcional fragmentada, mientras que el estado de consciencia mínima muestra recuperación parcial de conexiones de largo alcance y respuestas a comandos en el 20-40% de los casos.
Neuroplasticidad y Desarrollo — Cómo el Cerebro se Reestructura a lo Largo de la Vida
Formación de conexiones neuronales mediante sinaptogénesis y poda sináptica
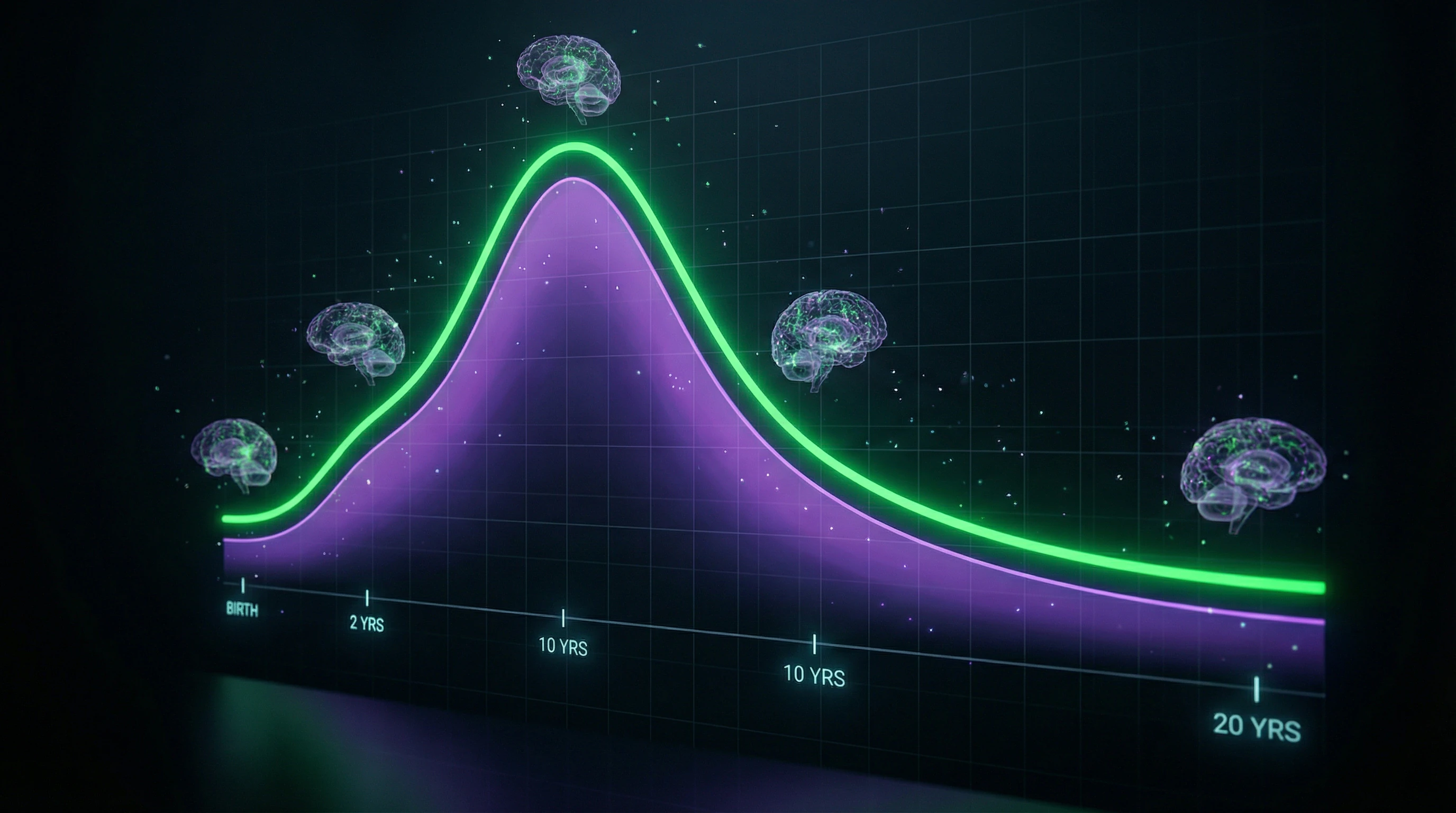
La sinaptogénesis alcanza su pico en diferentes períodos según las áreas: corteza visual — 3–4 meses (densidad sináptica hasta 150% del nivel adulto), corteza prefrontal — 1–2 años, seguida de poda sináptica que elimina hasta el 40% de las sinapsis durante la adolescencia.
El mecanismo depende de la actividad: las sinapsis frecuentemente utilizadas se estabilizan mediante la expresión de BDNF y receptores TrkB, mientras que las inactivas son marcadas por el complemento C1q y eliminadas por la microglía.
- Potenciación a largo plazo (LTP)
- Requiere activación de receptores NMDA, entrada de Ca²⁺ y fosforilación de receptores AMPA, aumentando la fuerza sináptica en 200–400% en minutos, con consolidación mediante síntesis proteica durante 1–3 horas.
- Ambiente enriquecido
- En roedores aumenta la densidad de espinas dendríticas en 25%, el volumen del hipocampo en 15% y la neurogénesis en el giro dentado en 50% comparado con condiciones estándar.
Períodos críticos del desarrollo cerebral y sus mecanismos moleculares
El período crítico para la visión binocular en humanos es de 3–8 años, cuando la deprivación monocular (estrabismo, cataratas) causa ambliopía irreversible debido al dominio del ojo abierto en la corteza visual.
La apertura y cierre de períodos críticos está regulada por el balance excitación/inhibición: la maduración de interneuronas positivas para parvalbúmina y redes perineuronales finaliza la plasticidad, mientras que su degradación con condroitinasa ABC en ratas adultas restaura la plasticidad juvenil.
El desarrollo lingüístico muestra un período crítico hasta los 7 años para la fonología (distinción de sonidos de la lengua materna) y hasta los 15 años para la sintaxis, con declive progresivo de la capacidad de adquisición de un segundo idioma sin acento de 0,7 puntos en la escala de dominio por cada año de retraso después de los 7 años.
La neurogénesis adulta persiste en la zona subgranular del hipocampo (700 neuronas nuevas/día en personas jóvenes, disminuyendo a 200/día a los 70 años) y la zona subventricular, con integración de nuevas neuronas en redes existentes durante 4–6 semanas.
Neurociencia Clínica — Patologías Cerebrales y Sus Fundamentos Neurobiológicos
Enfermedades neurodegenerativas y mecanismos de agregación proteica
La enfermedad de Alzheimer se construye sobre dos pilares patológicos: placas extracelulares de β-amiloide (Aβ42, oligomerizan a concentraciones >100 nM) y ovillos neurofibrilares intracelulares de proteína tau hiperfosforilada (fosforilación en 40+ sitios en lugar de 2-3 en condiciones normales). En la fase de demencia se pierde el 30-40% de las neuronas del hipocampo y la corteza entorrinal.
La patología se propaga según el esquema de Braak: estadios I-II (corteza entorrinal, sin síntomas) → III-IV (hipocampo, deterioro cognitivo leve) → V-VI (neocórtex, demencia grave). La correlación de la patología tau con el declive cognitivo (r=0,7-0,8) es significativamente más fuerte que para el amiloide (r=0,3-0,4).
| Enfermedad | Mecanismo primario | Proteína clave | Pérdida neuronal |
|---|---|---|---|
| Enfermedad de Parkinson | Muerte de neuronas dopaminérgicas de la sustancia negra | α-sinucleína (cuerpos de Lewy) | 60-80% al aparecer síntomas motores |
| ELA | Degeneración selectiva de motoneuronas | TDP-43 (97%) o SOD1 (20% casos familiares) | 2-3% unidades motoras/mes; supervivencia 3-5 años |
La enfermedad de Parkinson se propaga según la hipótesis de Braak: desde el bulbo olfatorio y el núcleo dorsal del vago hacia el mesencéfalo y la corteza. La esclerosis lateral amiotrófica (ELA) progresa con una pérdida del 2-3% de unidades motoras por mes, con una supervivencia mediana de 3-5 años desde el inicio de los síntomas.
Trastornos psiquiátricos y su neurobiología a nivel de circuitos
El trastorno depresivo mayor es un desequilibrio de actividad en la red prefrontal-límbica. La corteza prefrontal dorsolateral está hipoactiva (reducción del metabolismo del 15-25% por PET), la corteza cingulada anterior subgenual está hiperactiva (área 25 de Brodmann, +30-40%), el hipocampo se reduce un 8-10% en la depresión crónica debido a atrofia inducida por glucocorticoides.
La hipótesis monoaminérgica explica el efecto de los ISRS: aumentan la serotonina sináptica 3-5 veces, pero el efecto terapéutico aparece tras 2-4 semanas, ya que se requieren cambios neuroplásticos (aumento de BDNF, neurogénesis).
La esquizofrenia muestra un desequilibrio dopaminérgico: la vía mesolímbica está hiperactiva (receptores D2, +40-60% liberación de dopamina → síntomas positivos), la vía mesocortical está hipoactiva (corteza prefrontal → síntomas negativos y déficit cognitivo). La sustancia gris disminuye un 2-3%, los ventrículos se expanden un 20-30%.
El trastorno obsesivo-compulsivo (TOC) se caracteriza por hiperactividad del circuito orbitofrontal-estriado-tálamo-cortical: metabolismo en la corteza orbitofrontal +25-35%, en el núcleo caudado +15-20%. Tras terapia exitosa (ISRS o terapia cognitivo-conductual) la actividad se normaliza.
Neurotecnologías y Futuro — Interfaces y Modulación de la Actividad Cerebral
Interfaces cerebro-computadora y decodificación de la actividad neuronal
Las BCI invasivas con matrices de microelectrodos (Utah array, 96–128 electrodos) registran potenciales de acción de neuronas individuales de la corteza motora con resolución de 30 kHz. Esto permite decodificar la intención de movimiento con precisión del 90–95% y controlar extremidades robóticas con 7–10 grados de libertad en tiempo real (latencia <100 ms).
Los algoritmos de aprendizaje automático (redes neuronales recurrentes, filtros de Kalman) transforman patrones de actividad de 50–200 neuronas en trayectorias de movimiento. Los decodificadores co-adaptativos aprenden mediante refuerzo, ajustándose a los cambios en la señal.
- Las BCI no invasivas basadas en EEG utilizan P300 (potencial a los 300 ms tras el estímulo objetivo, amplitud 5–10 μV) o imágenes motoras (desincronización del ritmo μ 8–12 Hz en la corteza motora contralateral).
- El control de cursor o deletreador alcanza velocidades de 5–25 caracteres/minuto con precisión del 70–90%.
- La electrocorticografía (ECoG) con electrodos subdurales proporciona resolución intermedia (1–2 cm, 1 kHz), decodificando el habla con precisión del 75–90% para vocabulario limitado y 40–60% para habla libre.
Neuromodulación y aplicaciones terapéuticas de la estimulación cerebral
La estimulación cerebral profunda (DBS) del núcleo subtalámico en la enfermedad de Parkinson (130–185 Hz, 2–4 V, 60–90 μs) mejora los síntomas motores en 40–70% según la escala UPDRS y reduce la necesidad de levodopa en 50–60%. La eficacia se mantiene >10 años en el 70% de los pacientes.
Mecanismo: supresión de la oscilación β patológica (13–30 Hz) en los ganglios basales y normalización de la actividad tálamo-cortical. La DBS adaptativa, que regula la estimulación según los potenciales de campo locales (LFP), aumenta la eficacia en 20–30%.
La estimulación magnética transcraneal (TMS) de la corteza prefrontal dorsolateral (10 Hz, 3000 impulsos/sesión, 20–30 sesiones) muestra remisión de la depresión en 30–40% de pacientes resistentes a antidepresivos. El mecanismo incluye plasticidad tipo LTP y aumento del BDNF en 20–35%.
| Método | Parámetros | Efecto |
|---|---|---|
| tDCS (anódica) | 1–2 mA, 20–30 min | Aumenta la excitabilidad cortical en 30–40% |
| tDCS (catódica) | 1–2 mA, 20–30 min | Reduce la excitabilidad en 20–30% |
| tDCS + memoria de trabajo | Estimulación de áreas correspondientes | Mejora del 10–20% |
| tDCS + aprendizaje motor | Estimulación de áreas correspondientes | Aceleración del 15–25% |

Knowledge Access Protocol
FAQ
Preguntas Frecuentes
La neurociencia es un campo interdisciplinario que estudia la estructura, funciones y desarrollo del sistema nervioso. Integra biología, psicología, química y física para comprender el funcionamiento del cerebro, los mecanismos del comportamiento y los procesos cognitivos. Las investigaciones abarcan desde el nivel molecular hasta redes neuronales completas.
Las neuronas transmiten información mediante impulsos eléctricos y señales químicas en las sinapsis. Cuando el impulso alcanza el terminal neuronal, se liberan neurotransmisores que se unen a los receptores de la siguiente célula. Este proceso dura milisegundos y constituye la base de todas las funciones cerebrales.
La neuroplasticidad es la capacidad del cerebro para modificar su estructura y funciones en respuesta a la experiencia y el aprendizaje. Las conexiones neuronales pueden fortalecerse, debilitarse o formarse de nuevo a lo largo de toda la vida. Esta propiedad permite al cerebro recuperarse tras lesiones y adaptarse a nuevas condiciones.
No, es un mito extendido que ha sido refutado por la neuroimagen. Los estudios demuestran que todas las áreas cerebrales están activas y desempeñan funciones específicas, incluso en estado de reposo. Diferentes tareas activan distintas zonas, pero a lo largo del día se utiliza todo el cerebro.
La resonancia magnética muestra la actividad de áreas cerebrales, pero no «lee» pensamientos concretos. La resonancia magnética funcional registra cambios en el flujo sanguíneo relacionados con la actividad neuronal, permitiendo identificar qué zonas trabajan durante la realización de tareas. La decodificación de pensamientos complejos permanece fuera del alcance de las tecnologías actuales.
El consumo crónico y excesivo de alcohol puede causar daños irreversibles en las neuronas, especialmente en el hipocampo y la corteza prefrontal. Sin embargo, con consumo moderado y tras cesar la ingesta, el cerebro puede recuperarse parcialmente gracias a la neuroplasticidad. El grado de recuperación depende de la duración y gravedad del consumo.
Son eficaces el ejercicio físico regular, el sueño de calidad y la repetición espaciada de información. El ejercicio aeróbico estimula la neurogénesis en el hipocampo, mientras que el sueño consolida los recuerdos. También ayudan las técnicas mnemotécnicas, la actividad social y el aprendizaje de nuevas habilidades, que fortalecen las conexiones neuronales.
Los neurotransmisores son sustancias químicas que transmiten señales entre neuronas a través de las sinapsis. La dopamina regula la motivación y el placer, la serotonina el estado de ánimo, y el GABA la inhibición de la actividad nerviosa. El desequilibrio de neurotransmisores está relacionado con depresión, ansiedad y otros trastornos.
Las interfaces registran la actividad eléctrica cerebral mediante electrodos y la transforman en comandos para dispositivos. La tecnología utiliza EEG o sensores implantados para decodificar las intenciones del usuario. Se aplica para controlar prótesis, comunicación de pacientes paralizados y rehabilitación tras ictus.
Sí, los períodos críticos son ventanas temporales de máxima sensibilidad del cerebro a determinados estímulos. Por ejemplo, el desarrollo visual es más activo en los primeros años de vida, y las habilidades lingüísticas se adquieren mejor antes de la adolescencia. Tras el cierre de estas ventanas el aprendizaje es posible, pero menos eficaz.
Es una simplificación que no refleja la realidad. Ambos hemisferios participan en la mayoría de los procesos cognitivos, aunque tienen cierta especialización. Por ejemplo, el izquierdo está más asociado con el lenguaje, pero la creatividad requiere la interacción de ambos hemisferios. La neuroimagen muestra actividad compleja en cualquier tarea.
La enfermedad de Alzheimer se caracteriza por la acumulación de placas beta-amiloides y proteína tau en el cerebro, lo que provoca la muerte neuronal. Se ven afectadas las áreas responsables de la memoria y el pensamiento, especialmente el hipocampo y la corteza. El proceso comienza décadas antes de la aparición de síntomas y actualmente es irreversible.
La eficacia de la mayoría de los «entrenadores cerebrales» es limitada y no se transfiere a tareas cotidianas. Los estudios muestran que las mejoras son específicas para las tareas entrenadas. Son más útiles la actividad intelectual variada, el aprendizaje de idiomas, los instrumentos musicales y la actividad física.
El estrés crónico causa atrofia del hipocampo, deteriorando la memoria, y aumenta la amígdala, intensificando la ansiedad. El cortisol elevado daña las neuronas y suprime la neurogénesis. Sin embargo, estos cambios son parcialmente reversibles con la reducción del estrés, la meditación y la terapia.
La conciencia es el procesamiento integrado de información por redes neuronales distribuidas, especialmente en la corteza y el tálamo. Las teorías incluyen el espacio de trabajo global y la información integrada, pero no hay una comprensión completa. Las investigaciones estudian los correlatos neuronales de la conciencia en percepción, atención y autoconciencia.
Es un concepto teórico, lejos de la realización debido a la complejidad del cerebro y la falta de comprensión de la naturaleza de la conciencia. Se requiere el mapeo completo de 86 mil millones de neuronas y billones de sinapsis, así como reproducir su dinámica. Las cuestiones filosóficas sobre la identidad personal y la experiencia subjetiva permanecen sin resolver.
