Кандида и повышенная кишечная проницаемость: научные факты и мифыλ
Разбираем связь между грибковой микрофлорой и нарушением кишечного барьера на основе научных данных и клинических исследований
Overview
Термин «дырявый кишечник» мигрировал из альтернативной медицины в научный дискурс — за ним стоит измеримое явление: повышенная кишечная проницаемость. Candida albicans, обычный резидент микробиоты, при дисбалансе может разрушать плотные контакты эпителия 🧬 и провоцировать системное воспаление. Клинические данные связывают это с аутоиммунными состояниями, метаболическими нарушениями и хроническими воспалительными заболеваниями кишечника.
🛡️
Протокол Лапласа: Мы разделяем установленные научные факты о нарушении кишечного барьера от популярных упрощений, опираясь на рецензируемые исследования и клинические данные. Важно понимать разницу между доказанными механизмами и гипотезами, требующими дальнейшего изучения.
Reference Protocol
Научный фундамент
Доказательная база для критического анализа
Protocol: Evaluation
Проверь себя
Квизы по этой теме скоро появятся
⚡
Подробнее
Что на самом деле происходит с кишечным барьером при повышенной проницаемости
Научное определение и механизмы нарушения барьера
«Дырявый кишечник» — научно-популярный термин для повышенной кишечной проницаемости, состояния, при котором плотные контакты между эпителиальными клетками ослабевают и позволяют веществам из просвета кишки проникать в кровоток в увеличенных количествах.
Кишечный барьер — это многоуровневая система: слой слизи, эпителиальные клетки, плотные межклеточные соединения и иммунные компоненты слизистой оболочки. При её нарушении усиливается транспорт липополисахаридов грамотрицательных бактерий и других потенциально токсичных молекул через кишечную стенку.
| Компонент барьера | Функция | Что происходит при нарушении |
|---|---|---|
| Слой слизи | Физическая защита, среда для микробиоты | Снижение толщины, потеря защиты |
| Эпителиальные клетки | Селективный транспорт, метаболизм | Апоптоз, дисфункция, повышенная проницаемость |
| Плотные контакты (tight junctions) | Регуляция парацеллюлярного транспорта | Разрыв связей, неконтролируемый проход молекул |
| Иммунные компоненты | Распознавание патогенов, толерантность | Гиперактивация или дисрегуляция |
Повышенная проницаемость ассоциирована с хроническими заболеваниями почек, сердечно-сосудистыми и дерматологическими проблемами. Это не самостоятельный диагноз, а патофизиологический механизм, лежащий в основе множества заболеваний.
Роль плотных контактов между клетками эпителия
Плотные контакты (tight junctions) — ключевой элемент барьерной функции. Они формируют селективный барьер, регулирующий парацеллюлярный транспорт (движение веществ между клетками, а не через них).
- Трансмембранные белки
- Окклюдин, клаудины, JAM — пронизывают мембрану и создают физический затвор между клетками.
- Цитоплазматические белки
- ZO-1, ZO-2, ZO-3 — связывают комплекс с цитоскелетом, обеспечивая механическую прочность.
- Нарушение структуры
- Любой дефект в этих белках приводит к увеличению проницаемости и проникновению крупных молекул.
Провоспалительные цитокины, бактериальные токсины, изменения pH и окислительный стресс — всё это может нарушить целостность плотных контактов.
При дисфункции плотных контактов бактериальные компоненты и непереваренные пищевые антигены получают доступ к подслизистому слою, где взаимодействуют с иммунными клетками. Это инициирует локальное и системное воспаление, создавая порочный круг: воспаление дополнительно нарушает барьерную функцию.
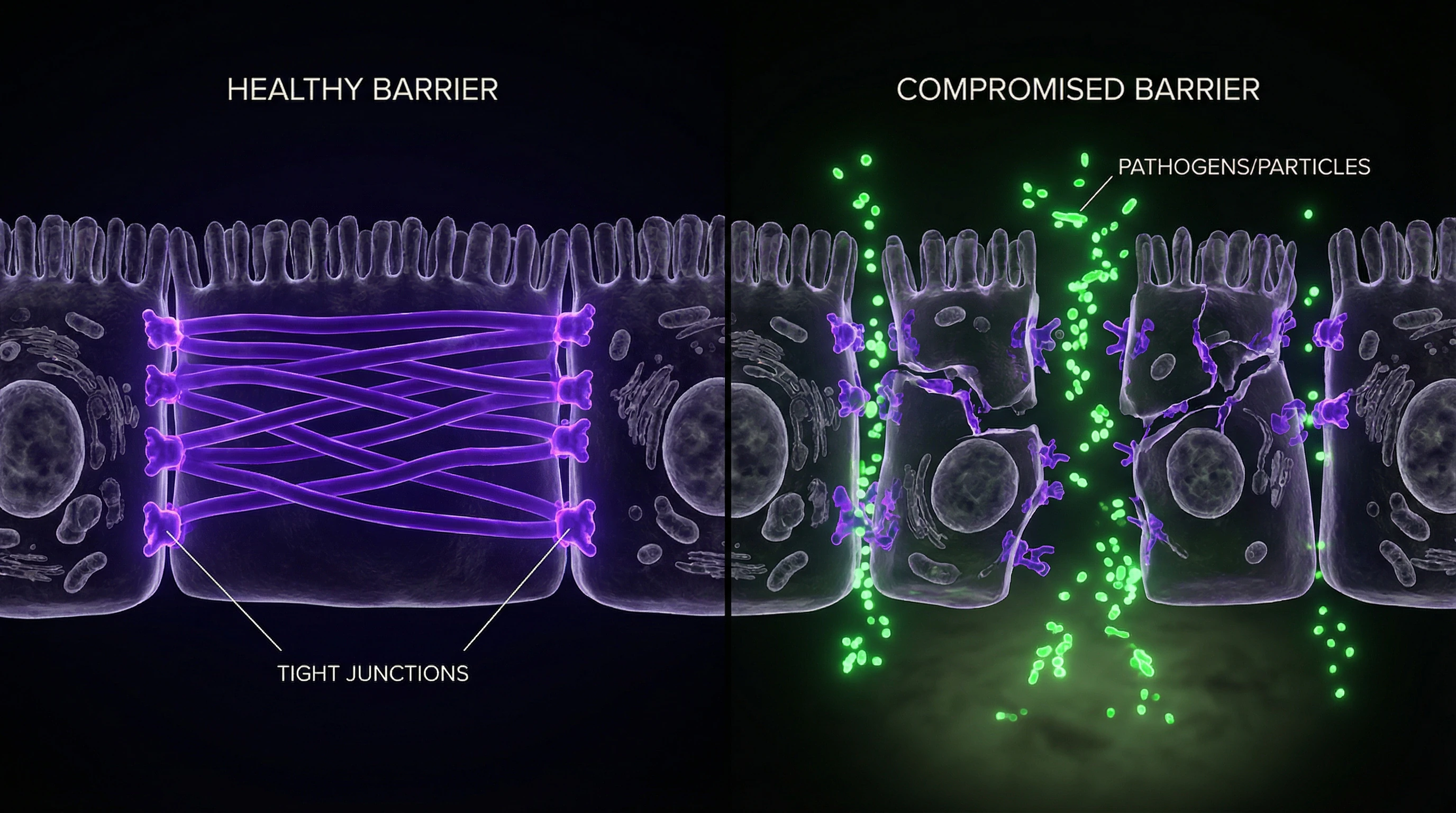
Candida в кишечнике: от нормального обитателя до патогена
Комменсальная роль грибов в составе микробиоты
Candida albicans — естественный обитатель кишечника, входит в состав нормальной микробиоты и существует в сбалансированных количествах без патологических последствий. Кишечная экосистема держится на динамическом равновесии между бактериями, грибами, вирусами и археями.
Candida сдерживается конкурентными взаимодействиями с бактериальной флорой и иммунным надзором хозяина. В небольших количествах эти грибы могут участвовать в метаболических процессах и тренировке иммунной системы.
- pH среды кишечника
- Доступность питательных веществ
- Продукция антимикробных пептидов эпителием
- Секреция иммуноглобулинов
Условия для избыточного роста и трансформации в патоген
Неконтролируемая пролиферация Candida начинается с дисбиоза — нарушения микробного баланса. Антибиотики широкого спектра уничтожают конкурирующие бактерии, освобождая ниши для оппортунистических микроорганизмов.
При избыточном росте Candida переходит из дрожжевой формы в гифальную (мицелиальную) — более инвазивную и способную повреждать ткани.
Иммунная дисфункция — критический фактор развития кандидоза. Здоровая иммунная система эффективно контролирует популяцию грибов; её нарушение при ВИЧ-инфекции, приёме кортикостероидов, химиотерапии или врождённых иммунодефицитах создаёт условия для инвазии.
Дополнительные триггеры: диета с высоким содержанием простых углеводов (питательный субстрат для грибов), хронический стресс и гормональные изменения. При создании благоприятных условий Candida запускает каскад патологических изменений, затрагивающих не только кишечник.
Механизмы воздействия Candida на проницаемость кишечного барьера
Прямое повреждение эпителия и плотных контактов
Candida albicans атакует кишечный барьер несколькими путями одновременно. Гифальная форма гриба физически проникает между эпителиальными клетками и инвазирует их, механически нарушая целостность монослоя.
Грибы секретируют протеолитические ферменты — секретируемые аспартильные протеазы и фосфолипазы, которые разрушают белки плотных контактов, особенно окклюдин. Результат: парацеллюлярная проницаемость растет.
- Кандидолизин (цитолитический пептидный токсин) формирует поры в мембранах эпителиальных клеток, вызывая их гибель
- Адгезины на поверхности грибов (Als3) обеспечивают прикрепление и индуцируют эндоцитоз — грибы проникают внутрь клеток
- Биопленки создают защищенную среду, усиливая резистентность к иммунным факторам и противогрибковым препаратам
Совокупность этих механизмов приводит к структурному нарушению барьера и увеличению проницаемости для различных молекул.
Роль дисбиоза и иммунного ответа в нарушении барьера
Избыточный рост Candida — одновременно следствие и причина микробного дисбаланса. Дисбиоз означает снижение разнообразия микробиоты, уменьшение полезных бактерий (особенно продуцентов короткоцепочечных жирных кислот) и рост условно-патогенных микроорганизмов.
Короткоцепочечные жирные кислоты, прежде всего бутират, обеспечивают энергией колоноциты и регулируют экспрессию белков плотных контактов. При дисбиозе их продукция падает — барьер ослабевает.
Иммунный ответ на избыточный рост Candida парадоксально усугубляет повреждение. Распознавание грибковых паттернов (Dectin-1, TLR2, TLR4) активирует продукцию провоспалительных цитокинов: TNF-α, IL-1β, IL-6, IL-17.
| Цитокин | Механизм повреждения барьера |
|---|---|
| TNF-α, IFN-γ | Непосредственно нарушают функцию плотных контактов, увеличивая проницаемость |
| IL-1β, IL-6, IL-17 | Поддерживают хроническое воспаление, усиливают иммунную активацию |
Хроническое воспаление создает порочный круг: повышенная проницаемость позволяет большему количеству антигенов проникать через барьер, что усиливает иммунную активацию и дальнейшее повреждение.
Нарушения кишечной микробиоты влияют даже на отдаленные исходы — например, на спонтанные преждевременные роды, демонстрируя системное значение кишечного барьера.
Научные доказательства и ограничения исследований связи кандиды с проницаемостью кишечника
Что подтверждено клиническими исследованиями
Повышенная кишечная проницаемость — реальный клинический феномен, документированный при хронической болезни почек, сердечно-сосудистых заболеваниях и дерматологических состояниях. Это указывает на системное значение барьерной функции кишечника.
Роль микробиоты в патогенезе заболеваний получила значительное научное подтверждение. Микробно-тканевой комплекс влияет на межиндивидуальную вариабельность исходов здоровья.
Candida albicans признана комменсальным организмом, способным становиться патогенной при определенных условиях — особенно на фоне антибиотикотерапии и иммунной дисфункции.
Механизмы повреждения барьера изучены детально: эндогенные и экзогенные факторы нарушают плотные контакты между эпителиальными клетками, увеличивая транспорт липополисахаридов грамотрицательных бактерий в кровоток.
| Фактор | Механизм действия | Статус доказательности |
|---|---|---|
| TNF-α, IFN-γ | Прямое нарушение белков плотных контактов | Подтверждено |
| Дисбиоз микробиоты | Связь с системными заболеваниями | Корреляционные данные |
| Candida-индуцированное воспаление | Порочный круг воспаления и проницаемости | Требует уточнения |
Области требующие дальнейшего изучения
Прямые доказательства специфической связи между кандидозом и синдромом повышенной проницаемости остаются ограниченными. Большинство доступных данных носят корреляционный, а не причинно-следственный характер.
Термин "дырявый кишечник" используется как в научном, так и в псевдонаучном контексте, создавая терминологическую путаницу и затрудняя интерпретацию исследований.
Систематические обзоры по этой конкретной теме немногочисленны. Нарративные обзоры могут подвергаться субъективному влиянию авторов.
Специфические пути, связывающие дисфункцию кишечника с системными заболеваниями, остаются предметом активных исследований, особенно в контексте осей "кишечник-орган".
Влияние материнской кишечной микробиоты на отдаленные исходы, такие как преждевременные роды, демонстрирует сложность системных взаимодействий, которые еще предстоит полностью расшифровать.
Необходимы рандомизированные контролируемые исследования для оценки эффективности терапевтических вмешательств, направленных на восстановление барьера при кандидозе.

Факторы риска и триггеры нарушения кишечного барьера при кандидозе
Антибиотики и иммуносупрессия
Антибиотикотерапия широкого спектра уничтожает конкурирующие бактериальные популяции, которые в норме сдерживают грибковую колонизацию. Это один из наиболее значимых факторов риска избыточного роста Candida в кишечнике.
Иммуносупрессивные состояния — ВИЧ-инфекция, химиотерапия, длительное применение кортикостероидов, иммунодефицитные синдромы — трансформируют комменсальную Candida в патогенную форму. Нарушение локального иммунитета слизистой оболочки (снижение секреторного IgA, дисфункция Th17-ответа) ослабляет защиту против грибковой инвазии.
Сочетание антибиотикотерапии и иммуносупрессии создает синергетический эффект, драматически повышая риск системного кандидоза и повреждения барьера.
Диета и образ жизни
Диета с высоким содержанием рафинированных углеводов и сахаров — основной источник энергии для грибов. Хронический стресс активирует гипоталамо-гипофизарно-надпочечниковую ось, повышает кортизол и изменяет состав микробиоты.
Злоупотребление алкоголем непосредственно повреждает кишечный эпителий, нарушает плотные контакты и способствует дисбиозу. Недостаточное потребление пищевых волокон снижает продукцию короткоцепочечных жирных кислот, необходимых для целостности эпителиального барьера и регуляции иммунного ответа.
| Фактор риска | Механизм воздействия | Последствие для барьера |
|---|---|---|
| Антибиотики широкого спектра | Элиминация конкурирующих бактерий | Неконтролируемый рост Candida |
| Иммуносупрессия | Снижение локального IgA и Th17 | Грибковая инвазия в эпителий |
| Высокоуглеводная диета | Энергетический субстрат для грибов | Пролиферация Candida |
| Хронический стресс | Гиперкортизолемия, дисбиоз | Повышение проницаемости |
| Алкоголь | Прямое повреждение эпителия | Нарушение плотных контактов |
| Дефицит пищевых волокон | Снижение короткоцепочечных жирных кислот | Ослабление барьера и иммунитета |
Диагностика и доказательные подходы к восстановлению кишечного барьера
Клинические методы оценки
Диагностика повышенной кишечной проницаемости остается сложной задачей из-за отсутствия стандартизированных тестов и четких диагностических критериев. Три основных подхода используются в практике, но каждый имеет ограничения.
| Метод | Принцип | Статус в клинике |
|---|---|---|
| Лактулоза-маннитол | Соотношение экскреции сахаров с мочой | Исследовательский; низкая доступность |
| Зонулин в сыворотке | Биомаркер проницаемости | Дискуссионная специфичность и значимость |
| Микробиология кала | Количественная оценка Candida | Стандарт для диагностики кандидоза |
Ключевой момент: простое присутствие Candida в кале — норма для здоровых людей. Диагноз требует количественной оценки грибковой нагрузки, а не просто обнаружения.
Доказательные стратегии восстановления барьера
Противогрибковая терапия флуконазолом или нистатином показана только при документированном избыточном росте Candida и под медицинским наблюдением. Назначение без микробиологического подтверждения — ошибка диагностического мышления.
Пробиотические штаммы Lactobacillus rhamnosus GG и Saccharomyces boulardii конкурируют с Candida и поддерживают барьерную функцию, но эффективность зависит от штамма и дозы. Это не универсальное решение.
Диетические вмешательства — ограничение рафинированных углеводов и увеличение пищевых волокон — модулируют микробиоту и улучшают метаболическое здоровье кишечника. Это базовый уровень, который должен быть первым шагом.
Глутамин, бутират и нутриенты, поддерживающие энергетический метаболизм энтероцитов, показывают потенциал в восстановлении целостности эпителия, но требуют дальнейших клинических исследований для определения оптимальных протоколов.
Комплексный протокол и риски самолечения
Восстановление кишечного барьера требует устранения провоцирующих факторов: необоснованное применение антибиотиков, коррекция иммунного статуса, модификация образа жизни. Это системный подход, а не точечное вмешательство.
Самодиагностика и самолечение без медицинского наблюдения несут реальные риски. Симптомы, приписываемые «дырявому кишечнику» и кандидозу, могут маскировать серьезные заболевания, требующие специфической терапии.
Индивидуализация терапевтических протоколов на основе клинической картины, лабораторных данных и факторов риска — ключ к эффективному восстановлению барьерной функции. Универсальных схем не существует.
Knowledge Access Protocol
FAQ
Часто задаваемые вопросы
Это популярное название повышенной кишечной проницаемости, когда нарушаются плотные контакты между клетками кишечника. В результате через кишечную стенку проникают вещества, которые в норме не должны попадать в кровоток — бактериальные токсины, непереваренные частицы пищи. Научный термин — нарушение структурно-функциональной целостности кишечного барьера.
Избыточный рост Candida может способствовать нарушению кишечного барьера, но не является единственной причиной. При дисбиозе грибки выделяют токсины и ферменты, которые повреждают эпителий кишечника. Однако прямая причинно-следственная связь требует дополнительных исследований — это многофакторный процесс.
Специфических симптомов нет — проявления неспецифичны и включают вздутие, нарушения стула, пищевые непереносимости, хроническую усталость. Могут возникать кожные проблемы, аллергические реакции, воспалительные процессы в разных органах. Диагноз ставится только врачом на основе комплексного обследования, а не по отдельным симптомам.
Да, антибиотики уничтожают не только патогенные, но и полезные бактерии, создавая условия для роста грибков. Candida устойчива к антибактериальным препаратам и занимает освободившуюся экологическую нишу. Особенно высок риск при длительных или повторных курсах антибиотикотерапии без пробиотической поддержки.
Диета — важный, но не единственный компонент восстановления кишечного барьера. Исключение провоцирующих продуктов (сахар, алкоголь, рафинированные углеводы) и добавление противовоспалительных нутриентов помогает, но требуется комплексный подход. Необходима работа с причинами: стресс, инфекции, медикаменты, под контролем специалиста.
В клинической практике используют тесты на зонулин (маркер проницаемости), липополисахариды (LPS), антитела к компонентам кишечной стенки. Также применяют лактулозо-маннитоловый тест и оценку кальпротектина. Однако стандартизированных протоколов диагностики пока нет — интерпретация результатов требует опыта врача.
Нет, Candida присутствует в кишечнике большинства здоровых людей как часть нормальной микробиоты. Проблемы возникают только при избыточном росте на фоне ослабленного иммунитета, дисбиоза или других факторов. Носительство грибков не равно заболеванию — важен баланс микроорганизмов.
Пробиотики могут поддерживать восстановление микробиоты и конкурировать с Candida за ресурсы, но не являются самостоятельным лечением. Эффективность зависит от штаммов, дозировок и индивидуальных особенностей. Лучшие результаты достигаются в комплексе с диетой, устранением триггеров и, при необходимости, противогрибковой терапией.
Да, хронический стресс напрямую повышает кишечную проницаемость через ось «мозг-кишечник». Гормоны стресса (кортизол) нарушают плотные контакты между клетками эпителия и меняют состав микробиоты. Это создает порочный круг: стресс ухудшает барьер, а нарушенный барьер усиливает воспаление и стрессовую реакцию.
Да, Candida использует простые углеводы (сахар, белую муку) как основной источник энергии для роста. Высокоуглеводная диета создает благоприятную среду для размножения грибков. Однако полное исключение углеводов не требуется — важен баланс и качество углеводов (предпочтение сложным, с клетчаткой).
Исследования показывают связь между повышенной кишечной проницаемостью и некоторыми аутоиммунными состояниями, но причинно-следственная связь не доказана окончательно. Нарушенный барьер может пропускать антигены, провоцирующие иммунный ответ. Однако неясно, что первично — проницаемость или аутоиммунный процесс; это область активных исследований.
Нет, самодиагностика ненадежна — симптомы кандидоза неспецифичны и совпадают с множеством других состояний. Популярные «домашние тесты» (например, со стаканом воды) не имеют научного обоснования. Диагноз требует лабораторных анализов (посев кала, ПЦР) и оценки клинической картины врачом-гастроэнтерологом или инфекционисто��.
Полезны продукты, богатые глютамином (костный бульон, мясо), омега-3 (жирная рыба), полифенолами (ягоды, зелень), цинком (семена тыквы). Ферментированные продукты (квашеная капуста, кефир) поддерживают микробиоту. Важна клетчатка из овощей для питания полезных бактерий, производящих короткоцепочечные жирные кислоты, укрепляющие барьер.
Сроки индивидуальны и зависят от степени повреждения, причин и соблюдения рекомендаций — от нескольких недель до нескольких месяцев. Эпителий кишечника обновляется каждые 3-5 дней, но восстановление функции барьера и микробиоты требует больше времени. Важна последовательность: устранение триггеров, противовоспалительная диета, поддержка микробиоты.
Да, системные противогрибковые средства могут нарушать баланс микробиоты, хотя и в меньшей степени, чем антибиотики. Они воздействуют не только на патогенные грибки, но и на комменсальные микроорганизмы. Поэтому назначаются строго по показаниям, курсами, с одновременной пробиотической поддержкой и под контролем врача.
Исследования показывают возможную связь через ось «кишечник-мозг»: дисбиоз и воспаление могут влиять на нейротрансмиттеры и настроение. Токсины Candida теоретически могут воздействовать на ЦНС при повышенной проницаемости. Однако прямые доказательства ограничены — это перспективное направление исследований, требующее осторожной интерпретации.
