Кишечные паразиты: влияние на микробиом и здоровье кишечникаλ
Научно обоснованный подход к пониманию связи между паразитарными инфекциями, составом микробиоты и функциональным здоровьем пищеварительной системы
Overview
Кишечные паразиты меняют состав микробиоты — 🧬 это не миф, а измеримый эффект с последствиями для иммунитета, усвоения нутриентов и барьерной функции кишечника. Механизм: конкуренция за ресурсы, токсины, воспаление слизистой. Группа риска — иммуносупрессия (химиотерапия, ВИЧ, трансплантация), но большинство «паразитарных паник» в соцсетях строится на подмене корреляции причинностью и игнорировании базовых ставок.
🛡️
Протокол Лапласа: Диагностика паразитарных инфекций требует лабораторного под��верждения. Самодиагностика по симптомам и профилактические «чистки» без медицинских показаний не рекомендуются. Лечение должно назначаться только после подтверждения диагноза квалифицированным специалистом.
Reference Protocol
Научный фундамент
Доказательная база для критического анализа
Navigation Matrix
Подразделы
[candida-leaky-gut]
Кандида и дырявый кишечник
Разбираем связь между грибковой микрофлорой и нарушением кишечного барьера на основе научных данных и клинических исследований
Изучить
[everyone-has-parasites]
У всех есть паразиты
Популярное утверждение о том, что паразиты есть у всех людей, не подтверждается научными данными и используется для продажи сомнительных продуктов.
Изучить
Protocol: Evaluation
Проверь себя
Квизы по этой теме скоро появятся
⚡
Подробнее
Типы кишечных паразитов и механизмы инфекции: что живёт в кишечнике
Кишечные паразиты — разнородная группа организмов, колонизирующих желудочно-кишечный тракт и питающихся за счёт хозяина. Выделяют две основные категории: гельминты (многоклеточные черви) и простейшие (одноклеточные организмы), каждая с уникальными механизмами взаимодействия.
Понимание биологии этих паразитов критично для разработки эффективных диагностических и терапевтических подходов.
Гельминты и простейшие: биологическая классификация
Гельминты включают три основных класса: нематоды (круглые черви), цестоды (ленточные черви) и трематоды (сосальщики). Каждый класс обладает специфическими морфологическими характеристиками и жизненными циклами.
Почвенные гельминты (soil-transmitted helminths, STH) широко распространены в африканских популяциях и демонстрируют измеримые корреляции с составом кишечного микробиома. Простейшие паразиты — лямблии, амёбы — характеризуются более коротким жизненным циклом и способностью к быстрому размножению в кишечной среде.
- Механизм воздействия гельминтов
- Механическое повреждение слизистой оболочки и конкуренция за питательные вещества.
- Механизм воздействия простейших
- Нарушение процессов всасывания и провокация локального воспаления.
- Парадокс размера
- Микроскопические простейшие могут вызывать более выраженную симптоматику, чем крупные гельминты.
Хроническая инфекция приводит к продукции токсинов и метаболитов, которые системно влияют на иммунную и нервную системы хозяина.
Пути передачи и факторы риска инфицирования
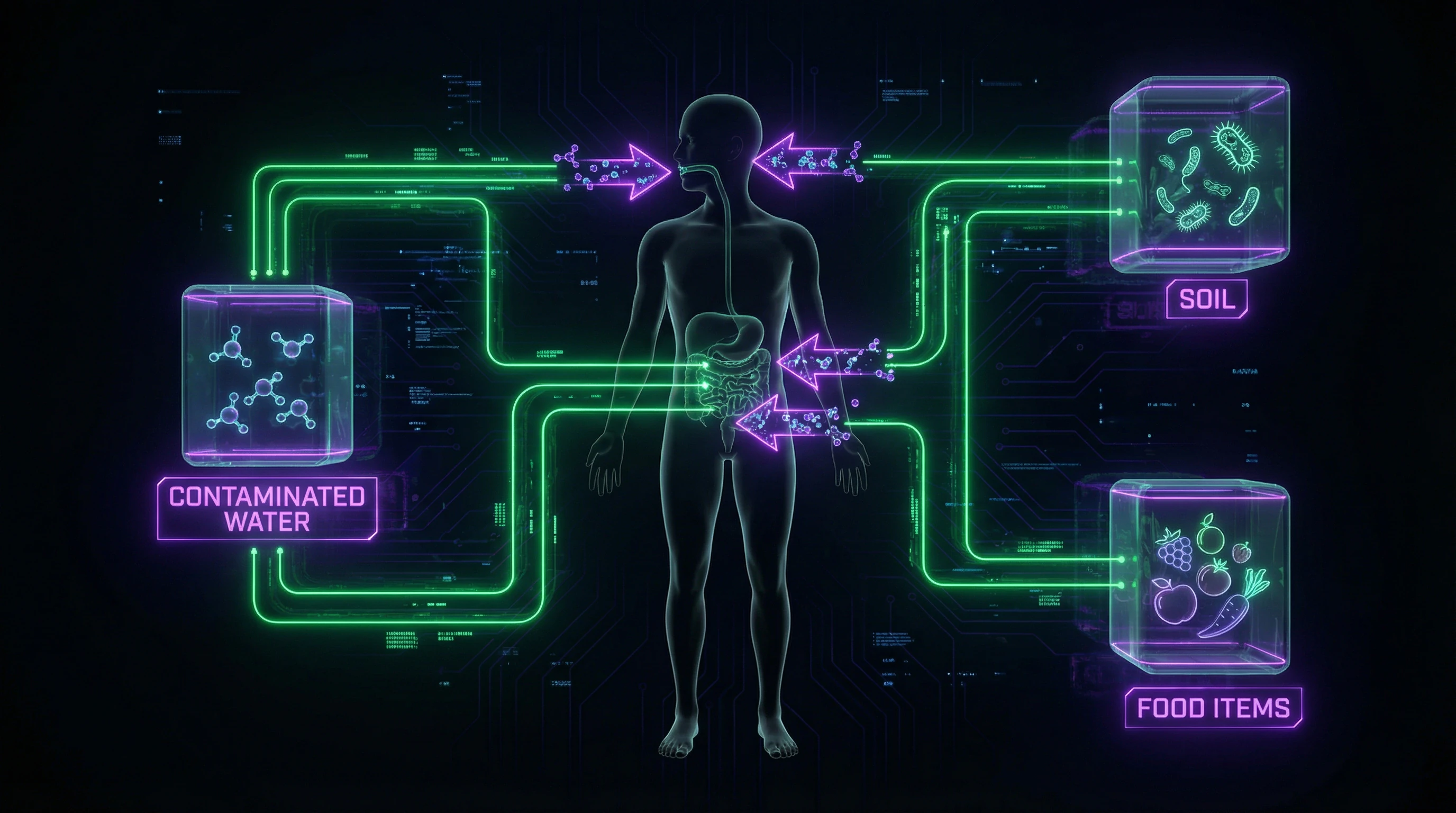
Основные пути передачи: фекально-оральный механизм через контаминированную воду и пищу, прямой контакт с заражённой почвой, трансмиссия через промежуточных хозяев.
| Фактор риска | Влияние на передачу |
|---|---|
| Географические и санитарные условия | Регионы с недостаточной очисткой воды и низким уровнем гигиены демонстрируют значительно более высокую заболеваемость |
| Иммунный статус | Иммунокомпрометированные пациенты проявляют повышенную восприимчивость из-за ослабленных защитных механизмов |
| Тип паразита | Почвенные гельминты требуют контакта с заражённой землёй; простейшие передаются через некипячёную воду |
| Сезонность | Пики инфицирования в периоды повышенной влажности и температуры |
| Профессиональная деятельность | Работа с сельским хозяйством или почвой существенно увеличивает вероятность заражения гельминтами |
Взаимодействие паразитов с кишечным микробиомом: изменение экосистемы
Присутствие кишечных паразитов инициирует каскад изменений в составе и функциональной активности кишечного микробиома — сложного сообщества микроорганизмов, играющих ключевую роль в пищеварении, иммунитете и гомеостазе организма. Современные метагеномные исследования выявили измеримые корреляции между паразитарными инфекциями и разнообразием микробиоты.
Эти взаимодействия носят двунаправленный характер: паразиты модифицируют микробное окружение, а микробиом влияет на выживаемость и вирулентность паразитов.
Влияние на разнообразие микробиоты
Паразитарные инфекции демонстрируют статистически значимые ассоциации с изменениями альфа- и бета-разнообразия кишечного микробиома, что подтверждено анализом метагеномных данных из африканских популяций. Почвенные гельминты коррелируют с увеличением общего микробного разнообразия, что может отражать адаптивный иммунный ответ или прямое влияние паразитарных метаболитов на микробную экологию.
Корреляция не означает причинно-следственную связь. Множественные факторы — диета, география, санитария — влияют на наблюдаемые паттерны микробного разнообразия.
Снижение разнообразия микробиоты ассоциируется с определёнными типами паразитарных инфекций, особенно при хронических простейших инвазиях, что может приводить к дисбиозу и нарушению барьерной функции кишечника.
- Конкуренция за питательные субстраты между паразитом и микробиотой
- Продукция антимикробных веществ паразитами
- Модуляция локального иммунного ответа, влияющая на микробный состав
Восстановление микробного разнообразия после элиминации паразитов происходит постепенно и может требовать дополнительных пробиотических вмешательств.
Изменения бактериального состава при инфекции
Специфические таксономические сдвиги в составе микробиома наблюдаются при различных паразитарных инфекциях: увеличение представленности провоспалительных бактерий семейства Enterobacteriaceae и снижение численности полезных комменсалов, таких как Faecalibacterium prausnitzii.
У иммунокомпрометированных пациентов выявлены особые паттерны изменений микробиоты, отличающиеся от таковых у иммунокомпетентных индивидов, что указывает на роль иммунного статуса в формировании микробно-паразитарных взаимодействий. Эти изменения могут усугублять клинические проявления и влиять на эффективность терапии.
| Функциональное нарушение | Механизм | Клиническое значение |
|---|---|---|
| Снижение короткоцепочечных жирных кислот | Потеря бутиратпродуцирующих бактерий | Ослабление барьера кишечника, воспаление |
| Нарушение метаболизма желчных кислот | Изменение микробного состава | Дисрегуляция липидного обмена |
| Снижение синтеза витаминов B и K | Элиминация синтезирующих штаммов | Дефицит микронутриентов, нарушение коагуляции |
Паразиты могут селективно подавлять рост определённых бактериальных штаммов через секрецию специфических молекул или изменение pH кишечной среды. Восстановление нормального бактериального состава после антипаразитарной терапии не всегда происходит спонтанно и может требовать целенаправленной модуляции микробиома.
Клинические проявления и симптомы: от локальных до системных эффектов
Паразитарные инфекции проявляются спектром от бессимптомного носительства до тяжёлых системных нарушений. Симптомы часто неспецифичны и имитируют гастроэнтерологические, иммунологические или психиатрические расстройства, что затрудняет диагностику.
Одних симптомов недостаточно для подтверждения инфекции — необходима лабораторная верификация.
Системные эффекты паразитарных инфекций
Хроническое воспаление, индуцированное паразитами, — ключевой механизм системных проявлений: хроническая усталость, анемия, дерматологические проблемы. Токсины и метаболиты паразитов проникают через повреждённую кишечную стенку в системный кровоток, влияя на отдалённые органы и системы.
Связь между паразитарными инфекциями и депрессией упоминается в популярных источниках, но прямая причинно-следственная связь не установлена. Депрессия — мультифакториальное расстройство; хроническая инфекция может быть лишь одним из множества способствующих факторов.
Аллергические реакции и кожные проявления возникают вследствие иммунной гиперреактивности на паразитарные антигены, но паразиты не единственная причина дерматологических состояний. Анемия развивается из-за кровопотери при инвазии гематофагами или нарушения всасывания железа и витамина B12.
Иммуномодулирующие эффекты паразитов могут как подавлять, так и чрезмерно активировать иммунную систему, приводя к аутоиммунным феноменам или повышенной восприимчивости к вторичным инфекциям.
Нарушения пищеварения и иммунитета
Мальабсорбция питательных веществ — прямое следствие повреждения кишечного эпителия и конкуренции паразитов за нутриенты. Развивается дефицит витаминов, минералов и белков.
- Нарушение барьерной функции кишечника способствует транслокации бактериальных компонентов и паразитарных антигенов в системный кровоток, хотя клиническая значимость остаётся предметом научных дебатов.
- Диспептические симптомы — диарея, запоры, вздутие, абдоминальная боль — возникают вследствие механического раздражения, воспаления и нарушения моторики кишечника.
- Иммунная дисрегуляция проявляется сдвигом в сторону Th2-ответа с повышенной продукцией IgE и эозинофилией, что усугубляет аллергические состояния.
Хроническая стимуляция иммунной системы паразитарными антигенами приводит к истощению иммунных резервов и парадоксальному снижению противоинфекционной защиты.
Диагностика требует комплексного лабораторного обследования: микроскопия кала, серологические тесты, молекулярно-генетические методы для точной идентификации возбудителя.
Диагностика паразитарных инфекций: от симптомов к лабораторному подтверждению
Лабораторные методы исследования
Микроскопическое исследование кала — золотой стандарт диагностики кишечных паразитов. Требуется трёхкратный забор с интервалом 3–5 дней для чувствительности 85–90%.
Метод концентрации по Като-Кац количественно оценивает интенсивность инвазии гельминтами — критично для выбора лечения и эпидемиологического мониторинга.
| Метод | Специфичность | Что выявляет | Ограничение |
|---|---|---|---|
| Микроскопия кала | 85–90% | Яйца, личинки, трофозоиты | Требует повторных проб |
| ПЦР | 95–99% | Видовая идентификация, криптоспоридии, микроспоридии | Дороже, не везде доступна |
| ИФА (серология) | Вариабельна | Антитела IgM/IgG | Не различает активную и перенесённую инфекцию |
| Копрология | — | pH, непереваренные волокна, жирные кислоты | Дополнительный метод |
Серологические тесты (ИФА) выявляют специфические антитела к паразитарным антигенам, но положительный результат может означать как активную инфекцию, так и перенесённую — требует клинической интерпретации.
Молекулярно-генетические методы (ПЦР) обеспечивают высокую специфичность и идентифицируют паразитов на видовом уровне, включая криптоспоридии и микроспоридии, трудно выявляемые микроскопически.
Эозинофилия периферической крови (>5% или >500 клеток/мкл) — косвенный маркер гельминтозов, особенно в миграционной фазе, но неспецифична и требует дифференциальной диагностики с аллергическими состояниями.
Дифференциальная диагностика
Симптомы паразитарных инфекций часто неспецифичны и перекрываются с воспалительными заболеваниями кишечника (ВЗК), синдромом раздраженного кишечника (СРК) и целиакией.
Хроническая диарея с примесью крови может указывать как на амебиаз, так и на язвенный колит. Эндоскопическое исследование с биопсией выявляет характерные язвы и трофозоиты Entamoeba histolytica в тканях.
Эозинофильный гастроэнтерит, вызванный тканевыми гельминтами, отличают от аллергических реакций на пищу и лекарства путём исключающей диеты и провокационных тестов.
У иммунокомпрометированных пациентов (онкологические больные, ВИЧ-инфицированные) паразитозы протекают атипично и часто сочетаются с оппортунистическими инфекциями.
Криптоспоридиоз и изоспороз при ВИЧ проявляются профузной диареей, имитирующей холеру. Требуются специальные методы окраски (Циля-Нильсена) для выявления ооцист.
Лабораторные маркеры воспаления (СРБ, фекальный кальпротектин) повышены как при паразитозах, так и при ВЗК. Значения >250 мкг/г более характерны для болезни Крона и язвенного колита.
Научно обоснованные подходы к лечению паразитарных инфекций
Антипаразитарная терапия
Выбор антигельминтного препарата зависит от вида паразита, интенсивности инвазии и состояния пациента. Самолечение без лабораторного подтверждения недопустимо: риск токсических эффектов и развития резистентности.
| Препарат | Спектр действия | Дозировка | Механизм |
|---|---|---|---|
| Альбендазол | Нематоды, некоторые цестоды | 400 мг однократно или 3 дня | Ингибирование полимеризации тубулина |
| Празиквантел | Трематоды, цестоды | 10–25 мг/кг (зависит от вида) | Высокая эффективность (85–95%), низкая токсичность |
| Метронидазол | Амебиаз, лямблиоз | 750 мг × 3 раза, 7–10 дней | Специфическая терапия протозойных инфекций |
| Нитазоксанид | Криптоспоридиоз | По схеме (иммунокомпетентные пациенты) | Альтернатива при резистентности |
Контроль эффективности проводится через 2–4 недели повторным паразитологическим исследованием кала. Персистенция паразитов указывает на резистентность или реинфекцию.
У онкологических пациентов дозировки требуют коррекции: миелосупрессия и гепатотоксичность химиотерапии меняют фармакокинетику антипаразитарных средств.
Восстановление микробиома после лечения
Антипаразитарная терапия, особенно метронидазол и антибиотики широкого спектра, вызывает дисбиоз: снижение разнообразия микробиоты и уменьшение популяций бактерий-продуцентов короткоцепочечных жирных кислот.
Восстановительная схема включает три компонента:
- Пробиотики (4–8 недель после лечения): Lactobacillus rhamnosus GG, Saccharomyces boulardii, Bifidobacterium longum — снижают частоту постинфекционного СРК.
- Пребиотики (5–10 г/день): инулин, фруктоолигосахариды стимулируют рост собственной полезной микрофлоры.
- Диетическая коррекция: ферментированные продукты (кефир, квашеная капуста), пищевые волокна (25–30 г/день) поддерживают восстановление и барьерную функцию кишечника.
Метагеномный анализ показывает: полное восстановление микробного разнообразия занимает 3–6 месяцев. У части пациентов сохраняются долгосрочные изменения состава микробиоты.
Мониторинг функциональных показателей (частота стула, абдоминальные симптомы) и при необходимости повторный анализ микробиома позволяют оценить эффективность восстановительной терапии.
Профилактика паразитарных инфекций и управление рисками
Санитарные практики и безопасность пищи
Мытьё рук с мылом после туалета, контакта с почвой и перед едой снижает риск фекально-орального заражения на 40–50%. Это самая эффективная и доступная профилактическая мера.
Термическая обработка мяса до 63°C для свинины и 71°C для говядины уничтожает личинки трихинелл и цистицерки. Овощи и фрукты в сыром виде промывают проточной водой, особенно при органических удобрениях.
Качество питьевой воды критично: кипячение 1 минуту или фильтрация через поры <1 мкм удаляют цисты лямблий и ооцисты криптоспоридий.
В эндемичных регионах избегают купания в пресноводных водоёмах (профилактика шистосомоза) и носят обувь на почве (защита от анкилостомидоза и стронгилоидоза). Дегельминтизация домашних животных каждые 3–6 месяцев минимизирует риск зоонозных паразитозов.
Группы повышенного риска
Иммунокомпрометированные пациенты — с онкологией, ВИЧ-инфекцией, на иммуносупрессивной терапии — имеют повышенный риск тяжёлого течения паразитозов. У онкобольных распространённость кишечных паразитарных инфекций достигает 15–30% в зависимости от региона, инфекции протекают атипично и диагностируются с задержкой.
| Группа риска | Основной риск | Профилактическая мера |
|---|---|---|
| Дети дошкольного возраста в коллективах | Острицы, лямблии (тесные контакты) | Регулярные профилактические обследования |
| Путешественники в эндемичные регионы | Множественные паразитозы | Строгая пищевая безопасность, обследование после возврата |
| Работники сельского хозяйства, ветеринары | Почвенные паразиты | Ежегодный скрининг, средства индивидуальной защиты |
| Беременные женщины | Ограничения в лечении | Планирование профилактики с учётом триместра |
Некоторые антигельминтные препараты противопоказаны в первом триместре беременности, поэтому профилактика и лечение согласуются с акушером с учётом потенциальных рисков для плода.

Knowledge Access Protocol
FAQ
Часто задаваемые вопросы
Кишечные паразиты делятся на две основные группы: гельминты (черви) и простейшие (одноклеточные организмы). К гельминтам относятся аскариды, острицы, ленточные черви и сосальщики, а к простейшим — лямблии и амёбы. Согласно исследованиям, эти паразиты по-разному влияют на состав кишечного микробиома (S1).
Паразиты значительно изменяют разнообразие и состав кишечной микробиоты. Исследования показывают корреляцию между присутствием гельминтов и изменением бактериального состава кишечника (S1). Эти изменения могут влиять на пищеварение, иммунитет и общее состояние здоровья.
Типичные симптомы включают хроническую усталость, нарушения пищеварения, анемию и кожные проблемы. Также могут наблюдаться аллергические реакции, снижение иммунитета и дефицит питательных веществ из-за нарушения всасывания. Важно понимать, что эти симптомы неспецифичны и требуют лабораторного подтверждения диагноза.
Нет, паразиты не являются прямой причиной депрессии. Хроническая паразитарная инфекция может способствовать развитию воспаления и влиять на настроение, но депрессия — многофакторное заболевание. Утверждения о паразитах как основной причине психических расстройств не подтверждены научными данными.
Нет, профилактическое лечение без диагностики не рекомендуется в регионах с низкой распространённостью паразитов. Антипаразитарные препараты имеют побочные эффекты и должны назначаться только при подтверждённой инфекции. Регулярные «чистки» без медицинских показаний могут нарушить баланс микробиома и навредить здоровью.
Основной метод — анализ кала на яйца гельминтов и цисты простейших, часто требуется трёхкратное исследование. Дополнительно могут назначаться анализы крови на антитела, соскоб на энтеробиоз и серологические тесты. Выбор методов зависит от клинической картины и предполагаемого типа паразита (S1, S2).
Лечение должно проводиться под контролем врача с использованием специфических антипаразитарных препаратов. Выбор лекарства зависит от типа паразита: для гельминтов используют альбендазол или мебендазол, для простейших — метронидазол. После лечения важно восстановить микробиом с помощью пробиотиков и правильного питания.
Наибольший риск у людей с ослабленным иммунитетом, включая онкологических больных, детей и пожилых. Также в группе риска те, кто путешествует в эндемичные регионы, работает с почвой или животными. Исследования показывают повышенную восприимчивость у пациентов с иммуносупрессией (S2).
Да, некоторые паразиты передаются от животных к человеку (зоонозы). Токсокароз от собак и кошек, эхинококкоз от собак — примеры таких инфекций. Регулярная дегельминтизация питомцев, соблюдение гигиены после контакта с животными и мытьё рук снижают риск заражения.
После антипаразитарной терапии рекомендуется курс пробиотиков с лакто- и бифидобактериями. Важно включить в рацион ферментированные продукты, клетчатку и пребиотики для питания полезной микрофлоры. Восстановление может занять от нескольких недель до месяцев в зависимости от степени нарушения (S1).
Нет, это миф. Паразиты могут способствовать кожным проявлениям через хроническое воспаление и аллергические реакции, но не являются единственной причиной дерматологических заболеваний. Большинство кожных проблем имеют другие причины: генетику, аллергии, аутоиммунные процессы или инфекции.
Ключевые меры — тщательное мытьё рук, термическая обработка мяса и рыбы, мытьё овощей и фруктов. Важно пить только очищенную воду, особенно в путешествиях, и соблюдать санитарные нормы. Эти простые правила значительно снижают риск заражения паразитами.
Да, паразиты конкурируют за питательные вещества и могут нарушать всасывание в кишечнике. Это приводит к дефициту железа, витамина B12, фолиевой кислоты и других нутриентов. Хроническая паразитарная инфекция часто сопровождается анемией и гиповитаминозами, требующими коррекции.
Некоторые паразиты повышают риск определённых видов рака при длительной инфекции. Например, описторхоз связан с холангиокарциномой, а шистосомоз — с раком мочевого пузыря. Онкологические пациенты также более уязвимы к паразитарным инфекциям из-за ослабленного иммунитета (S2).
В регионах с недостаточной очисткой воды это возможно, особенно для простейших (лямблии, криптоспоридии). В городах РФ с современными системами водоподготовки риск минимален, но сохраняется в сельской местности. При сомнениях в качестве воды рекомендуется кипячение или использование фильтров.
Паразиты модулируют иммунный ответ, часто подавляя его для собственного выживания. Это может приводить к хроническому воспалению, изменению баланса Th1/Th2 иммунитета и повышенной восприимчивости к другим инфекциям. Исследования показывают сложное взаимодействие между паразитами, микробиомом и иммунной системой (S1, S2).
