Candida y permeabilidad intestinal aumentada: hechos científicos y mitosλ
Analizamos la conexión entre la microflora fúngica y el deterioro de la barrera intestinal basándonos en evidencia científica y estudios clínicos
Overview
El término "intestino permeable" ha migrado de la medicina alternativa al discurso científico — detrás de él existe un fenómeno medible: el aumento de la permeabilidad intestinal. Candida albicans, residente habitual de la microbiota, puede destruir las uniones estrechas del epitelio 🧬 y provocar inflamación sistémica cuando existe un desequilibrio. Los datos clínicos relacionan esto con estados autoinmunes, trastornos metabólicos y enfermedades inflamatorias intestinales crónicas.
🛡️
Protocolo Laplace: Separamos los hechos científicos establecidos sobre la alteración de la barrera intestinal de las simplificaciones populares, basándonos en investigaciones revisadas por pares y datos clínicos. Es importante comprender la diferencia entre mecanismos probados e hipótesis que requieren mayor estudio.
Reference Protocol
Base Científica
Marco basado en evidencia para análisis crítico
Protocol: Evaluation
Ponte a Prueba
Cuestionarios sobre este tema próximamente
⚡
Más Información
Qué sucede realmente con la barrera intestinal en la permeabilidad aumentada
Definición científica y mecanismos de alteración de la barrera
«Intestino permeable» es un término divulgativo para la permeabilidad intestinal aumentada, una condición en la que las uniones estrechas entre células epiteliales se debilitan y permiten que sustancias del lumen intestinal penetren en el torrente sanguíneo en cantidades aumentadas.
La barrera intestinal es un sistema multinivel: capa de mucosa, células epiteliales, uniones intercelulares estrechas y componentes inmunitarios de la mucosa. Cuando se altera, aumenta el transporte de lipopolisacáridos de bacterias gramnegativas y otras moléculas potencialmente tóxicas a través de la pared intestinal.
| Componente de la barrera | Función | Qué ocurre al alterarse |
|---|---|---|
| Capa de mucosa | Protección física, medio para microbiota | Reducción del grosor, pérdida de protección |
| Células epiteliales | Transporte selectivo, metabolismo | Apoptosis, disfunción, permeabilidad aumentada |
| Uniones estrechas (tight junctions) | Regulación del transporte paracelular | Ruptura de conexiones, paso incontrolado de moléculas |
| Componentes inmunitarios | Reconocimiento de patógenos, tolerancia | Hiperactivación o desregulación |
La permeabilidad aumentada se asocia con enfermedades renales crónicas, problemas cardiovasculares y dermatológicos. No es un diagnóstico independiente, sino un mecanismo fisiopatológico subyacente a múltiples enfermedades.
Papel de las uniones estrechas entre células epiteliales
Las uniones estrechas (tight junctions) son el elemento clave de la función de barrera. Forman una barrera selectiva que regula el transporte paracelular (movimiento de sustancias entre células, no a través de ellas).
- Proteínas transmembrana
- Ocludina, claudinas, JAM — atraviesan la membrana y crean un cierre físico entre células.
- Proteínas citoplasmáticas
- ZO-1, ZO-2, ZO-3 — conectan el complejo con el citoesqueleto, proporcionando resistencia mecánica.
- Alteración estructural
- Cualquier defecto en estas proteínas conduce al aumento de permeabilidad y penetración de moléculas grandes.
Citocinas proinflamatorias, toxinas bacterianas, cambios de pH y estrés oxidativo — todo esto puede alterar la integridad de las uniones estrechas.
Cuando las uniones estrechas se disfuncionan, componentes bacterianos y antígenos alimentarios no digeridos acceden a la capa submucosa, donde interactúan con células inmunitarias. Esto inicia inflamación local y sistémica, creando un círculo vicioso: la inflamación altera aún más la función de barrera.
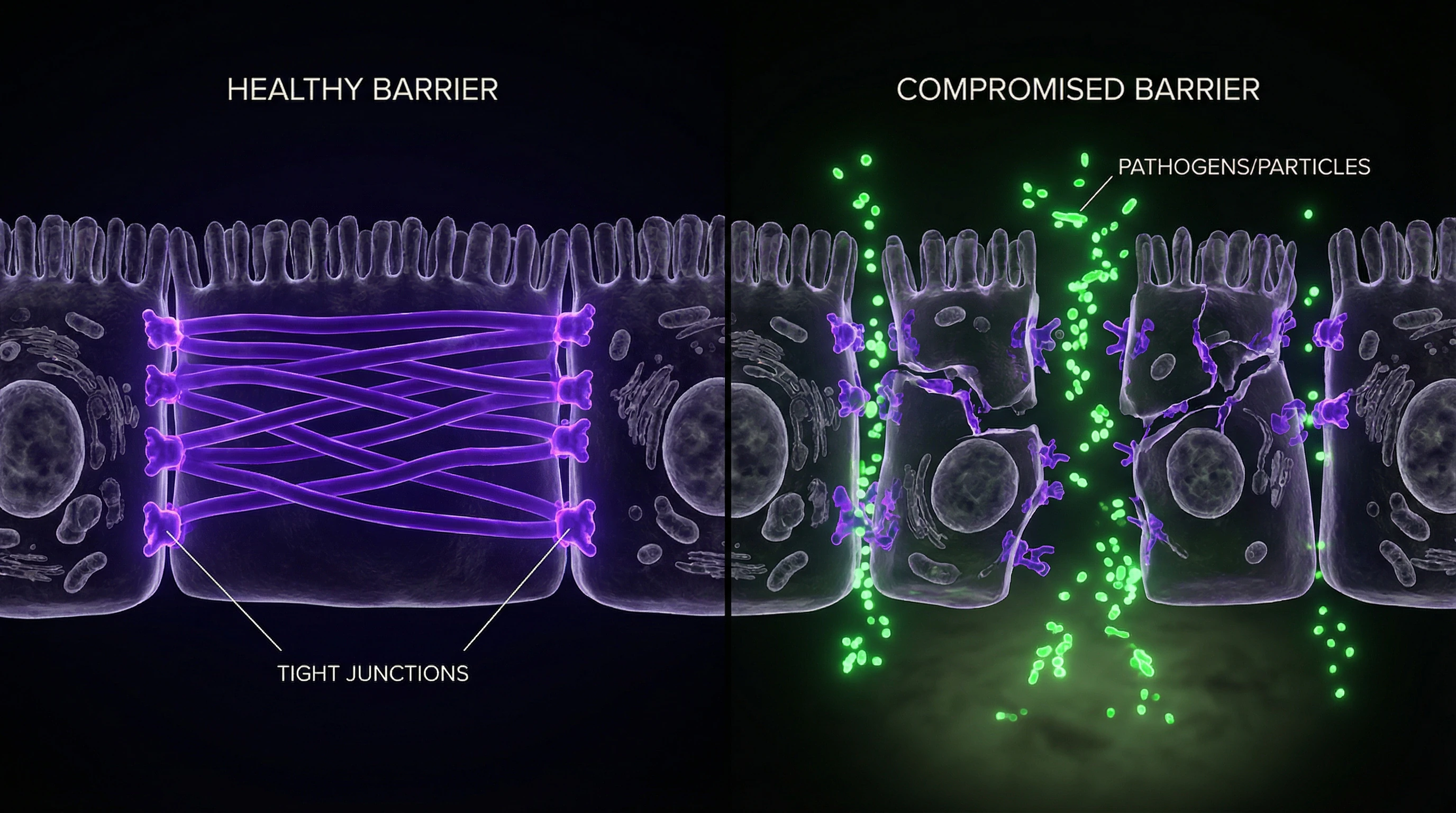
Candida en el intestino: de habitante normal a patógeno
Papel comensal de los hongos en la microbiota
Candida albicans es un habitante natural del intestino, forma parte de la microbiota normal y existe en cantidades equilibradas sin consecuencias patológicas. El ecosistema intestinal se mantiene mediante un equilibrio dinámico entre bacterias, hongos, virus y arqueas.
Candida está controlada por interacciones competitivas con la flora bacteriana y la vigilancia inmunitaria del huésped. En pequeñas cantidades, estos hongos pueden participar en procesos metabólicos y en el entrenamiento del sistema inmunitario.
- pH del medio intestinal
- Disponibilidad de nutrientes
- Producción de péptidos antimicrobianos por el epitelio
- Secreción de inmunoglobulinas
Condiciones para el crecimiento excesivo y transformación en patógeno
La proliferación descontrolada de Candida comienza con la disbiosis, una alteración del equilibrio microbiano. Los antibióticos de amplio espectro destruyen las bacterias competidoras, liberando nichos para microorganismos oportunistas.
Durante el crecimiento excesivo, Candida pasa de la forma levaduriforme a la hifal (micelial), más invasiva y capaz de dañar tejidos.
La disfunción inmunitaria es un factor crítico en el desarrollo de candidiasis. Un sistema inmunitario sano controla eficazmente la población de hongos; su alteración en infección por VIH, uso de corticosteroides, quimioterapia o inmunodeficiencias congénitas crea condiciones para la invasión.
Desencadenantes adicionales: dieta alta en carbohidratos simples (sustrato nutritivo para los hongos), estrés crónico y cambios hormonales. Al crearse condiciones favorables, Candida desencadena una cascada de cambios patológicos que afectan no solo al intestino.
Mecanismos de acción de Candida sobre la permeabilidad de la barrera intestinal
Daño directo al epitelio y uniones estrechas
Candida albicans ataca la barrera intestinal por varios caminos simultáneamente. La forma hifal del hongo penetra físicamente entre las células epiteliales y las invade, alterando mecánicamente la integridad de la monocapa.
Los hongos secretan enzimas proteolíticas (proteasas aspárticas secretadas y fosfolipasas) que destruyen las proteínas de las uniones estrechas, especialmente la ocludina. Resultado: aumenta la permeabilidad paracelular.
- La candidalisina (toxina peptídica citolítica) forma poros en las membranas de las células epiteliales, causando su muerte
- Las adhesinas en la superficie de los hongos (Als3) aseguran la adhesión e inducen endocitosis: los hongos penetran dentro de las células
- Las biopelículas crean un entorno protegido, aumentando la resistencia a factores inmunitarios y antifúngicos
El conjunto de estos mecanismos conduce a una alteración estructural de la barrera y al aumento de la permeabilidad para diversas moléculas.
Papel de la disbiosis y la respuesta inmunitaria en la alteración de la barrera
El crecimiento excesivo de Candida es simultáneamente consecuencia y causa del desequilibrio microbiano. La disbiosis significa reducción de la diversidad de la microbiota, disminución de bacterias beneficiosas (especialmente productoras de ácidos grasos de cadena corta) y crecimiento de microorganismos condicionalmente patógenos.
Los ácidos grasos de cadena corta, principalmente el butirato, proporcionan energía a los colonocitos y regulan la expresión de proteínas de las uniones estrechas. Durante la disbiosis, su producción cae y la barrera se debilita.
La respuesta inmunitaria al crecimiento excesivo de Candida agrava paradójicamente el daño. El reconocimiento de patrones fúngicos (Dectin-1, TLR2, TLR4) activa la producción de citocinas proinflamatorias: TNF-α, IL-1β, IL-6, IL-17.
| Citocina | Mecanismo de daño a la barrera |
|---|---|
| TNF-α, IFN-γ | Alteran directamente la función de las uniones estrechas, aumentando la permeabilidad |
| IL-1β, IL-6, IL-17 | Mantienen la inflamación crónica, intensifican la activación inmunitaria |
La inflamación crónica crea un círculo vicioso: el aumento de permeabilidad permite que más antígenos penetren la barrera, lo que intensifica la activación inmunitaria y el daño adicional.
Las alteraciones de la microbiota intestinal afectan incluso a resultados distantes, como partos prematuros espontáneos, demostrando la importancia sistémica de la barrera intestinal.
Evidencia científica y limitaciones de los estudios sobre la relación entre cándida y permeabilidad intestinal
Qué confirman los estudios clínicos
El aumento de la permeabilidad intestinal es un fenómeno clínico real, documentado en enfermedad renal crónica, enfermedades cardiovasculares y afecciones dermatológicas. Esto indica la importancia sistémica de la función de barrera intestinal.
El papel de la microbiota en la patogénesis de enfermedades ha recibido considerable respaldo científico. El complejo microbio-tisular influye en la variabilidad interindividual de los resultados de salud.
Candida albicans está reconocida como un organismo comensal capaz de volverse patógeno bajo ciertas condiciones, especialmente tras antibioterapia y disfunción inmunitaria.
Los mecanismos de daño a la barrera están estudiados en detalle: factores endógenos y exógenos alteran las uniones estrechas entre células epiteliales, aumentando el transporte de lipopolisacáridos de bacterias gramnegativas al torrente sanguíneo.
| Factor | Mecanismo de acción | Estado de evidencia |
|---|---|---|
| TNF-α, IFN-γ | Alteración directa de proteínas de uniones estrechas | Confirmado |
| Disbiosis de microbiota | Asociación con enfermedades sistémicas | Datos correlacionales |
| Inflamación inducida por Candida | Círculo vicioso de inflamación y permeabilidad | Requiere aclaración |
Áreas que requieren mayor investigación
La evidencia directa de una conexión específica entre candidiasis y síndrome de permeabilidad aumentada permanece limitada. La mayoría de los datos disponibles son correlacionales, no causales.
El término "intestino permeable" se utiliza tanto en contextos científicos como pseudocientíficos, creando confusión terminológica y dificultando la interpretación de estudios.
Las revisiones sistemáticas sobre este tema específico son escasas. Las revisiones narrativas pueden estar sujetas a influencia subjetiva de los autores.
Las vías específicas que conectan la disfunción intestinal con enfermedades sistémicas siguen siendo objeto de investigación activa, especialmente en el contexto de los ejes "intestino-órgano".
La influencia de la microbiota intestinal materna en resultados a largo plazo, como partos prematuros, demuestra la complejidad de las interacciones sistémicas que aún quedan por descifrar completamente.
Se necesitan ensayos controlados aleatorizados para evaluar la eficacia de intervenciones terapéuticas dirigidas a restaurar la barrera en candidiasis.

Factores de riesgo y desencadenantes de la alteración de la barrera intestinal en la candidiasis
Antibióticos e inmunosupresión
La antibioterapia de amplio espectro elimina poblaciones bacterianas competidoras que normalmente limitan la colonización fúngica. Este es uno de los factores de riesgo más significativos del crecimiento excesivo de Candida en el intestino.
Los estados inmunosupresores —infección por VIH, quimioterapia, uso prolongado de corticosteroides, síndromes de inmunodeficiencia— transforman la Candida comensal en forma patógena. La alteración de la inmunidad local de la mucosa (reducción de IgA secretora, disfunción de la respuesta Th17) debilita la protección contra la invasión fúngica.
La combinación de antibioterapia e inmunosupresión crea un efecto sinérgico, aumentando dramáticamente el riesgo de candidiasis sistémica y daño de la barrera.
Dieta y estilo de vida
Una dieta alta en carbohidratos refinados y azúcares es la principal fuente de energía para los hongos. El estrés crónico activa el eje hipotálamo-hipófisis-suprarrenal, eleva el cortisol y altera la composición de la microbiota.
El consumo excesivo de alcohol daña directamente el epitelio intestinal, altera las uniones estrechas y favorece la disbiosis. La ingesta insuficiente de fibra dietética reduce la producción de ácidos grasos de cadena corta, necesarios para la integridad de la barrera epitelial y la regulación de la respuesta inmune.
| Factor de riesgo | Mecanismo de acción | Consecuencia para la barrera |
|---|---|---|
| Antibióticos de amplio espectro | Eliminación de bacterias competidoras | Crecimiento descontrolado de Candida |
| Inmunosupresión | Reducción de IgA local y Th17 | Invasión fúngica del epitelio |
| Dieta alta en carbohidratos | Sustrato energético para hongos | Proliferación de Candida |
| Estrés crónico | Hipercortisolemia, disbiosis | Aumento de la permeabilidad |
| Alcohol | Daño directo del epitelio | Alteración de las uniones estrechas |
| Déficit de fibra dietética | Reducción de ácidos grasos de cadena corta | Debilitamiento de la barrera e inmunidad |
Diagnóstico y enfoques basados en evidencia para la restauración de la barrera intestinal
Métodos clínicos de evaluación
El diagnóstico de la permeabilidad intestinal aumentada sigue siendo un desafío debido a la ausencia de pruebas estandarizadas y criterios diagnósticos claros. Se utilizan tres enfoques principales en la práctica, pero cada uno tiene limitaciones.
| Método | Principio | Estado en clínica |
|---|---|---|
| Lactulosa-manitol | Relación de excreción de azúcares en orina | Investigación; baja disponibilidad |
| Zonulina sérica | Biomarcador de permeabilidad | Especificidad y relevancia controvertidas |
| Microbiología fecal | Evaluación cuantitativa de Candida | Estándar para diagnóstico de candidiasis |
Punto clave: la simple presencia de Candida en heces es normal en personas sanas. El diagnóstico requiere evaluación cuantitativa de la carga fúngica, no solo detección.
Estrategias basadas en evidencia para la restauración de la barrera
La terapia antifúngica con fluconazol o nistatina está indicada solo ante sobrecrecimiento documentado de Candida y bajo supervisión médica. La prescripción sin confirmación microbiológica es un error de razonamiento diagnóstico.
Las cepas probióticas Lactobacillus rhamnosus GG y Saccharomyces boulardii compiten con Candida y apoyan la función de barrera, pero la eficacia depende de la cepa y la dosis. No es una solución universal.
Las intervenciones dietéticas —limitación de carbohidratos refinados y aumento de fibra alimentaria— modulan la microbiota y mejoran la salud metabólica intestinal. Este es el nivel básico que debe ser el primer paso.
La glutamina, el butirato y los nutrientes que apoyan el metabolismo energético de los enterocitos muestran potencial en la restauración de la integridad epitelial, pero requieren más estudios clínicos para determinar protocolos óptimos.
Protocolo integral y riesgos de la automedicación
La restauración de la barrera intestinal requiere eliminar factores desencadenantes: uso injustificado de antibióticos, corrección del estado inmunitario, modificación del estilo de vida. Es un enfoque sistémico, no una intervención puntual.
El autodiagnóstico y la automedicación sin supervisión médica conllevan riesgos reales. Los síntomas atribuidos al "intestino permeable" y la candidiasis pueden enmascarar enfermedades graves que requieren terapia específica.
La individualización de los protocolos terapéuticos basada en el cuadro clínico, datos de laboratorio y factores de riesgo es clave para la restauración efectiva de la función de barrera. No existen esquemas universales.
Knowledge Access Protocol
FAQ
Preguntas Frecuentes
Es el nombre popular de la permeabilidad intestinal aumentada, cuando se alteran las uniones estrechas entre las células del intestino. Como resultado, sustancias que normalmente no deberían pasar al torrente sanguíneo atraviesan la pared intestinal: toxinas bacterianas, partículas de alimentos no digeridos. El término científico es alteración de la integridad estructural y funcional de la barrera intestinal.
El crecimiento excesivo de Candida puede contribuir a la alteración de la barrera intestinal, pero no es la única causa. En la disbiosis, los hongos liberan toxinas y enzimas que dañan el epitelio intestinal. Sin embargo, la relación causal directa requiere más investigación: es un proceso multifactorial.
No hay síntomas específicos: las manifestaciones son inespecíficas e incluyen hinchazón, alteraciones del tránsito intestinal, intolerancias alimentarias, fatiga crónica. Pueden aparecer problemas cutáneos, reacciones alérgicas, procesos inflamatorios en diferentes órganos. El diagnóstico lo establece únicamente un médico mediante evaluación integral, no por síntomas aislados.
Sí, los antibióticos destruyen no solo bacterias patógenas sino también beneficiosas, creando condiciones para el crecimiento de hongos. Candida es resistente a los antibacterianos y ocupa el nicho ecológico liberado. El riesgo es especialmente alto con tratamientos prolongados o repetidos sin apoyo probiótico.
La dieta es un componente importante, pero no el único, para restaurar la barrera intestinal. Eliminar alimentos desencadenantes (azúcar, alcohol, carbohidratos refinados) y añadir nutrientes antiinflamatorios ayuda, pero se requiere un enfoque integral. Es necesario trabajar las causas: estrés, infecciones, medicamentos, bajo supervisión de un especialista.
En la práctica clínica se utilizan pruebas de zonulina (marcador de permeabilidad), lipopolisacáridos (LPS), anticuerpos contra componentes de la pared intestinal. También se emplea el test de lactulosa-manitol y evaluación de calprotectina. Sin embargo, aún no existen protocolos diagnósticos estandarizados: la interpretación de resultados requiere experiencia médica.
No, Candida está presente en el intestino de la mayoría de personas sanas como parte de la microbiota normal. Los problemas surgen solo con crecimiento excesivo en contexto de inmunidad debilitada, disbiosis u otros factores. Ser portador de hongos no equivale a enfermedad: lo importante es el equilibrio de microorganismos.
Los probióticos pueden apoyar la restauración de la microbiota y competir con Candida por recursos, pero no son un tratamiento independiente. La eficacia depende de las cepas, dosis y características individuales. Los mejores resultados se logran combinándolos con dieta, eliminación de desencadenantes y, si es necesario, terapia antifúngica.
Sí, el estrés crónico aumenta directamente la permeabilidad intestinal a través del eje cerebro-intestino. Las hormonas del estrés (cortisol) alteran las uniones estrechas entre células epiteliales y modifican la composición de la microbiota. Esto crea un círculo vicioso: el estrés deteriora la barrera, y la barrera alterada intensifica la inflamación y la respuesta al estrés.
Sí, Candida utiliza carbohidratos simples (azúcar, harina blanca) como fuente principal de energía para crecer. Una dieta alta en carbohidratos crea un ambiente favorable para la multiplicación de hongos. Sin embargo, no es necesario eliminar completamente los carbohidratos: lo importante es el equilibrio y la calidad (preferir complejos, con fibra).
Los estudios muestran una asociación entre el aumento de la permeabilidad intestinal y algunas condiciones autoinmunes, pero la relación causal no está definitivamente demostrada. Una barrera comprometida puede permitir el paso de antígenos que desencadenan respuestas inmunitarias. Sin embargo, no está claro qué es primario: la permeabilidad o el proceso autoinmune; esta es un área de investigación activa.
No, el autodiagnóstico no es fiable: los síntomas de la candidiasis son inespecíficos y coinciden con numerosas otras condiciones. Las «pruebas caseras» populares (como la del vaso de agua) carecen de fundamento científico. El diagnóstico requiere análisis de laboratorio (cultivo de heces, PCR) y evaluación del cuadro clínico por un gastroenterólogo o especialista en enfermedades infecciosas.
Son beneficiosos los alimentos ricos en glutamina (caldo de huesos, carne), omega-3 (pescado graso), polifenoles (frutos rojos, verduras de hoja verde), zinc (semillas de calabaza). Los alimentos fermentados (chucrut, kéfir) apoyan la microbiota. Es importante la fibra de las verduras para alimentar las bacterias beneficiosas que producen ácidos grasos de cadena corta, fortaleciendo la barrera.
Los plazos son individuales y dependen del grado de daño, las causas y el cumplimiento de las recomendaciones: desde varias semanas hasta varios meses. El epitelio intestinal se renueva cada 3-5 días, pero la restauración de la función de barrera y la microbiota requiere más tiempo. Es fundamental la constancia: eliminar desencadenantes, dieta antiinflamatoria, apoyo a la microbiota.
Sí, los antifúngicos sistémicos pueden alterar el equilibrio de la microbiota, aunque en menor medida que los antibióticos. Actúan no solo sobre hongos patógenos, sino también sobre microorganismos comensales. Por ello se prescriben estrictamente según indicación médica, en ciclos, con apoyo probiótico simultáneo y bajo supervisión facultativa.
Las investigaciones muestran una posible conexión a través del eje intestino-cerebro: la disbiosis y la inflamación pueden influir en los neurotransmisores y el estado de ánimo. Las toxinas de Candida teóricamente podrían afectar al SNC cuando hay permeabilidad aumentada. Sin embargo, las pruebas directas son limitadas: es una línea de investigación prometedora que requiere interpretación cautelosa.
