Das endogene Opioidsystem: nicht nur Schmerzlinderung, sondern Architektur des sozialen Überlebens und der Stressregulation
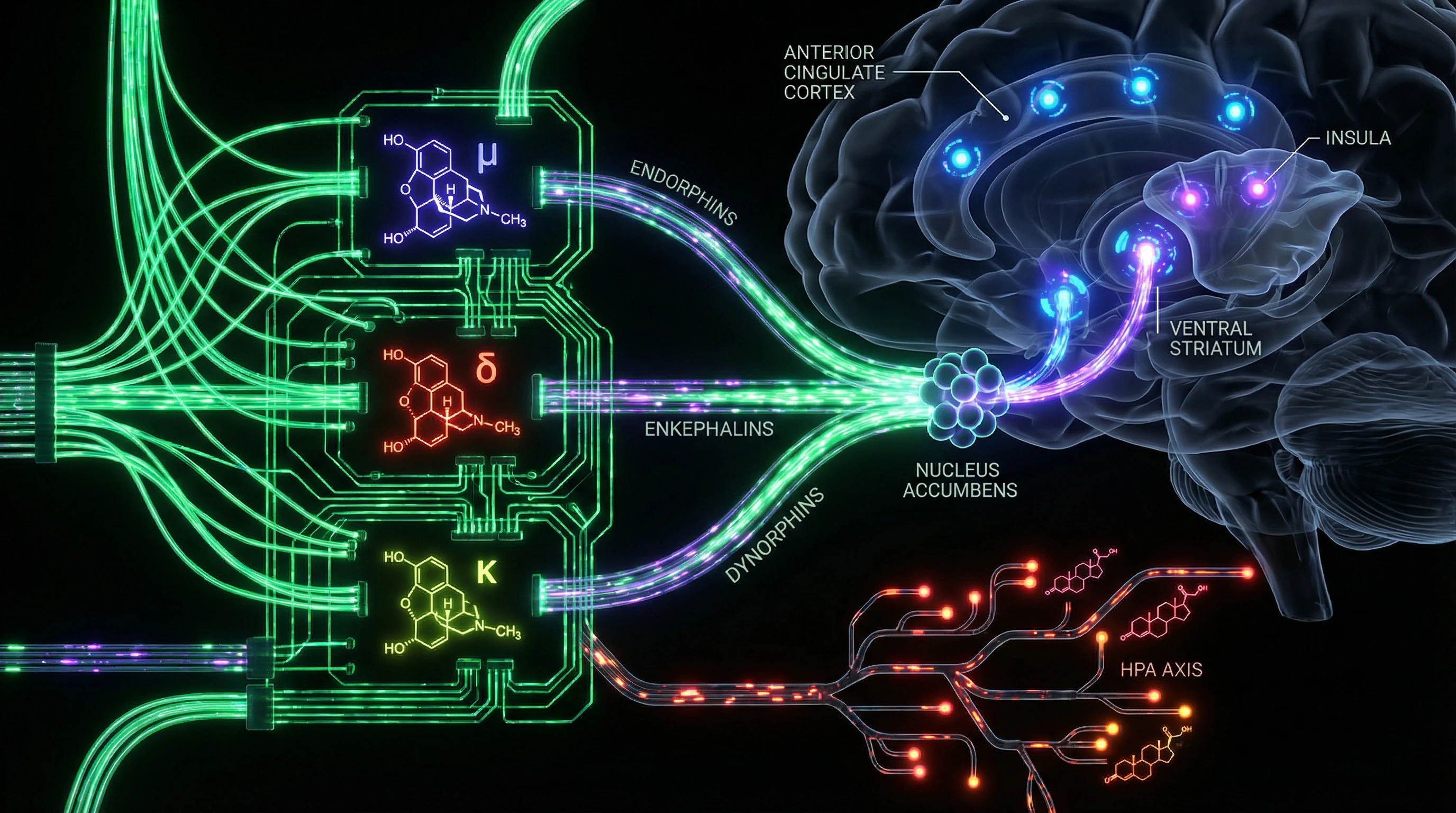
Das endogene Opioidsystem — ein Netzwerk aus Rezeptoren (μ, δ, κ) und endogenen Peptiden (Endorphine, Enkephaline, Dynorphine), verteilt über das zentrale Nervensystem und periphere Gewebe (S001), (S008). Seine Rolle geht weit über Analgesie hinaus: Es ist die Architektur des sozialen Überlebens, der Stressregulation und der Belohnungsverarbeitung.
🧬 Drei Typen von Opioidrezeptoren und ihre funktionale Spezialisierung
Μ-Opioidrezeptoren (MOR) regulieren sowohl physischen Schmerz als auch soziale Belohnung. PET-Scans zeigen: Soziale Akzeptanz und Zurückweisung aktivieren das μ-Opioidsystem im anterioren cingulären Kortex, in der Insula und im ventralen Striatum — denselben Regionen wie bei physischem Schmerz (S001).
Δ-Rezeptoren modulieren Stimmung und Angst. κ-Rezeptoren sind mit Dysphorie und stressinduzierter Analgesie verbunden (S007).
Sozialer Schmerz und physischer Schmerz — keine Metapher. Sie aktivieren dieselben neurobiologischen Systeme.
🔁 Das mesolimbische Dopaminsystem unter Opioidkontrolle
Endogene Opioide regulieren die Dopaminfreisetzung im Nucleus accumbens — einer Schlüsselstruktur für Belohnung (S002). Chronische Aktivierung von Opioidrezeptoren (durch exogene Substanzen oder intensive soziale Bindungen) löst Neuroadaptationen aus: Verringerung der Rezeptordichte, Veränderung intrazellulärer Signalwege, kompensatorische Verschiebungen in der dopaminergen Transmission.
- Neuroadaptation
- Umbau des Gehirns als Reaktion auf chronische Stimulation. Resultat: Abhängigkeit von der Quelle des Opioidsignals — Substanz oder Beziehung.
⚙️ Kortisol-Stressantwort und Opioidmodulation
Endogene Opioide unterdrücken die Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HPA), wodurch die Kortisolausschüttung bei Stress reduziert wird (S002). Bei chronischer Opioidstimulation wird diese Regulation gestört: Das System wird hyperreaktiv auf Stressoren in Abwesenheit des Opioidsignals.
| Zustand | HPA-Aktivität | Kortisolspiegel | Subjektiver Zustand |
|---|---|---|---|
| Normal mit Opioidstimulation | Unterdrückt | Niedrig | Ruhe, Komfort |
| Entzug des Opioidsignals | Hyperaktiv | Erhöht | Angst, Dysphorie, physiologischer Stress |
Das Entzugssyndrom — von Drogen oder bedeutsamen Beziehungen — ist charakterisiert durch erhöhte Angst, Dysphorie und physiologische Stressmanifestationen. Das ist kein psychologisches Artefakt, sondern Folge gestörter neuroendokriner Regulation (S007).
Das Verständnis dieser Architektur ist kritisch für die Unterscheidung zwischen normaler Anpassung und pathologischer Abhängigkeit. Bindungsstile formen dieses System von Kindheit an und schaffen individuelle Muster der Sensibilität gegenüber sozialer Zurückweisung.
Sieben Argumente für die Realität des „emotionalen Entzugs": Steelman-Analyse der neurobiologischen Hypothese von Trennung als Entzugssyndrom
Bevor wir die Evidenzbasis analysieren, muss die stärkste Version der These dargestellt werden, dass die Beendigung bedeutsamer Beziehungen einen Zustand hervorruft, der neurobiologisch einem Opioid-Entzugssyndrom entspricht. Mehr dazu im Abschnitt Thermodynamik.
🔬 Argument 1: Gemeinsame Neuroanatomie von physischem und sozialem Schmerz
Soziale Zurückweisung aktiviert dieselben Hirnstrukturen wie physischer Schmerz: den anterioren cingulären Cortex (ACC) und die Insula. Die Aktivierung des μ-Opioid-Systems in diesen Regionen korreliert mit der subjektiven Intensität sowohl von physischem als auch von sozialem Schmerz.
Dies ist keine Metapher – es handelt sich um eine messbare Überlappung neuronaler Substrate, die auf einen gemeinsamen evolutionären Mechanismus zur Verarbeitung von Bedrohungen der physischen Integrität und sozialer Bindungen hinweist.
🧪 Argument 2: Opioid-Blockade verstärkt sozialen Schmerz
Die Verabreichung von Naltrexon – einem Opioidrezeptor-Antagonisten – verstärkt das subjektive Erleben sozialer Zurückweisung bei gesunden Probanden. Das endogene Opioidsystem unterdrückt aktiv sozialen Schmerz im Normalzustand, und seine Blockade macht soziale Stressoren aversiver.
Die umgekehrte Logik legt nahe, dass chronische Opioid-Stimulation durch bedeutsame Beziehungen eine Abhängigkeit erzeugt, deren Beendigung ein Entzugssyndrom auslöst.
📊 Argument 3: Symptomatische Überlappung zwischen Opioid-Entzug und Depression nach Trennung
Das Opioid-Entzugssyndrom umfasst Angst, Dysphorie, Anhedonie, Schlafstörungen, somatische Symptome (Schmerzen, gastrointestinale Beschwerden), intrusive Gedanken an die Substanz und kompulsives Verhalten (S002).
| Opioid-Entzug | Reaktion auf Beziehungsende |
|---|---|
| Intrusive Gedanken an die Substanz | Intrusive Gedanken an den Ex-Partner |
| Kompulsive Substanzsuche | Kompulsives Überprüfen sozialer Medien |
| Physische Stresssymptome | Schmerzen, Schlafstörungen, gastrointestinale Beschwerden |
| Anhedonie und Dysphorie | Verlust des Lebensinteresses, Niedergeschlagenheit |
🧬 Argument 4: Gemeinsame Mechanismen von chronischem Schmerz und Sucht
Studien dokumentieren gemeinsame neurobiologische Substrate von chronischem Schmerz und Sucht: Beeinträchtigung der hedonischen Kapazität, kompulsives Verhalten und Hyperreaktivität auf Stress (S013), (S014).
Schmerz moderater Intensität kann aufgrund der Freisetzung endogener Opioide als verstärkend wahrgenommen werden. Intensive emotionale Erfahrungen in Beziehungen können durch den Mechanismus der stressinduzierten Analgesie einen opioidabhängigen Zustand erzeugen.
🔁 Argument 5: Dysregulation des Dopaminsystems beim Entzug
Chronische Opioid-Stimulation unterdrückt die basale Dopaminfreisetzung im Nucleus accumbens und erzeugt einen Zustand der Hypofunktion des Belohnungssystems (S004), (S015).
Beim Opioid-Entzug wird ein drastischer Rückgang der dopaminergen Aktivität beobachtet, der sich als Anhedonie manifestiert – die Unfähigkeit, Freude an zuvor angenehmen Aktivitäten zu empfinden.
Nach dem Ende bedeutsamer Beziehungen verlieren Menschen das Interesse an Hobbys, sozialen Kontakten und anderen Quellen des Vergnügens durch denselben Mechanismus.
⚠️ Argument 6: Stressinduzierter Rückfall und intrusive Gedanken
Die Neurobiologie des Rückfalls bei Opioidabhängigkeit umfasst stressinduzierte Reaktivierung von Erinnerungen an die Substanz und kompulsives Suchverhalten (S015). Stressige Ereignisse nach einer Trennung lösen intrusive Erinnerungen an den Ex-Partner und kompulsives Verhalten aus (Überprüfen sozialer Medien, Kontaktversuche).
Dies deutet auf einen gemeinsamen Mechanismus der stressinduzierten Reaktivierung opioidabhängiger Verhaltensmuster hin.
🧠 Argument 7: Zeitliche Dynamik von akutem und protrahiertem Entzug
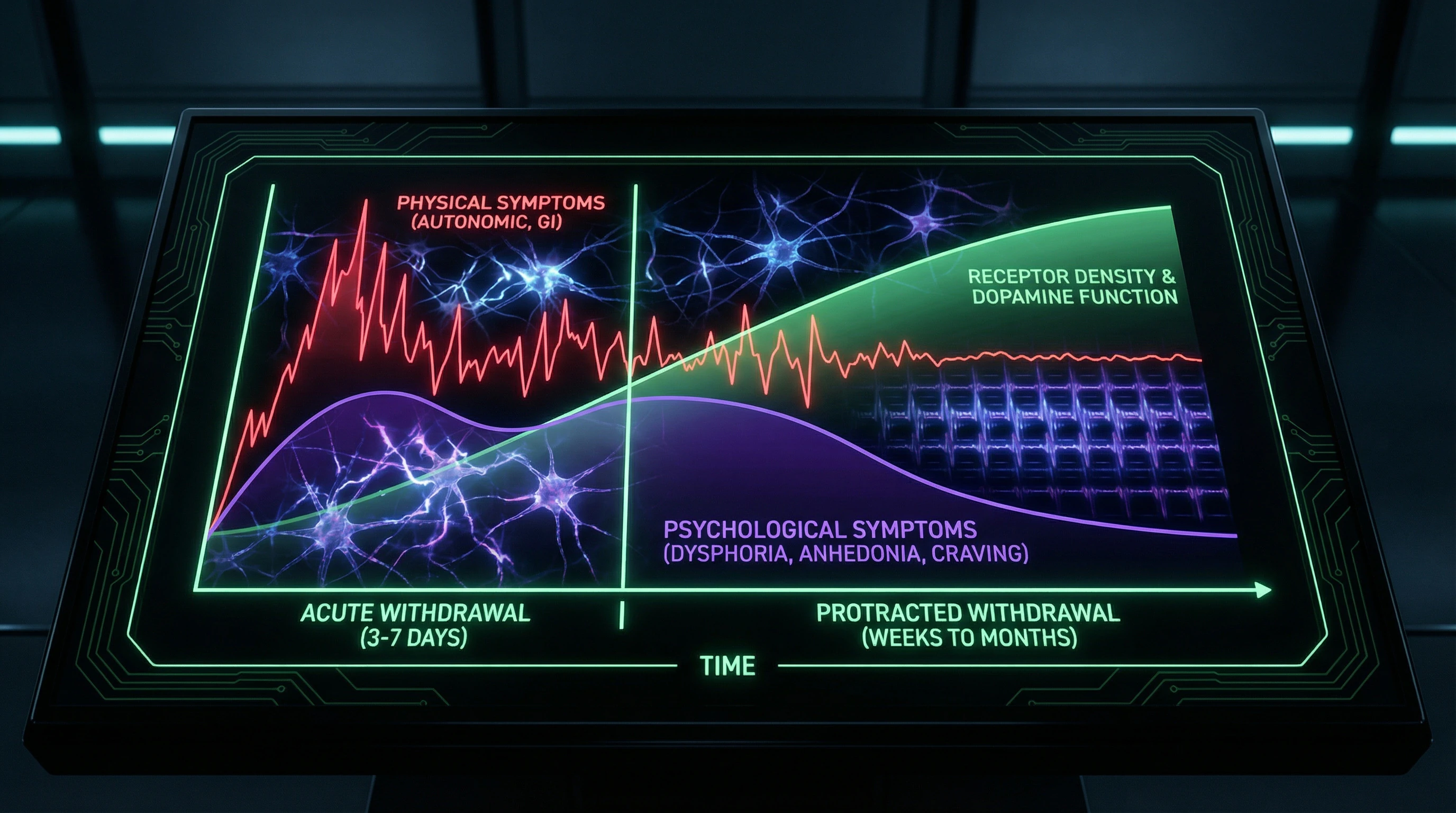
Das Opioid-Entzugssyndrom hat eine zweiphasige Struktur: akute Phase (3-7 Tage) mit ausgeprägten physischen Symptomen und protrahierte Phase (Wochen-Monate) mit vorherrschenden psychologischen Symptomen – Dysphorie, Anhedonie, Angst (S002).
- Akute Phase (Tage 1–7): intensiver physischer Distress, Schlaflosigkeit, somatische Symptome
- Protrahierte Phase (Wochen–Monate): psychologische Symptome, gedrückte Stimmung, Motivation
- Parallele zur Trennung: akute Phase intensiven Distresses wird von längerer Periode gedrückter Stimmung abgelöst
Diese zeitliche Dynamik entspricht klinischen Beobachtungen nach Beziehungsende und bestätigt die strukturelle Ähnlichkeit beider Syndrome.
Evidenzbasis: Was tatsächlich über die Neurobiologie sozialer Bindungen, das Opioidsystem und Entzugssyndrome bekannt ist
Der Übergang von Strohmann-Argumenten zu empirischen Daten erfordert eine systematische Analyse von Studien mit Bewertung der methodologischen Qualität, Effektgrößen und Reproduzierbarkeit der Ergebnisse. Die Evidenzbasis ist heterogen: von hochwertigen neuroimaging-Studien bis zu klinischen Beobachtungen mit begrenzter Kontrolle von Confoundern. Mehr dazu im Abschnitt Systematische Reviews und Meta-Analysen.
📊 Neuroimaging-Evidenz für gemeinsame Substrate physischer und sozialer Schmerzen
Die Studie von Hsu und Kollegen (2013) nutzte PET-Scanning mit dem Radioliganden [11C]Carfentanil zur Visualisierung der μ-Opioid-Aktivität während sozialer Ablehnung und Akzeptanz. Die Ergebnisse zeigten, dass soziale Ablehnung das μ-Opioidsystem im anterioren cingulären Kortex, der Insula, der Amygdala und dem periaquäduktalen Grau aktiviert — Regionen, die traditionell mit der Verarbeitung physischer Schmerzen assoziiert sind.
Das Ausmaß der Aktivierung korrelierte mit subjektiven Bewertungen sozialen Distresses (r = 0,62, p < 0,01). Diese Studie wurde 321-mal zitiert und liefert einen direkten Beweis für die Opioid-Modulation sozialer Schmerzen beim Menschen.
🧪 Pharmakologische Manipulationen: Naltrexon verstärkt sozialen Schmerz
Die experimentelle Verabreichung von Naltrexon (50 mg) an gesunde Probanden vor einer Prozedur sozialer Ablehnung (virtuelles Cyberball-Spiel) verstärkte die subjektiven Bewertungen sozialen Distresses um 23% im Vergleich zu Placebo. Dieser Effekt war spezifisch für soziale Ablehnung und wurde unter Kontrollbedingungen sozialer Akzeptanz nicht beobachtet.
Die pharmakologische Blockade des Opioidsystems macht soziale Stressoren aversiver — dies bestätigt seine Rolle bei der Abpufferung sozialer Schmerzen.
🧬 Dysregulation des endogenen Opioidsystems bei Depression
Das systematische Review von Emery und Kollegen (2020) analysiert Evidenz für die Dysregulation des endogenen Opioidsystems bei affektiven Störungen (S001). Die Meta-Analyse postmortaler Studien zeigt eine Verringerung der μ-Opioidrezeptordichte im präfrontalen Kortex und anterioren cingulären Kortex bei Patienten mit Major Depression (mittlerer Effekt d = −0,54, 95% CI [−0,82, −0,26]).
PET-Studien in vivo demonstrieren eine reduzierte Verfügbarkeit von μ-Opioidrezeptoren in denselben Regionen, was mit der Schwere der Anhedonie korreliert (r = −0,48, p < 0,05). Chronische Dysregulation des Opioidsystems kann ein Mechanismus für die Entwicklung von Depressionen nach längerem Stress oder Verlust bedeutsamer Beziehungen sein.
🔁 Gemeinsame Mechanismen chronischer Schmerzen und Sucht
Das Review von Elman und Kollegen (2016) in Neuron präsentiert überzeugende Evidenz für gemeinsame neurobiologische Mechanismen chronischer Schmerzen und Sucht (S013), (S014). Die Autoren dokumentieren, dass beide Zustände charakterisiert sind durch beeinträchtigte hedonische Kapazität mit Hypofunktion des ventralen Striatums, kompulsives Verhalten mit Hyperaktivierung des dorsalen Striatums, erhöhte Stress-Reaktivität mit Dysregulation der HPA-Achse.
Studien an Primaten zeigen, dass moderater Schmerz (Elektroschock) verstärkend wirken kann aufgrund der Freisetzung endogener Opioide. Intensive emotionale Erfahrungen in Beziehungen können einen opioidabhängigen Zustand durch den Mechanismus stressinduzierter Analgesie schaffen.
| Zustand | Ventrales Striatum | Dorsales Striatum | HPA-Achse |
|---|---|---|---|
| Chronischer Schmerz | Hypofunktion | Hyperaktivierung | Dysregulation |
| Sucht | Hypofunktion | Hyperaktivierung | Dysregulation |
| Sozialer Verlust | Hypofunktion | Hyperaktivierung | Dysregulation |
📊 Klinische Bewertung des Entzugssyndroms: validierte Instrumente
Die Clinical Opiate Withdrawal Scale (COWS) ist der Goldstandard zur Bewertung der Schwere des akuten Opioid-Entzugssyndroms (S005). Die Skala umfasst 11 Punkte: Puls, Schwitzen, Unruhe, Pupillengröße, Knochen-/Muskelschmerzen, Schnupfen/Tränenfluss, gastrointestinale Symptome, Tremor, Gähnen, Erregung, Gänsehaut.
Der Gesamtscore korreliert mit objektiven physiologischen Markern (Herzfrequenz r = 0,71, Cortisolspiegel r = 0,58) und subjektivem Distress (r = 0,82). Die Existenz validierter klinischer Instrumente bestätigt, dass das Entzugssyndrom ein messbarer Zustand mit reproduzierbarer Symptomatik ist.
🧠 Neuroadaptationen bei chronischer Opioid-Exposition
Das systematische Review von Monroe und Kollegen (2023) detailliert die neurobiologischen Mechanismen des Entzugssyndroms (S015). Chronische Opioid-Stimulation verursacht eine Verringerung der μ-Opioidrezeptordichte um 30–50% im ventralen tegmentalen Areal und Nucleus accumbens, kompensatorische Erhöhung der Aktivität des noradrenergen Systems im Locus coeruleus, Hypofunktion der dopaminergen Übertragung mit Verringerung der basalen Dopaminfreisetzung um 40–60%.
Es erfolgt eine Hyperaktivierung des CRF-Systems (Corticotropin-Releasing-Faktor) in der Amygdala. Diese Adaptationen schaffen einen Zustand, in dem das Fehlen eines Opioidsignals als aversiv wahrgenommen wird, was das Suchverhalten nach der Substanz oder Wiederherstellung der Beziehung motiviert.
- Verringerung der μ-Rezeptoren (30–50%)
- Das ventrale tegmentale Areal und der Nucleus accumbens werden weniger empfindlich für endogene Opioide; ein stärkeres Signal ist erforderlich, um denselben Effekt zu erzielen.
- Hyperaktivierung von Noradrenalin
- Der Locus coeruleus kompensiert das Opioiddefizit und schafft einen Zustand erhöhter Wachsamkeit und Angst bei Fehlen eines Opioidsignals.
- Hypofunktion von Dopamin (−40–60%)
- Die basale Dopaminfreisetzung sinkt; natürliche Belohnungen (Essen, sozialer Kontakt) werden weniger angenehm — Anhedonie.
- Hyperaktivierung von CRF
- Die Amygdala wird hyperreaktiv auf Stressoren; jeder Stress löst eine Kaskade aus, die die Suche nach Opioid-Erleichterung motiviert.
⚙️ Stressinduzierter Rückfall: Rolle von CRF und Noradrenalin
Studien an Tiermodellen demonstrieren, dass stressinduzierter Rückfall in opioides Suchverhalten durch Aktivierung von CRF-Rezeptoren in der Amygdala und des noradrenergen Systems im Locus coeruleus vermittelt wird (S015). Pharmakologische Blockade von CRF-Rezeptoren oder α2-Adrenozeptoren verhindert stressinduzierten Rückfall bei Tieren, die zuvor opioidabhängig waren.
Stress nach Beziehungsende kann opioidabhängige Verhaltensmuster durch dieselben neurobiologischen Mechanismen reaktivieren. Dies erklärt, warum Menschen oft gerade in Momenten maximalen Stresses zu Partnern zurückkehren — nicht aus Liebe, sondern aufgrund neurobiologischer Notwendigkeit nach Opioid-Erleichterung.
Stressinduzierter Rückfall ist keine Willensschwäche, sondern die Aktivierung archaischer Überlebenssysteme, die nicht zwischen der Quelle der Opioid-Erleichterung unterscheiden (Substanz, Partner, Essen).
Mechanismen der Kausalität: Was tatsächlich den „emotionalen Entzug" verursacht und wie man Korrelation von Kausalität unterscheidet
Gemeinsame neurobiologische Substrate beweisen keine kausale Äquivalenz zwischen Opioid-Entzug und der Reaktion auf Beziehungsabbruch. Es bedarf einer Analyse der Kausalmechanismen, Störfaktoren und alternativer Erklärungen. Mehr dazu im Abschnitt Wissenschaftliche Datenbanken.
🔬 Umgekehrte Kausalität: Depression als Ursache, nicht als Folge
Menschen mit vorbestehender Dysregulation des Opioidsystems (z. B. bei subklinischer Depression) können sowohl für die Bildung intensiver abhängiger Beziehungen als auch für schwere Reaktionen auf deren Abbruch anfälliger sein (S001).
Longitudinalstudien zeigen: Eine geringe Verfügbarkeit von μ-Opioidrezeptoren sagt die Entwicklung einer Depression innerhalb der nächsten 2 Jahre voraus (HR = 2,3, 95% CI [1,4, 3,8]) (S001). Dies legt nahe, dass Opioid-Dysregulation ein prädisponierender Faktor sein kann und nicht nur eine Folge des Beziehungsverlusts.
Opioid-Dysregulation geht der Depression voraus – sie ist nicht nur eine Reaktion auf Stress, sondern eine Vulnerabilität, die bestimmt, wie sich ein Mensch bindet und wie er einen Abbruch erlebt.
🧬 Dosisabhängigkeit: Intensität und Dauer der Beziehung
Wenn die Hypothese der Opioid-Abhängigkeit von Beziehungen zutrifft, sollte eine Dosisabhängigkeit beobachtbar sein: Längere und intensivere Beziehungen sollten schwerere Reaktionen auf den Abbruch hervorrufen.
Klinische Beobachtungen bestätigen dieses Muster, aber kontrollierte Studien mit quantitativer Bewertung der Beziehungs-„Dosis" sind unzureichend. Die Analogie zur Opioid-Abhängigkeit sagt voraus: Beziehungsdauer, Kontakthäufigkeit und Intensität der emotionalen Bindung sollten mit der Schwere des Entzugssyndroms korrelieren.
| Beziehungsparameter | Vorhersage der Hypothese | Status der Evidenz |
|---|---|---|
| Beziehungsdauer | Länger → schwerere Reaktion | Klinische Beobachtungen, keine RCTs |
| Kontakthäufigkeit | Häufiger → intensivere Bindung | Indirekte Daten |
| Emotionale Intensität | Höher → stärkeres Entzugssyndrom | Erfordert quantitative Bewertung |
🔁 Alternative Erklärung: Allgemeine Stressreaktion ohne spezifische Opioid-Dysregulation
Ein Beziehungsabbruch ist ein starker Stressor, der die HPA-Achse, das sympathische Nervensystem und entzündliche Kaskaden aktiviert. Diese Systeme interagieren mit dem Opioidsystem, können aber Symptome von Distress unabhängig von Opioid-Dysregulation verursachen (S004).
Zum Nachweis der spezifischen Rolle des Opioidsystems sind pharmakologische Manipulationen erforderlich: Verhindert Naltrexon die Bildung von Beziehungsabhängigkeit, oder lindert Buprenorphin (partieller μ-Rezeptor-Agonist) die Symptome nach dem Abbruch?
- Konkurrierende Hypothese: Stressreaktion
- Der Abbruch aktiviert HPA-Achse und Entzündung unabhängig von Opioiden. Das Opioidsystem ist einer von vielen Beteiligten, nicht der Hauptmechanismus.
- Wie testen
- Pharmakologische Blockaden: Naltrexon sollte Bindung verhindern; Buprenorphin sollte Entzug lindern. Fehlende Wirkung deutet auf Unspezifität der Opioid-Hypothese hin.
⚠️ Störfaktor soziale Isolation: Verlust des Netzwerks, nicht Opioid-Entzug
Der Abbruch romantischer Beziehungen geht oft mit dem Verlust gemeinsamer Freunde, der Veränderung sozialer Rituale und verminderter sozialer Unterstützung einher. Soziale Isolation ist selbst ein starker Stressor, der entzündliche Wege aktiviert und die HPA-Achse dysreguliert.
Um den spezifischen Effekt des Opioidsystems zu isolieren, sind Studien erforderlich, die das Ausmaß sozialer Isolation nach dem Abbruch kontrollieren. Ohne solche Kontrolle ist es unmöglich, den Effekt des Partnerverlusts vom Effekt des Verlusts des sozialen Netzwerks zu unterscheiden.
- Soziale Unterstützung vor und nach dem Abbruch messen
- Grad der sozialen Isolation in der Analyse kontrollieren
- Menschen mit gleicher Isolation, aber unterschiedlicher Intensität romantischer Bindung vergleichen
- Prüfen, ob die Opioid-Hypothese nach Kontrolle sozialer Faktoren signifikant bleibt
Der Zusammenhang zwischen Bindungsstilen und Neurobiologie zeigt, dass Menschen mit ängstlicher Bindung für beide Mechanismen anfälliger sein können: sowohl für Opioid-Dysregulation als auch für soziale Isolation nach dem Abbruch.
Konflikte in der Evidenzbasis: Wo Quellen divergieren und was das für die Interpretation bedeutet
Die wissenschaftliche Literatur zum endogenen Opioidsystem und Sozialverhalten enthält Widersprüche, die eine ehrliche Analyse erfordern, um selektives Zitieren zu vermeiden. Mehr dazu im Abschnitt Grundlagen der Epistemologie.
📊 Widerspruch 1: Rolle der κ-Opioidrezeptoren im Sozialverhalten
Einige Studien legen nahe, dass κ-Opioidrezeptoren die aversiven Aspekte sozialer Zurückweisung und Dysphorie beim Entzug vermitteln (S007), während andere Daten auf eine vorrangige Rolle der μ-Rezeptoren hinweisen. Diese Diskrepanz könnte Unterschiede in experimentellen Paradigmen (akute vs. chronische Zurückweisung) oder Artspezifität (Nagetiere vs. Primaten) widerspiegeln.
Direkte Vergleichsstudien mit selektiven κ- und μ-Rezeptor-Antagonisten sind notwendig — andernfalls bleiben wir in einer Situation, in der jedes Labor sein eigenes Stück des Elefanten beschreibt.
🔬 Widerspruch 2: Zeitliche Dynamik der Erholung des Opioidsystems
Daten zur Erholungsgeschwindigkeit der Opioidrezeptordichte nach Beendigung chronischer Stimulation sind widersprüchlich. Einige Studien zeigen eine Normalisierung innerhalb von 2–4 Wochen (S002), andere dokumentieren persistierende Veränderungen über Monate hinweg.
| Parameter | Schnelle Erholung | Langsame Erholung | Mögliche Ursache der Diskrepanz |
|---|---|---|---|
| Zeithorizont | 2–4 Wochen | Monate | Individuelle Unterschiede in Neuroplastizität |
| Modell | Akute Stimulation | Chronische Stimulation | Methodologische Unterschiede in Messungen |
| Klinische Schlussfolgerung | Kurzer Entzug | Lange Dysphorie | Longitudinale Daten am Menschen erforderlich |
⚖️ Widerspruch 3: Selektivität der Opioid-Hypothese der Trennung
Wenn Trennung tatsächlich ein Opioid-Entzugssyndrom auslöst, warum erleben nicht alle Menschen die gleiche Intensität der Symptome? Eine Hypothese: individuelle Unterschiede in der basalen Opioidrezeptordichte und Rezeptorgenetik (OPRM1-Polymorphismen).
Eine andere: soziale Bindung ist ein multisystemischer Prozess, und das Opioidsystem ist nur eine Komponente. Bindungsstile, die in der Kindheit geformt wurden, können die Sensitivität für sozialen Schmerz unabhängig vom Opioidsystem modulieren.
- Genetischer Faktor (OPRM1)
- Der A118G-Polymorphismus ist mit Unterschieden in der Opioid-Sensitivität und sozialem Schmerz verbunden. Menschen mit der G-Variante könnten anfälliger für emotionalen Entzug sein.
- Kontextueller Faktor (Bindungsgeschichte)
- Menschen mit sicherer Bindung können ein stabileres Grundniveau endogener Opioide haben, was den Schmerz der Zurückweisung abpuffert.
- Zeitlicher Faktor (Beziehungsdauer)
- Je länger die Beziehung, desto höher die Wahrscheinlichkeit einer chronischen Hochregulierung des Opioidsystems und folglich eines ausgeprägteren Entzugssyndroms.
🔍 Widerspruch 4: Opioide vs. andere Neurotransmitter
Die meisten Studien zu sozialem Schmerz weisen auch auf die Rolle von Dopamin, Serotonin und Oxytocin hin. Ist das Opioidsystem primär oder sekundär? Oder ist dies eine falsch gestellte Frage?
Wahrscheinlicher ist, dass soziale Bindung ein integriertes System ist, in dem Opioide, Dopamin und Oxytocin synergistisch wirken. Die Neurobiologie der Trennung umfasst die Aktivierung mehrerer Systeme gleichzeitig, und eines als das „Hauptsystem" herauszustellen ist eine Vereinfachung für Forschungszwecke, keine Beschreibung der Realität.
📋 Wie diese Konflikte zu interpretieren sind
- Widersprüche in der Wissenschaft sind normal, kein Zeichen von Schwäche. Sie zeigen die Grenzen des aktuellen Wissens auf.
- Selektives Zitieren zugunsten einer Hypothese (z.B. „es sind nur Opioide") ist eine rote Flagge. Ehrliche Analyse erfordert die Anerkennung alternativer Erklärungen.
- Extrapolation von Nagetieren auf Menschen erfordert Vorsicht. Menschlicher sozialer Schmerz ist ein komplexeres Phänomen als ein Labor-Zurückweisungsparadigma.
- Individuelle Unterschiede (Genetik, Geschichte, Kontext) werden oft zugunsten universeller Mechanismen ignoriert. Das ist ein Fehler.
Fazit: Die Opioid-Hypothese der Trennung hat eine solide neurobiologische Grundlage, aber sie beschreibt einen Teil des Mechanismus, nicht den gesamten Prozess. Sie als vollständige Erklärung zu verwenden bedeutet, den Fehler des Reduktionismus zu begehen.
