Candida und erhöhte Darmpermeabilität: wissenschaftliche Fakten und Mythenλ
Wir analysieren den Zusammenhang zwischen Pilzmikrobiota und der Störung der Darmbarriere auf Basis wissenschaftlicher Daten und klinischer Studien
Overview
Der Begriff „Leaky Gut" ist aus der Alternativmedizin in den wissenschaftlichen Diskurs gewandert — dahinter steht ein messbares Phänomen: die erhöhte Darmpermeabilität. Candida albicans, ein gewöhnlicher Bewohner der Mikrobiota, kann bei Dysbalance die Tight Junctions des Epithels zerstören 🧬 und systemische Entzündungen provozieren. Klinische Daten verbinden dies mit Autoimmunerkrankungen, Stoffwechselstörungen und chronisch-entzündlichen Darmerkrankungen.
🛡️
Laplace-Protokoll: Wir trennen etablierte wissenschaftliche Fakten über die Störung der Darmbarriere von populären Vereinfachungen und stützen uns auf peer-reviewte Studien und klinische Daten. Es ist wichtig, den Unterschied zwischen bewiesenen Mechanismen und Hypothesen zu verstehen, die weitere Untersuchungen erfordern.
Reference Protocol
Wissenschaftliche Grundlage
Evidenzbasierter Rahmen für kritische Analyse
Protocol: Evaluation
Teste Dich
Quiz zu diesem Thema kommt bald
⚡
Vertiefung
Was tatsächlich mit der Darmbarriere bei erhöhter Permeabilität geschieht
Wissenschaftliche Definition und Mechanismen der Barrierestörung
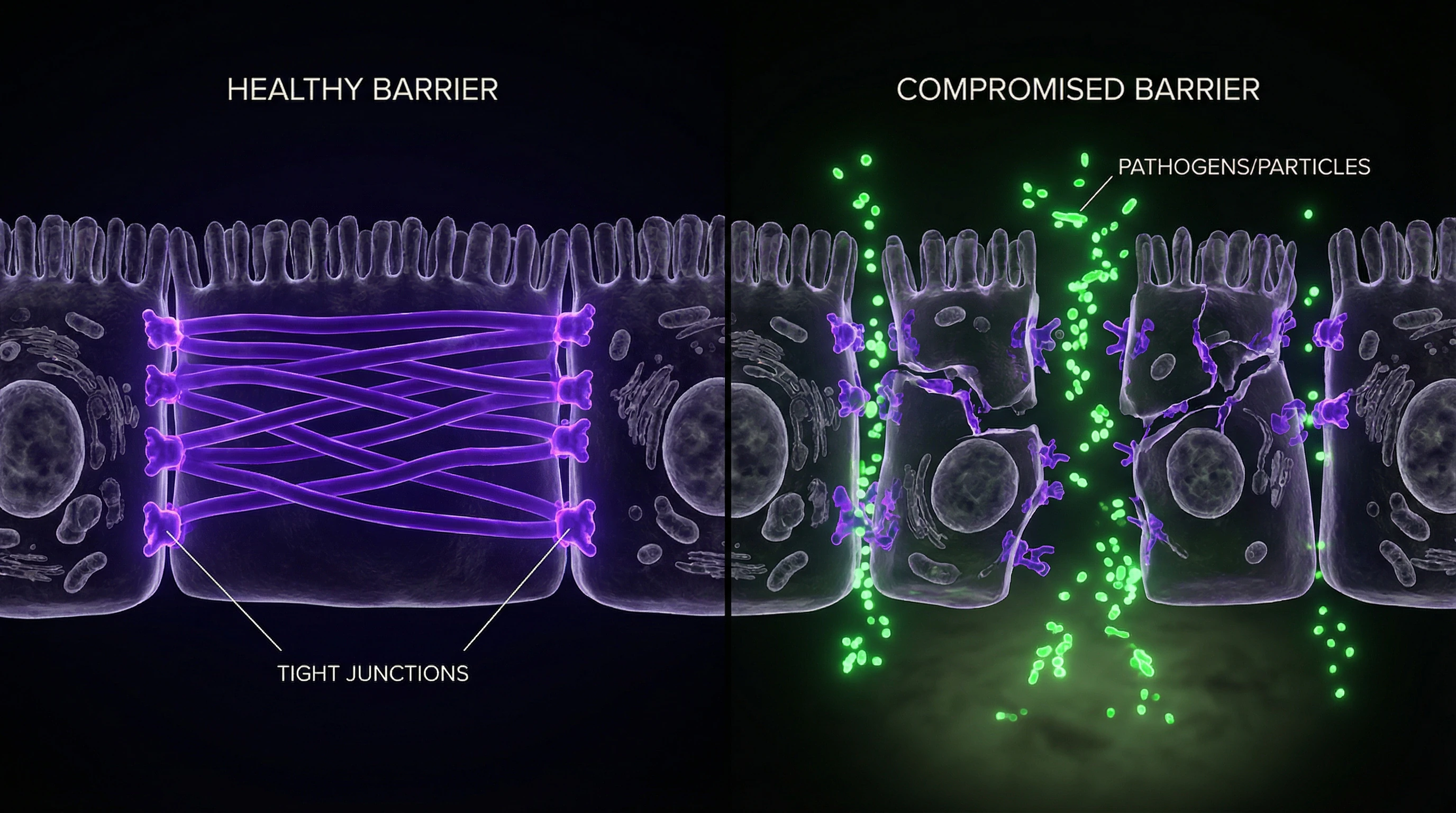
„Leaky Gut" – ein populärwissenschaftlicher Begriff für erhöhte Darmpermeabilität, einen Zustand, bei dem die Tight Junctions zwischen Epithelzellen geschwächt werden und Substanzen aus dem Darmlumen in erhöhten Mengen in den Blutkreislauf gelangen können.
Die Darmbarriere ist ein mehrschichtiges System: Schleimschicht, Epithelzellen, Tight Junctions und Immunkomponenten der Schleimhaut. Bei ihrer Störung verstärkt sich der Transport von Lipopolysacchariden gramnegativer Bakterien und anderen potenziell toxischen Molekülen durch die Darmwand.
| Barrierekomponente | Funktion | Was bei Störung geschieht |
|---|---|---|
| Schleimschicht | Physischer Schutz, Umgebung für Mikrobiota | Verringerung der Dicke, Verlust des Schutzes |
| Epithelzellen | Selektiver Transport, Metabolismus | Apoptose, Dysfunktion, erhöhte Permeabilität |
| Tight Junctions | Regulation des parazellulären Transports | Bruch der Verbindungen, unkontrollierter Moleküldurchgang |
| Immunkomponenten | Pathogenerkennung, Toleranz | Hyperaktivierung oder Dysregulation |
Erhöhte Permeabilität ist mit chronischen Nierenerkrankungen, kardiovaskulären und dermatologischen Problemen assoziiert. Dies ist keine eigenständige Diagnose, sondern ein pathophysiologischer Mechanismus, der vielen Erkrankungen zugrunde liegt.
Rolle der Tight Junctions zwischen Epithelzellen
Tight Junctions sind das Schlüsselelement der Barrierefunktion. Sie bilden eine selektive Barriere, die den parazellulären Transport reguliert (Bewegung von Substanzen zwischen den Zellen, nicht durch sie hindurch).
- Transmembranproteine
- Occludin, Claudine, JAM – durchdringen die Membran und schaffen eine physische Abdichtung zwischen den Zellen.
- Zytoplasmatische Proteine
- ZO-1, ZO-2, ZO-3 – verbinden den Komplex mit dem Zytoskelett und gewährleisten mechanische Festigkeit.
- Strukturstörung
- Jeder Defekt in diesen Proteinen führt zu erhöhter Permeabilität und Eindringen großer Moleküle.
Proinflammatorische Zytokine, bakterielle Toxine, pH-Veränderungen und oxidativer Stress – all dies kann die Integrität der Tight Junctions beeinträchtigen.
Bei Dysfunktion der Tight Junctions erhalten bakterielle Komponenten und unverdaute Nahrungsantigene Zugang zur Submukosa, wo sie mit Immunzellen interagieren. Dies initiiert lokale und systemische Entzündungen und schafft einen Teufelskreis: Entzündung beeinträchtigt zusätzlich die Barrierefunktion.
Candida im Darm: vom normalen Bewohner zum Krankheitserreger
Kommensale Rolle der Pilze in der Mikrobiota
Candida albicans ist ein natürlicher Darmbewohner, gehört zur normalen Mikrobiota und existiert in ausgewogenen Mengen ohne pathologische Folgen. Das Darmökosystem basiert auf einem dynamischen Gleichgewicht zwischen Bakterien, Pilzen, Viren und Archaeen.
Candida wird durch kompetitive Wechselwirkungen mit der bakteriellen Flora und die Immunüberwachung des Wirts in Schach gehalten. In geringen Mengen können diese Pilze an Stoffwechselprozessen und dem Training des Immunsystems beteiligt sein.
- pH-Wert der Darmumgebung
- Verfügbarkeit von Nährstoffen
- Produktion antimikrobieller Peptide durch das Epithel
- Sekretion von Immunglobulinen
Bedingungen für übermäßiges Wachstum und Transformation zum Pathogen
Die unkontrollierte Proliferation von Candida beginnt mit Dysbiose – einer Störung des mikrobiellen Gleichgewichts. Breitspektrum-Antibiotika vernichten konkurrierende Bakterien und schaffen Nischen für opportunistische Mikroorganismen.
Bei übermäßigem Wachstum wechselt Candida von der Hefe- zur Hyphenform (Myzelform) – invasiver und fähig, Gewebe zu schädigen.
Immunologische Dysfunktion ist ein kritischer Faktor bei der Entwicklung von Candidose. Ein gesundes Immunsystem kontrolliert die Pilzpopulation effektiv; seine Beeinträchtigung bei HIV-Infektion, Kortikosteroid-Einnahme, Chemotherapie oder angeborenen Immundefekten schafft Bedingungen für eine Invasion.
Zusätzliche Auslöser: Ernährung mit hohem Gehalt an einfachen Kohlenhydraten (Nährsubstrat für Pilze), chronischer Stress und hormonelle Veränderungen. Bei günstigen Bedingungen löst Candida eine Kaskade pathologischer Veränderungen aus, die nicht nur den Darm betreffen.
Mechanismen der Candida-Wirkung auf die Durchlässigkeit der Darmbarriere
Direkte Schädigung des Epithels und der Tight Junctions
Candida albicans greift die Darmbarriere auf mehreren Wegen gleichzeitig an. Die Hyphenform des Pilzes dringt physisch zwischen Epithelzellen ein und invadiert sie, wodurch die Integrität der Monoschicht mechanisch gestört wird.
Die Pilze sezernieren proteolytische Enzyme – sekretierte Aspartylproteasen und Phospholipasen, die Tight-Junction-Proteine, insbesondere Occludin, zerstören. Ergebnis: Die parazelluläre Permeabilität steigt.
- Candidalysin (zytolytisches Peptidtoxin) bildet Poren in Membranen von Epithelzellen und verursacht deren Tod
- Adhäsine auf der Pilzoberfläche (Als3) ermöglichen Anheftung und induzieren Endozytose – Pilze dringen in Zellen ein
- Biofilme schaffen eine geschützte Umgebung und verstärken die Resistenz gegen Immunfaktoren und Antimykotika
Die Gesamtheit dieser Mechanismen führt zu struktureller Barriereschädigung und erhöhter Permeabilität für verschiedene Moleküle.
Rolle von Dysbiose und Immunantwort bei der Barrierestörung
Übermäßiges Candida-Wachstum ist gleichzeitig Folge und Ursache mikrobiellen Ungleichgewichts. Dysbiose bedeutet verringerte Mikrobiota-Diversität, Abnahme nützlicher Bakterien (besonders Produzenten kurzkettiger Fettsäuren) und Zunahme bedingt pathogener Mikroorganismen.
Kurzkettige Fettsäuren, vor allem Butyrat, versorgen Kolonozyten mit Energie und regulieren die Expression von Tight-Junction-Proteinen. Bei Dysbiose sinkt ihre Produktion – die Barriere schwächt sich.
Die Immunantwort auf übermäßiges Candida-Wachstum verschlimmert paradoxerweise die Schädigung. Die Erkennung von Pilzmustern (Dectin-1, TLR2, TLR4) aktiviert die Produktion proinflammatorischer Zytokine: TNF-α, IL-1β, IL-6, IL-17.
| Zytokin | Mechanismus der Barriereschädigung |
|---|---|
| TNF-α, IFN-γ | Stören direkt die Tight-Junction-Funktion und erhöhen die Permeabilität |
| IL-1β, IL-6, IL-17 | Erhalten chronische Entzündung aufrecht, verstärken Immunaktivierung |
Chronische Entzündung schafft einen Teufelskreis: Erhöhte Permeabilität ermöglicht mehr Antigenen, die Barriere zu durchdringen, was die Immunaktivierung und weitere Schädigung verstärkt.
Störungen der Darmmikrobiota beeinflussen sogar entfernte Outcomes – beispielsweise spontane Frühgeburten, was die systemische Bedeutung der Darmbarriere demonstriert.
Wissenschaftliche Evidenz und Forschungslücken zum Zusammenhang zwischen Candida und Darmpermeabilität
Was durch klinische Studien belegt ist
Erhöhte Darmpermeabilität ist ein reales klinisches Phänomen, das bei chronischer Nierenerkrankung, kardiovaskulären Erkrankungen und dermatologischen Zuständen dokumentiert wurde. Dies weist auf die systemische Bedeutung der intestinalen Barrierefunktion hin.
Die Rolle der Mikrobiota in der Krankheitspathogenese hat erhebliche wissenschaftliche Bestätigung erhalten. Der mikrobiell-gewebliche Komplex beeinflusst die interindividuelle Variabilität von Gesundheitsoutcomes.
Candida albicans ist als kommensaler Organismus anerkannt, der unter bestimmten Bedingungen pathogen werden kann — insbesondere im Kontext von Antibiotikatherapie und Immundysfunktion.
Die Mechanismen der Barriereschädigung sind detailliert untersucht: Endogene und exogene Faktoren stören Tight Junctions zwischen Epithelzellen und erhöhen den Transport von Lipopolysacchariden gramnegativer Bakterien in den Blutkreislauf.
| Faktor | Wirkmechanismus | Evidenzstatus |
|---|---|---|
| TNF-α, IFN-γ | Direkte Störung von Tight-Junction-Proteinen | Bestätigt |
| Mikrobiota-Dysbiose | Assoziation mit systemischen Erkrankungen | Korrelative Daten |
| Candida-induzierte Entzündung | Teufelskreis aus Entzündung und Permeabilität | Erfordert Klärung |
Bereiche, die weitere Untersuchung erfordern
Direkte Evidenz für einen spezifischen Zusammenhang zwischen Candidose und erhöhter Darmpermeabilität bleibt begrenzt. Die meisten verfügbaren Daten sind korrelativ und nicht kausal.
Der Begriff "Leaky Gut" wird sowohl in wissenschaftlichen als auch in pseudowissenschaftlichen Kontexten verwendet, was terminologische Verwirrung schafft und die Interpretation von Studien erschwert.
Systematische Reviews zu diesem spezifischen Thema sind rar. Narrative Reviews können subjektiven Einflüssen der Autoren unterliegen.
Spezifische Signalwege, die Darmdysfunktion mit systemischen Erkrankungen verbinden, bleiben Gegenstand aktiver Forschung, insbesondere im Kontext der "Darm-Organ-Achsen".
Der Einfluss der mütterlichen Darmmikrobiota auf Langzeitoutcomes wie Frühgeburten demonstriert die Komplexität systemischer Interaktionen, die noch vollständig entschlüsselt werden müssen.
Randomisierte kontrollierte Studien sind erforderlich, um die Wirksamkeit therapeutischer Interventionen zur Barriererestauration bei Candidose zu bewerten.

Risikofaktoren und Auslöser für die Störung der Darmbarriere bei Candidiasis
Antibiotika und Immunsuppression
Breitspektrum-Antibiotikatherapie eliminiert konkurrierende Bakterienpopulationen, die normalerweise die Pilzbesiedlung eindämmen. Dies ist einer der bedeutendsten Risikofaktoren für übermäßiges Candida-Wachstum im Darm.
Immunsuppressive Zustände — HIV-Infektion, Chemotherapie, Langzeitanwendung von Kortikosteroiden, Immundefizienz-Syndrome — transformieren kommensale Candida in eine pathogene Form. Die Beeinträchtigung der lokalen Schleimhautimmunität (Verringerung von sekretorischem IgA, Dysfunktion der Th17-Antwort) schwächt die Abwehr gegen Pilzinvasion.
Die Kombination aus Antibiotikatherapie und Immunsuppression erzeugt einen synergistischen Effekt, der das Risiko für systemische Candidiasis und Barriereschädigung dramatisch erhöht.
Ernährung und Lebensstil
Eine Ernährung mit hohem Gehalt an raffinierten Kohlenhydraten und Zucker ist die Hauptenergiequelle für Pilze. Chronischer Stress aktiviert die Hypothalamus-Hypophysen-Nebennierenrinden-Achse, erhöht Cortisol und verändert die Zusammensetzung der Mikrobiota.
Alkoholmissbrauch schädigt direkt das Darmepithel, stört Tight Junctions und fördert Dysbiose. Unzureichende Aufnahme von Ballaststoffen reduziert die Produktion kurzkettiger Fettsäuren, die für die Integrität der Epithelbarriere und die Regulation der Immunantwort notwendig sind.
| Risikofaktor | Wirkmechanismus | Folge für die Barriere |
|---|---|---|
| Breitspektrum-Antibiotika | Elimination konkurrierender Bakterien | Unkontrolliertes Candida-Wachstum |
| Immunsuppression | Verringerung von lokalem IgA und Th17 | Pilzinvasion ins Epithel |
| Kohlenhydratreiche Ernährung | Energiesubstrat für Pilze | Candida-Proliferation |
| Chronischer Stress | Hypercortisolämie, Dysbiose | Erhöhte Permeabilität |
| Alkohol | Direkte Epithelschädigung | Störung der Tight Junctions |
| Ballaststoffmangel | Verringerung kurzkettiger Fettsäuren | Schwächung von Barriere und Immunität |
Diagnostik und evidenzbasierte Ansätze zur Wiederherstellung der Darmbarriere
Klinische Bewertungsmethoden
Die Diagnose einer erhöhten Darmpermeabilität bleibt aufgrund fehlender standardisierter Tests und klarer diagnostischer Kriterien eine Herausforderung. Drei Hauptansätze werden in der Praxis verwendet, aber jeder hat Einschränkungen.
| Methode | Prinzip | Klinischer Status |
|---|---|---|
| Lactulose-Mannitol | Verhältnis der Zuckerausscheidung im Urin | Forschungsstadium; geringe Verfügbarkeit |
| Zonulin im Serum | Biomarker für Permeabilität | Umstrittene Spezifität und Bedeutung |
| Stuhlmikrobiologie | Quantitative Bewertung von Candida | Standard für Candidose-Diagnose |
Entscheidender Punkt: Das bloße Vorhandensein von Candida im Stuhl ist bei gesunden Menschen normal. Die Diagnose erfordert eine quantitative Bewertung der Pilzbelastung, nicht nur den Nachweis.
Evidenzbasierte Strategien zur Barriereregeneration
Eine antimykotische Therapie mit Fluconazol oder Nystatin ist nur bei dokumentiertem übermäßigem Candida-Wachstum und unter ärztlicher Aufsicht indiziert. Eine Verschreibung ohne mikrobiologische Bestätigung ist ein Fehler im diagnostischen Denken.
Probiotische Stämme wie Lactobacillus rhamnosus GG und Saccharomyces boulardii konkurrieren mit Candida und unterstützen die Barrierefunktion, aber die Wirksamkeit hängt von Stamm und Dosis ab. Dies ist keine universelle Lösung.
Diätetische Interventionen – Einschränkung raffinierter Kohlenhydrate und Erhöhung der Ballaststoffzufuhr – modulieren die Mikrobiota und verbessern die metabolische Darmgesundheit. Dies ist die Grundlage, die der erste Schritt sein sollte.
Glutamin, Butyrat und Nährstoffe, die den Energiestoffwechsel der Enterozyten unterstützen, zeigen Potenzial bei der Wiederherstellung der Epithelintegrität, erfordern jedoch weitere klinische Studien zur Bestimmung optimaler Protokolle.
Umfassendes Protokoll und Risiken der Selbstbehandlung
Die Wiederherstellung der Darmbarriere erfordert die Beseitigung auslösender Faktoren: ungerechtfertigter Antibiotikaeinsatz, Korrektur des Immunstatus, Lebensstilmodifikation. Dies ist ein systemischer Ansatz, keine punktuelle Intervention.
Selbstdiagnose und Selbstbehandlung ohne ärztliche Aufsicht bergen reale Risiken. Symptome, die dem „Leaky Gut" und der Candidose zugeschrieben werden, können ernsthafte Erkrankungen maskieren, die eine spezifische Therapie erfordern.
Die Individualisierung therapeutischer Protokolle basierend auf klinischem Bild, Labordaten und Risikofaktoren ist der Schlüssel zur effektiven Wiederherstellung der Barrierefunktion. Universelle Schemata existieren nicht.
Knowledge Access Protocol
FAQ
Häufig gestellte Fragen
Dies ist die populäre Bezeichnung für eine erhöhte Darmpermeabilität, bei der die Tight Junctions zwischen den Darmzellen gestört sind. Dadurch gelangen Substanzen durch die Darmwand in den Blutkreislauf, die normalerweise nicht passieren sollten — bakterielle Toxine, unverdaute Nahrungspartikel. Der wissenschaftliche Begriff lautet Störung der strukturell-funktionellen Integrität der Darmbarriere.
Übermäßiges Candida-Wachstum kann zur Störung der Darmbarriere beitragen, ist aber nicht die einzige Ursache. Bei Dysbiose setzen Pilze Toxine und Enzyme frei, die das Darmepithel schädigen. Der direkte Kausalzusammenhang erfordert jedoch weitere Forschung — es handelt sich um einen multifaktoriellen Prozess.
Es gibt keine spezifischen Symptome — die Manifestationen sind unspezifisch und umfassen Blähungen, Stuhlunregelmäßigkeiten, Nahrungsmittelunverträglichkeiten, chronische Müdigkeit. Es können Hautprobleme, allergische Reaktionen und entzündliche Prozesse in verschiedenen Organen auftreten. Die Diagnose wird nur vom Arzt auf Basis einer umfassenden Untersuchung gestellt, nicht anhand einzelner Symptome.
Ja, Antibiotika zerstören nicht nur pathogene, sondern auch nützliche Bakterien und schaffen damit Bedingungen für Pilzwachstum. Candida ist resistent gegen antibakterielle Präparate und besetzt die freigewordene ökologische Nische. Besonders hoch ist das Risiko bei längeren oder wiederholten Antibiotikakuren ohne probiotische Unterstützung.
Ernährung ist ein wichtiger, aber nicht der einzige Bestandteil der Wiederherstellung der Darmbarriere. Das Weglassen provozierender Lebensmittel (Zucker, Alkohol, raffinierte Kohlenhydrate) und die Zugabe entzündungshemmender Nährstoffe hilft, erfordert aber einen ganzheitlichen Ansatz. Notwendig ist die Arbeit an den Ursachen: Stress, Infektionen, Medikamente, unter Kontrolle eines Spezialisten.
In der klinischen Praxis werden Tests auf Zonulin (Permeabilitätsmarker), Lipopolysaccharide (LPS), Antikörper gegen Darmwandkomponenten verwendet. Auch der Lactulose-Mannitol-Test und die Bewertung von Calprotectin kommen zum Einsatz. Standardisierte Diagnoseprotokolle existieren jedoch noch nicht — die Interpretation der Ergebnisse erfordert ärztliche Erfahrung.
Nein, Candida ist bei den meisten gesunden Menschen als Teil der normalen Mikrobiota im Darm vorhanden. Probleme entstehen nur bei übermäßigem Wachstum aufgrund geschwächter Immunität, Dysbiose oder anderer Faktoren. Das Vorhandensein von Pilzen bedeutet nicht automatisch Erkrankung — wichtig ist das Gleichgewicht der Mikroorganismen.
Probiotika können die Wiederherstellung der Mikrobiota unterstützen und mit Candida um Ressourcen konkurrieren, sind aber keine eigenständige Behandlung. Die Wirksamkeit hängt von Stämmen, Dosierungen und individuellen Besonderheiten ab. Die besten Ergebnisse werden in Kombination mit Ernährung, Beseitigung von Triggern und gegebenenfalls antimykotischer Therapie erzielt.
Ja, chronischer Stress erhöht die Darmpermeabilität direkt über die Hirn-Darm-Achse. Stresshormone (Cortisol) stören die Tight Junctions zwischen Epithelzellen und verändern die Zusammensetzung der Mikrobiota. Dies schafft einen Teufelskreis: Stress verschlechtert die Barriere, und die gestörte Barriere verstärkt Entzündungen und Stressreaktionen.
Ja, Candida nutzt einfache Kohlenhydrate (Zucker, Weißmehl) als Hauptenergiequelle für Wachstum. Eine kohlenhydratreiche Ernährung schafft ein günstiges Milieu für Pilzvermehrung. Ein vollständiger Verzicht auf Kohlenhydrate ist jedoch nicht erforderlich — wichtig sind Balance und Qualität der Kohlenhydrate (Bevorzugung komplexer Kohlenhydrate mit Ballaststoffen).
Studien zeigen einen Zusammenhang zwischen erhöhter Darmpermeabilität und bestimmten Autoimmunerkrankungen, aber ein kausaler Zusammenhang ist nicht abschließend bewiesen. Eine gestörte Barriere kann Antigene durchlassen, die eine Immunreaktion auslösen. Unklar bleibt jedoch, was primär ist — die Permeabilität oder der Autoimmunprozess; dies ist ein Gebiet aktiver Forschung.
Nein, Selbstdiagnosen sind unzuverlässig — die Symptome einer Candida-Infektion sind unspezifisch und überschneiden sich mit zahlreichen anderen Erkrankungen. Populäre „Heimtests
Hilfreich sind Lebensmittel, die reich an Glutamin (Knochenbrühe, Fleisch), Omega-3-Fettsäuren (fetter Fisch), Polyphenolen (Beeren, Blattgemüse) und Zink (Kürbiskerne) sind. Fermentierte Lebensmittel (Sauerkraut, Kefir) unterstützen die Mikrobiota. Wichtig sind Ballaststoffe aus Gemüse zur Ernährung nützlicher Bakterien, die kurzkettige Fettsäuren produzieren, welche die Barriere stärken.
Die Dauer ist individuell und hängt vom Ausmaß der Schädigung, den Ursachen und der Einhaltung der Empfehlungen ab — von einigen Wochen bis zu mehreren Monaten. Das Darmepithel erneuert sich alle 3-5 Tage, aber die Wiederherstellung der Barrierefunktion und der Mikrobiota erfordert mehr Zeit. Wichtig ist Konsequenz: Beseitigung von Triggern, entzündungshemmende Ernährung, Unterstützung der Mikrobiota.
Ja, systemische Antimykotika können das Gleichgewicht der Mikrobiota stören, wenn auch in geringerem Maße als Antibiotika. Sie wirken nicht nur auf pathogene Pilze, sondern auch auf kommensale Mikroorganismen. Daher werden sie streng nach Indikation, kurweise, mit gleichzeitiger probiotischer Unterstützung und unter ärztlicher Kontrolle verordnet.
Studien zeigen einen möglichen Zusammenhang über die Darm-Hirn-Achse: Dysbiose und Entzündungen können Neurotransmitter und Stimmung beeinflussen. Candida-Toxine könnten theoretisch bei erhöhter Permeabilität auf das ZNS einwirken. Direkte Beweise sind jedoch begrenzt — dies ist ein vielversprechendes Forschungsgebiet, das vorsichtige Interpretation erfordert.
