Darmparasiten: Auswirkungen auf das Mikrobiom und die Darmgesundheitλ
Wissenschaftlich fundierter Ansatz zum Verständnis des Zusammenhangs zwischen parasitären Infektionen, Mikrobiota-Zusammensetzung und funktioneller Gesundheit des Verdauungssystems
Overview
Darmparasiten verändern die Zusammensetzung der Mikrobiota — 🧬 das ist kein Mythos, sondern ein messbarer Effekt mit Folgen für Immunität, Nährstoffaufnahme und Darmbarrierefunktion. Mechanismus: Konkurrenz um Ressourcen, Toxine, Schleimhautentzündung. Risikogruppe — Immunsuppression (Chemotherapie, HIV, Transplantation), aber die meisten „Parasiten-Paniken" in sozialen Medien basieren auf der Verwechslung von Korrelation mit Kausalität und der Ignorierung von Basisraten.
🛡️
Laplace-Protokoll: Die Diagnose parasitärer Infektionen erfordert eine Laborbestätigung. Selbstdiagnose anhand von Symptomen und prophylaktische „Reinigungen" ohne medizinische Indikation werden nicht empfohlen. Die Behandlung sollte nur nach Bestätigung der Diagnose durch einen qualifizierten Facharzt verordnet werden.
Reference Protocol
Wissenschaftliche Grundlage
Evidenzbasierter Rahmen für kritische Analyse
Navigation Matrix
Unterabschnitte
[candida-leaky-gut]
Candida und Leaky-Gut-Syndrom
Wir analysieren den Zusammenhang zwischen Pilzmikrobiota und der Störung der Darmbarriere auf Basis wissenschaftlicher Daten und klinischer Studien
Erkunden
[everyone-has-parasites]
Jeder hat Parasiten
Die weit verbreitete Behauptung, dass alle Menschen Parasiten haben, wird durch wissenschaftliche Daten nicht gestützt und dient dem Verkauf fragwürdiger Produkte.
Erkunden
Protocol: Evaluation
Teste Dich
Quiz zu diesem Thema kommt bald
⚡
Vertiefung
Arten von Darmparasiten und Infektionsmechanismen: Was im Darm lebt
Darmparasiten sind eine heterogene Gruppe von Organismen, die den Gastrointestinaltrakt besiedeln und sich auf Kosten des Wirts ernähren. Man unterscheidet zwei Hauptkategorien: Helminthen (mehrzellige Würmer) und Protozoen (einzellige Organismen), jede mit einzigartigen Interaktionsmechanismen.
Das Verständnis der Biologie dieser Parasiten ist entscheidend für die Entwicklung effektiver diagnostischer und therapeutischer Ansätze.
Helminthen und Protozoen: Biologische Klassifikation
Helminthen umfassen drei Hauptklassen: Nematoden (Rundwürmer), Zestoden (Bandwürmer) und Trematoden (Saugwürmer). Jede Klasse besitzt spezifische morphologische Merkmale und Lebenszyklen.
Bodenübertragene Helminthen (soil-transmitted helminths, STH) sind in afrikanischen Populationen weit verbreitet und zeigen messbare Korrelationen mit der Zusammensetzung des Darmmikrobioms. Parasitäre Protozoen – Giardien, Amöben – zeichnen sich durch kürzere Lebenszyklen und die Fähigkeit zur schnellen Vermehrung im Darmmilieu aus.
- Wirkmechanismus der Helminthen
- Mechanische Schädigung der Schleimhaut und Konkurrenz um Nährstoffe.
- Wirkmechanismus der Protozoen
- Störung der Absorptionsprozesse und Provokation lokaler Entzündungen.
- Größenparadoxon
- Mikroskopische Protozoen können ausgeprägtere Symptomatik verursachen als große Helminthen.
Chronische Infektionen führen zur Produktion von Toxinen und Metaboliten, die systemisch das Immun- und Nervensystem des Wirts beeinflussen.
Übertragungswege und Risikofaktoren für Infektionen
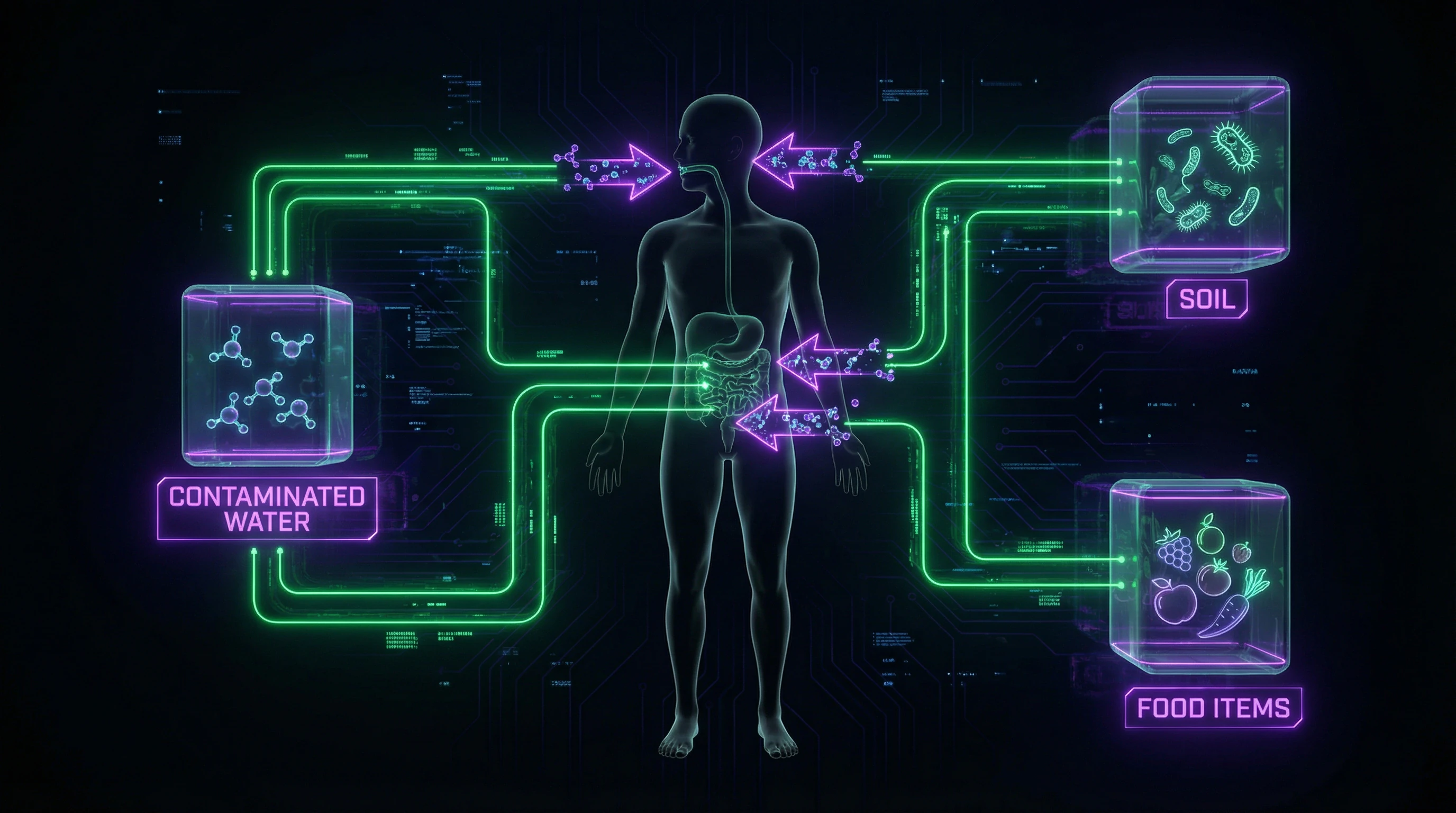
Hauptübertragungswege: fäkal-oraler Mechanismus durch kontaminiertes Wasser und Nahrung, direkter Kontakt mit infiziertem Boden, Transmission durch Zwischenwirte.
| Risikofaktor | Einfluss auf Übertragung |
|---|---|
| Geografische und sanitäre Bedingungen | Regionen mit unzureichender Wasseraufbereitung und niedrigem Hygieneniveau zeigen signifikant höhere Erkrankungsraten |
| Immunstatus | Immungeschwächte Patienten weisen erhöhte Anfälligkeit aufgrund geschwächter Abwehrmechanismen auf |
| Parasitentyp | Bodenübertragene Helminthen erfordern Kontakt mit infizierter Erde; Protozoen werden durch ungekochtes Wasser übertragen |
| Saisonalität | Infektionsspitzen in Perioden erhöhter Feuchtigkeit und Temperatur |
| Berufliche Tätigkeit | Arbeit in Landwirtschaft oder mit Boden erhöht die Wahrscheinlichkeit einer Helmintheninfektion erheblich |
Interaktion von Parasiten mit dem Darmmikrobiom: Veränderung des Ökosystems
Die Anwesenheit von Darmparasiten initiiert eine Kaskade von Veränderungen in der Zusammensetzung und funktionellen Aktivität des Darmmikrobioms — einer komplexen Gemeinschaft von Mikroorganismen, die eine Schlüsselrolle bei Verdauung, Immunität und Homöostase des Organismus spielen. Moderne metagenomische Studien haben messbare Korrelationen zwischen parasitären Infektionen und der Diversität der Mikrobiota aufgezeigt.
Diese Interaktionen sind bidirektional: Parasiten modifizieren die mikrobielle Umgebung, während das Mikrobiom das Überleben und die Virulenz der Parasiten beeinflusst.
Einfluss auf die Diversität der Mikrobiota
Parasitäre Infektionen zeigen statistisch signifikante Assoziationen mit Veränderungen der Alpha- und Beta-Diversität des Darmmikrobioms, was durch Analysen metagenomischer Daten aus afrikanischen Populationen bestätigt wurde. Bodenhelminthen korrelieren mit einer Zunahme der gesamten mikrobiellen Diversität, was eine adaptive Immunantwort oder den direkten Einfluss parasitärer Metaboliten auf die mikrobielle Ökologie widerspiegeln könnte.
Korrelation bedeutet nicht Kausalität. Multiple Faktoren — Ernährung, Geographie, Hygiene — beeinflussen die beobachteten Muster mikrobieller Diversität.
Eine Verringerung der Mikrobiota-Diversität wird mit bestimmten Arten parasitärer Infektionen assoziiert, insbesondere bei chronischen Protozoeninfektionen, was zu Dysbiose und Beeinträchtigung der Darmbarrierefunktion führen kann.
- Konkurrenz um Nährstoffsubstrate zwischen Parasit und Mikrobiota
- Produktion antimikrobieller Substanzen durch Parasiten
- Modulation der lokalen Immunantwort mit Auswirkung auf die mikrobielle Zusammensetzung
Die Wiederherstellung der mikrobiellen Diversität nach Elimination der Parasiten erfolgt graduell und kann zusätzliche probiotische Interventionen erfordern.
Veränderungen der bakteriellen Zusammensetzung bei Infektion
Spezifische taxonomische Verschiebungen in der Zusammensetzung des Mikrobioms werden bei verschiedenen parasitären Infektionen beobachtet: Zunahme proinflammatorischer Bakterien der Familie Enterobacteriaceae und Abnahme nützlicher Kommensalen wie Faecalibacterium prausnitzii.
Bei immunsupprimierten Patienten wurden besondere Muster von Mikrobiota-Veränderungen identifiziert, die sich von denen immunkompetenter Individuen unterscheiden, was auf die Rolle des Immunstatus bei der Formung mikrobiell-parasitärer Interaktionen hinweist. Diese Veränderungen können klinische Manifestationen verschlimmern und die Therapieeffizienz beeinflussen.
| Funktionelle Störung | Mechanismus | Klinische Bedeutung |
|---|---|---|
| Verringerung kurzkettiger Fettsäuren | Verlust butyratproduzierender Bakterien | Schwächung der Darmbarriere, Entzündung |
| Störung des Gallensäuremetabolismus | Veränderung der mikrobiellen Zusammensetzung | Dysregulation des Lipidstoffwechsels |
| Verringerte Synthese von Vitaminen B und K | Elimination synthetisierender Stämme | Mikronährstoffmangel, Gerinnungsstörungen |
Parasiten können selektiv das Wachstum bestimmter Bakterienstämme durch Sekretion spezifischer Moleküle oder Veränderung des pH-Werts der Darmmilieu unterdrücken. Die Wiederherstellung der normalen bakteriellen Zusammensetzung nach antiparasitärer Therapie erfolgt nicht immer spontan und kann eine gezielte Modulation des Mikrobioms erfordern.
Klinische Manifestationen und Symptome: von lokalen bis systemischen Effekten
Parasitäre Infektionen manifestieren sich in einem Spektrum von asymptomatischem Trägerstatus bis zu schweren systemischen Störungen. Die Symptome sind oft unspezifisch und imitieren gastroenterologische, immunologische oder psychiatrische Erkrankungen, was die Diagnose erschwert.
Symptome allein reichen nicht aus, um eine Infektion zu bestätigen — eine labordiagnostische Verifizierung ist erforderlich.
Systemische Effekte parasitärer Infektionen
Chronische, durch Parasiten induzierte Entzündungen sind der Schlüsselmechanismus systemischer Manifestationen: chronische Erschöpfung, Anämie, dermatologische Probleme. Toxine und Metaboliten der Parasiten gelangen durch die geschädigte Darmwand in den systemischen Blutkreislauf und beeinflussen entfernte Organe und Systeme.
Der Zusammenhang zwischen parasitären Infektionen und Depression wird in populären Quellen erwähnt, aber ein direkter kausaler Zusammenhang ist nicht etabliert. Depression ist eine multifaktorielle Erkrankung; chronische Infektionen können lediglich einer von vielen beitragenden Faktoren sein.
Allergische Reaktionen und Hautmanifestationen entstehen infolge immunologischer Hyperreaktivität auf parasitäre Antigene, aber Parasiten sind nicht die einzige Ursache dermatologischer Zustände. Anämie entwickelt sich durch Blutverlust bei Invasion hämatophager Parasiten oder durch gestörte Absorption von Eisen und Vitamin B12.
Immunmodulierende Effekte von Parasiten können das Immunsystem sowohl supprimieren als auch übermäßig aktivieren, was zu Autoimmunphänomenen oder erhöhter Anfälligkeit für Sekundärinfektionen führt.
Verdauungs- und Immunstörungen
Malabsorption von Nährstoffen ist eine direkte Folge der Schädigung des Darmepithels und der Konkurrenz der Parasiten um Nährstoffe. Es entwickeln sich Defizite an Vitaminen, Mineralstoffen und Proteinen.
- Die Störung der intestinalen Barrierefunktion begünstigt die Translokation bakterieller Komponenten und parasitärer Antigene in den systemischen Blutkreislauf, wobei die klinische Signifikanz Gegenstand wissenschaftlicher Debatten bleibt.
- Dyspeptische Symptome — Diarrhö, Obstipation, Blähungen, abdominale Schmerzen — entstehen infolge mechanischer Irritation, Entzündung und gestörter Darmmotilität.
- Immunologische Dysregulation manifestiert sich durch eine Verschiebung in Richtung Th2-Antwort mit erhöhter IgE-Produktion und Eosinophilie, was allergische Zustände verschlimmert.
Chronische Stimulation des Immunsystems durch parasitäre Antigene führt zur Erschöpfung der Immunreserven und zu einer paradoxen Verminderung der antiinfektiösen Abwehr.
Die Diagnostik erfordert eine umfassende Laboruntersuchung: Stuhlmikroskopie, serologische Tests, molekulargenetische Methoden zur präzisen Identifikation des Erregers.
Diagnostik parasitärer Infektionen: Von Symptomen zur Laborbestätigung
Labordiagnostische Verfahren
Die mikroskopische Stuhluntersuchung ist der Goldstandard zur Diagnose intestinaler Parasiten. Eine dreimalige Probenentnahme im Abstand von 3–5 Tagen ist erforderlich, um eine Sensitivität von 85–90% zu erreichen.
Die Kato-Katz-Konzentrationsmethode ermöglicht eine quantitative Bewertung der Helminthen-Befallsintensität – entscheidend für die Therapiewahl und epidemiologisches Monitoring.
| Methode | Spezifität | Nachweis von | Einschränkung |
|---|---|---|---|
| Stuhlmikroskopie | 85–90% | Eier, Larven, Trophozoiten | Erfordert wiederholte Proben |
| PCR | 95–99% | Speziesidentifikation, Kryptosporidien, Mikrosporidien | Teurer, nicht überall verfügbar |
| ELISA (Serologie) | Variabel | Antikörper IgM/IgG | Unterscheidet nicht zwischen aktiver und durchgemachter Infektion |
| Koprologie | — | pH-Wert, unverdaute Fasern, Fettsäuren | Ergänzende Methode |
Serologische Tests (ELISA) weisen spezifische Antikörper gegen parasitäre Antigene nach, aber ein positives Ergebnis kann sowohl eine aktive als auch eine durchgemachte Infektion bedeuten – klinische Interpretation erforderlich.
Molekulargenetische Methoden (PCR) bieten hohe Spezifität und identifizieren Parasiten auf Speziesebene, einschließlich Kryptosporidien und Mikrosporidien, die mikroskopisch schwer nachweisbar sind.
Eosinophilie im peripheren Blut (>5% oder >500 Zellen/µl) ist ein indirekter Marker für Helminthosen, besonders in der Migrationsphase, aber unspezifisch und erfordert Differentialdiagnostik gegenüber allergischen Zuständen.
Differentialdiagnostik
Symptome parasitärer Infektionen sind oft unspezifisch und überschneiden sich mit chronisch-entzündlichen Darmerkrankungen (CED), Reizdarmsyndrom (RDS) und Zöliakie.
Chronische Diarrhö mit Blutbeimengung kann sowohl auf Amöbiasis als auch auf Colitis ulcerosa hinweisen. Endoskopische Untersuchung mit Biopsie zeigt charakteristische Ulzera und Trophozoiten von Entamoeba histolytica im Gewebe.
Eosinophile Gastroenteritis durch Gewebshelminthen wird von allergischen Reaktionen auf Nahrungsmittel und Medikamente durch Eliminationsdiät und Provokationstests unterschieden.
Bei immunsupprimierten Patienten (Krebspatienten, HIV-Infizierte) verlaufen Parasitosen atypisch und sind häufig mit opportunistischen Infektionen kombiniert.
Kryptosporidiose und Isosporiasis bei HIV manifestieren sich durch profuse Diarrhö, die Cholera imitiert. Spezielle Färbemethoden (Ziehl-Neelsen) sind zum Nachweis von Oozysten erforderlich.
Labormarker für Entzündung (CRP, fäkales Calprotectin) sind sowohl bei Parasitosen als auch bei CED erhöht. Werte >250 µg/g sind charakteristischer für Morbus Crohn und Colitis ulcerosa.
Wissenschaftlich fundierte Ansätze zur Behandlung parasitärer Infektionen
Antiparasitäre Therapie
Die Wahl des Anthelminthikums hängt von der Parasitenart, der Befallsintensität und dem Zustand des Patienten ab. Selbstmedikation ohne Laborbestätigung ist unzulässig: Risiko toxischer Effekte und Resistenzentwicklung.
| Präparat | Wirkungsspektrum | Dosierung | Mechanismus |
|---|---|---|---|
| Albendazol | Nematoden, einige Zestoden | 400 mg einmalig oder 3 Tage | Hemmung der Tubulinpolymerisation |
| Praziquantel | Trematoden, Zestoden | 10–25 mg/kg (abhängig von der Art) | Hohe Wirksamkeit (85–95%), geringe Toxizität |
| Metronidazol | Amöbiasis, Giardiasis | 750 mg × 3-mal täglich, 7–10 Tage | Spezifische Therapie protozoischer Infektionen |
| Nitazoxanid | Kryptosporidiose | Nach Schema (immunkompetente Patienten) | Alternative bei Resistenz |
Die Wirksamkeitskontrolle erfolgt nach 2–4 Wochen durch wiederholte parasitologische Stuhluntersuchung. Persistierende Parasiten weisen auf Resistenz oder Reinfektion hin.
Bei onkologischen Patienten erfordern Dosierungen eine Anpassung: Myelosuppression und Hepatotoxizität der Chemotherapie verändern die Pharmakokinetik antiparasitärer Mittel.
Wiederherstellung des Mikrobioms nach der Behandlung
Antiparasitäre Therapie, insbesondere Metronidazol und Breitspektrum-Antibiotika, verursacht Dysbiose: Verringerung der Mikrobiota-Diversität und Abnahme der Populationen kurzkettige Fettsäuren produzierender Bakterien.
Das Wiederherstellungsschema umfasst drei Komponenten:
- Probiotika (4–8 Wochen nach Behandlung): Lactobacillus rhamnosus GG, Saccharomyces boulardii, Bifidobacterium longum — reduzieren die Häufigkeit postinfektiösen Reizdarmsyndroms.
- Präbiotika (5–10 g/Tag): Inulin, Fructooligosaccharide stimulieren das Wachstum der eigenen nützlichen Mikroflora.
- Diätetische Korrektur: fermentierte Lebensmittel (Kefir, Sauerkraut), Ballaststoffe (25–30 g/Tag) unterstützen die Wiederherstellung und Barrierefunktion des Darms.
Metagenomische Analysen zeigen: Die vollständige Wiederherstellung der mikrobiellen Diversität dauert 3–6 Monate. Bei einem Teil der Patienten bleiben langfristige Veränderungen der Mikrobiota-Zusammensetzung bestehen.
Monitoring funktioneller Parameter (Stuhlfrequenz, abdominale Symptome) und bei Bedarf wiederholte Mikrobiomanalyse ermöglichen die Bewertung der Wirksamkeit der Wiederherstellungstherapie.
Prävention parasitärer Infektionen und Risikomanagement
Hygienepraktiken und Lebensmittelsicherheit
Händewaschen mit Seife nach dem Toilettengang, Bodenkontakt und vor dem Essen reduziert das Risiko fäkal-oraler Übertragung um 40–50%. Dies ist die effektivste und zugänglichste Präventionsmaßnahme.
Thermische Behandlung von Fleisch auf 63°C für Schweinefleisch und 71°C für Rindfleisch tötet Trichinellenlarven und Zystizerkose ab. Gemüse und Obst werden roh unter fließendem Wasser gewaschen, besonders bei organischer Düngung.
Die Qualität des Trinkwassers ist kritisch: Abkochen für 1 Minute oder Filtration durch Poren <1 µm entfernt Giardien-Zysten und Kryptosporidien-Oozysten.
In endemischen Regionen wird das Baden in Süßwassergewässern vermieden (Schistosomiasis-Prävention) und Schuhwerk auf Böden getragen (Schutz vor Hakenwurm und Strongyloidiasis). Entwurmung von Haustieren alle 3–6 Monate minimiert das Risiko zoonotischer Parasitosen.
Hochrisikogruppen
Immungeschwächte Patienten — mit Krebserkrankungen, HIV-Infektion, unter immunsuppressiver Therapie — haben ein erhöhtes Risiko für schwere Verläufe von Parasitosen. Bei Krebspatienten erreicht die Prävalenz intestinaler parasitärer Infektionen je nach Region 15–30%, Infektionen verlaufen atypisch und werden verzögert diagnostiziert.
| Risikogruppe | Hauptrisiko | Präventionsmaßnahme |
|---|---|---|
| Vorschulkinder in Gemeinschaftseinrichtungen | Madenwürmer, Giardien (enge Kontakte) | Regelmäßige präventive Untersuchungen |
| Reisende in endemische Regionen | Multiple Parasitosen | Strikte Lebensmittelsicherheit, Untersuchung nach Rückkehr |
| Landwirtschaftliche Arbeiter, Tierärzte | Bodenparasiten | Jährliches Screening, persönliche Schutzausrüstung |
| Schwangere Frauen | Behandlungseinschränkungen | Präventionsplanung unter Berücksichtigung des Trimesters |
Einige Anthelminthika sind im ersten Schwangerschaftstrimester kontraindiziert, daher werden Prävention und Behandlung mit dem Geburtshelfer unter Berücksichtigung potenzieller Risiken für den Fötus abgestimmt.

Knowledge Access Protocol
FAQ
Häufig gestellte Fragen
Darmparasiten werden in zwei Hauptgruppen unterteilt: Helminthen (Würmer) und Protozoen (einzellige Organismen). Zu den Helminthen gehören Spulwürmer, Madenwürmer, Bandwürmer und Saugwürmer, zu den Protozoen zählen Giardien und Amöben. Studien zufolge beeinflussen diese Parasiten das Darmmikrobiom auf unterschiedliche Weise (S1).
Parasiten verändern die Vielfalt und Zusammensetzung der Darmmikrobiota erheblich. Forschungsergebnisse zeigen eine Korrelation zwischen dem Vorhandensein von Helminthen und Veränderungen der bakteriellen Darmzusammensetzung (S1). Diese Veränderungen können Verdauung, Immunsystem und allgemeinen Gesundheitszustand beeinflussen.
Typische Symptome umfassen chronische Müdigkeit, Verdauungsstörungen, Anämie und Hautprobleme. Auch allergische Reaktionen, geschwächte Immunabwehr und Nährstoffmangel durch gestörte Resorption können auftreten. Wichtig ist zu verstehen, dass diese Symptome unspezifisch sind und eine labordiagnostische Bestätigung erfordern.
Nein, Parasiten sind keine direkte Ursache für Depressionen. Chronische parasitäre Infektionen können zur Entwicklung von Entzündungen beitragen und die Stimmung beeinflussen, aber Depression ist eine multifaktorielle Erkrankung. Behauptungen über Parasiten als Hauptursache psychischer Störungen sind wissenschaftlich nicht belegt.
Nein, prophylaktische Behandlungen ohne Diagnose werden in Regionen mit niedriger Parasitenprävalenz nicht empfohlen. Antiparasitäre Medikamente haben Nebenwirkungen und sollten nur bei bestätigter Infektion verschrieben werden. Regelmäßige „Reinigungen
Die Hauptmethode ist die Stuhluntersuchung auf Wurmeier und Protozoenzysten, oft ist eine dreifache Untersuchung erforderlich. Zusätzlich können Blutuntersuchungen auf Antikörper, Abstriche auf Enterobiasis und serologische Tests angeordnet werden. Die Methodenwahl hängt vom klinischen Bild und dem vermuteten Parasitentyp ab (S1, S2).
Die Behandlung muss unter ärztlicher Kontrolle mit spezifischen antiparasitären Medikamenten erfolgen. Die Medikamentenwahl hängt vom Parasitentyp ab: Für Helminthen werden Albendazol oder Mebendazol eingesetzt, für Protozoen Metronidazol. Nach der Behandlung ist die Wiederherstellung des Mikrobioms durch Probiotika und richtige Ernährung wichtig.
Das größte Risiko haben Menschen mit geschwächtem Immunsystem, einschließlich Krebspatienten, Kinder und ältere Menschen. Zur Risikogruppe gehören auch Reisende in endemische Regionen sowie Personen, die mit Erde oder Tieren arbeiten. Studien zeigen erhöhte Anfälligkeit bei Patienten mit Immunsuppression (S2).
Ja, einige Parasiten werden von Tieren auf Menschen übertragen (Zoonosen). Toxokariasis von Hunden und Katzen sowie Echinokokkose von Hunden sind Beispiele solcher Infektionen. Regelmäßige Entwurmung von Haustieren, Einhaltung der Hygiene nach Tierkontakt und Händewaschen reduzieren das Infektionsrisiko.
Nach antiparasitärer Therapie wird eine Probiotika-Kur mit Lakto- und Bifidobakterien empfohlen. Wichtig ist die Aufnahme fermentierter Lebensmittel, Ballaststoffe und Präbiotika zur Ernährung der nützlichen Mikroflora. Die Wiederherstellung kann je nach Grad der Störung mehrere Wochen bis Monate dauern (S1).
Nein, das ist ein Mythos. Parasiten können durch chronische Entzündungen und allergische Reaktionen zu Hauterscheinungen beitragen, sind aber nicht die einzige Ursache dermatologischer Erkrankungen. Die meisten Hautprobleme haben andere Ursachen: Genetik, Allergien, Autoimmunprozesse oder Infektionen.
Wichtigste Maßnahmen sind gründliches Händewaschen, thermische Behandlung von Fleisch und Fisch sowie das Waschen von Obst und Gemüse. Wichtig ist, nur gereinigtes Wasser zu trinken, besonders auf Reisen, und sanitäre Standards einzuhalten. Diese einfachen Regeln reduzieren das Infektionsrisiko mit Parasiten erheblich.
Ja, Parasiten konkurrieren um Nährstoffe und können die Resorption im Darm beeinträchtigen. Dies führt zu Mangel an Eisen, Vitamin B12, Folsäure und anderen Nährstoffen. Chronische parasitäre Infektionen gehen häufig mit Anämie und Hypovitaminosen einher, die eine Korrektur erfordern.
Einige Parasiten erhöhen bei langfristiger Infektion das Risiko für bestimmte Krebsarten. Beispielsweise ist Opisthorchiasis mit Cholangiokarzinom verbunden, Schistosomiasis mit Blasenkrebs. Krebspatienten sind aufgrund geschwächter Immunität auch anfälliger für parasitäre Infektionen (S2).
In Regionen mit unzureichender Wasseraufbereitung ist dies möglich, besonders bei Protozoen (Lamblien, Kryptosporidien). In deutschen Städten mit modernen Wasseraufbereitungssystemen ist das Risiko minimal, bleibt aber in ländlichen Gebieten bestehen. Bei Zweifeln an der Wasserqualität wird Abkochen oder die Verwendung von Filtern empfohlen.
Parasiten modulieren die Immunantwort und unterdrücken sie oft zu ihrem eigenen Überleben. Dies kann zu chronischen Entzündungen, Veränderungen des Th1/Th2-Immungleichgewichts und erhöhter Anfälligkeit für andere Infektionen führen. Studien zeigen komplexe Wechselwirkungen zwischen Parasiten, Mikrobiom und Immunsystem (S1, S2).
