 📡 Bioresonanztherapie
📡 BioresonanztherapieBewertung von Medizintechnologien: Geräte und Diagnostikλ
Spezialisierte Methoden zur Bewertung des klinischen und wirtschaftlichen Nutzens von Medizinprodukten und Diagnostiktechnologien für regulatorische Entscheidungen und Kostenerstattung
Overview
Medizinprodukte und Diagnostik erfordern andere Bewertungsmethoden als Arzneimittel: iterative Innovationen, Lernkurven der Anwender, prozedurale Abhängigkeit und kleine Stichproben schaffen methodologische Herausforderungen für systematische Reviews und klinische Validierung. Regulatorische Anforderungen der EU MDR/IVDR, Technologiebewertung durch NICE und HTA-Jurisdiktionen prägen die Evidenzlandschaft — 🧩 klinische Wirksamkeit wird durch gesundheitsökonomische Analysen und den Nachweis des realen Nutzens für Gesundheitssysteme ergänzt.
🛡️
Laplace-Protokoll: Spezialisierte HTA-Frameworks für Medizinprodukte und Diagnostik berücksichtigen die einzigartigen Eigenschaften der Technologien und gewährleisten eine angemessene Nutzenbewertung bei geringerem Evidenzumfang und dynamischer technologischer Entwicklung.
Reference Protocol
Wissenschaftliche Grundlage
Evidenzbasierter Rahmen für kritische Analyse
Navigation Matrix
Unterabschnitte
[bioresonance]
Bioresonanztherapie
Umfassende Bewertung der Bioresonanztherapie auf Basis systematischer Reviews, klinischer Studien und des wissenschaftlichen Konsenses über methodologische Limitationen
Erkunden
[fake-diagnostics]
Fehldiagnosen
Falschdiagnostik bezeichnet betrügerische medizinische Praktiken, die unwissenschaftliche Methoden, unnötige Verfahren und gefälschte Geräte einsetzen, um Patienten auszubeuten und Profit zu erzielen.
Erkunden
Protocol: Evaluation
Teste Dich
Quiz zu diesem Thema kommt bald
Sector L1
Artikel
Forschungsmaterialien, Essays und tiefe Einblicke in die Mechanismen des kritischen Denkens.
 📡 Bioresonanztherapie
📡 Bioresonanztherapie 📡 Bioresonanztherapie
📡 Bioresonanztherapie 📡 Bioresonanztherapie
📡 Bioresonanztherapie 📡 Bioresonanztherapie
📡 Bioresonanztherapie 🔍 Fehldiagnosen
🔍 Fehldiagnosen 🔍 Fehldiagnosen
🔍 Fehldiagnosen⚡
Vertiefung
Spezifika von HTA für Medizinprodukte: Warum pharmazeutische Methoden hier nicht funktionieren
Die Bewertung von Medizintechnologien (HTA) für Geräte und Diagnostik erfordert grundlegend andere Ansätze als für pharmazeutische Präparate. Medizinprodukte unterliegen iterativen Verbesserungen, sind von den Fähigkeiten des Anwenders abhängig und zeigen einen Lernkurveneffekt – Faktoren, die bei der Bewertung von Arzneimitteln nicht vorhanden sind.
Regulierungsbehörden, einschließlich der NICE-Ausschüsse, erkennen ausdrücklich die Notwendigkeit spezialisierter Bewertungskriterien für Medizinprodukte an, die deren einzigartige Eigenschaften berücksichtigen.
Unterschiede zur pharmazeutischen Technologiebewertung
Traditionelle HTA-Frameworks, die für Arzneimittel entwickelt wurden, berücksichtigen nicht die Verfahrensabhängigkeit von Medizinprodukten. Das Ergebnis wird nicht nur durch die Technologie selbst bestimmt, sondern auch durch die Qualifikation des medizinischen Personals, was eine erhebliche Variabilität der klinischen Ergebnisse erzeugt.
| Parameter | Pharmazeutische Präparate | Medizinprodukte |
|---|---|---|
| Variabilität der Ergebnisse | Minimal (patientenabhängig) | Hoch (anwender- und technikabhängig) |
| Stichprobengrößen in Studien | Groß, standardisiert | Oft kleiner, heterogen |
| Lernkurve | Nicht vorhanden | Kritisch für Dateninterpretation |
| Iterative Verbesserungen | Selten im Lebenszyklus | Kontinuierlich, erfordern Neubewertung |
Systematische Literaturübersichten für Medizinprodukte stoßen auf kleinere Stichprobengrößen, Heterogenität der Interventionen und anwenderabhängige Ergebnisse – Probleme, die für pharmazeutische Studien untypisch sind.
- Gesundheitsökonomische Bewertung von Medizinprodukten
- Erfordert spezifische Ansätze: Budgetauswirkungsanalysen und Kosten-Nutzen-Bewertungen werden kritisch für Erstattungsentscheidungen, wobei die Anforderungen an gesundheitsökonomische Evidenz in verschiedenen Jurisdiktionen zunehmen.
Iterative Innovationen und Lernkurven der Anwender
Medizinprodukte unterliegen kontinuierlichen iterativen Verbesserungen während des Produktlebenszyklus. Zum Zeitpunkt des Abschlusses der Bewertung kann sich die Technologie bereits verändert haben, was eine einzigartige Herausforderung für HTA darstellt.
Der Lernkurveneffekt bedeutet, dass sich die klinischen Ergebnisse verbessern, je mehr Erfahrung das medizinische Personal mit dem Gerät sammelt, was die Interpretation früher klinischer Daten erschwert.
- Adaptive Bewertungsmethoden müssen die Evolution der Technologie und der Anwenderfähigkeiten berücksichtigen
- Innovationen in der medizinischen Versorgung demonstrieren ihren Wert durch klinische Wirksamkeit, ökonomische Auswirkungen und Real-World-Effektivität in der Praxis
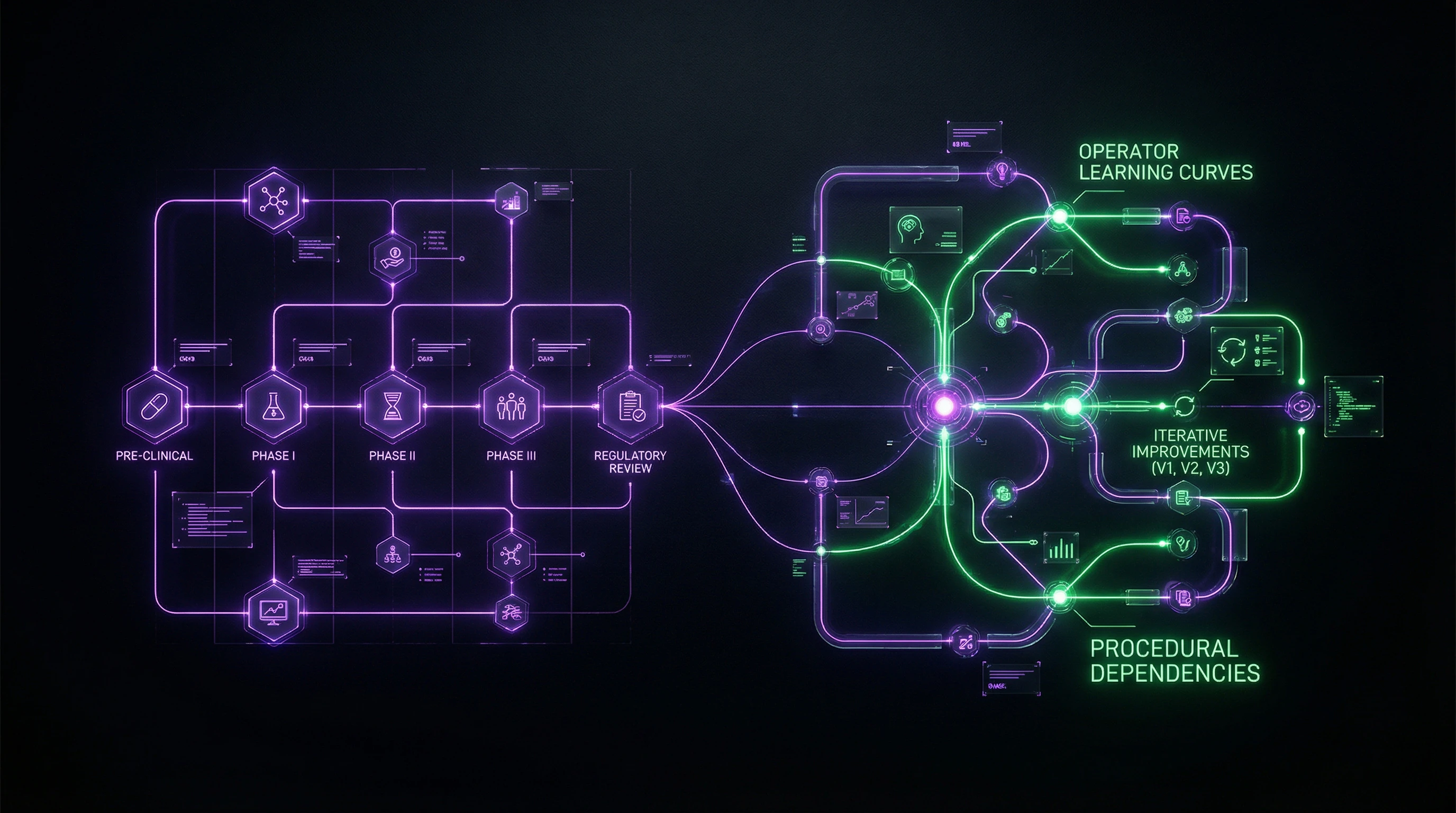
Systematische Literaturübersichten für Medizinprodukte: Anpassung der Methodik an die Datenrealität
Systematische Übersichten für Medizinprodukte und Diagnostik erfordern wesentliche Anpassungen gegenüber pharmazeutischen Methoden. Hauptherausforderungen: kleine Stichprobengrößen, hohe Heterogenität der Interventionen, Abhängigkeit der Ergebnisse von den Fähigkeiten des Anwenders.
Methodische Anpassungen für Medizinprodukte und Diagnostik
Die klinische Validierung von Medizinprodukten ist ein kontinuierlicher Prozess über den gesamten Produktlebenszyklus. Die Methodik muss prozedurale Abhängigkeiten und Lerneffekte berücksichtigen, die die Dateninterpretation beeinflussen.
Die Bewertung der gesundheitsökonomischen Auswirkungen wird für diagnostische Modalitäten obligatorisch. Literaturübersichten müssen nicht nur die klinische Wirksamkeit abdecken, sondern auch Kostenanalysen, Budgetauswirkungen und praktische Anwendbarkeit.
| Schlüsselparameter | Pharmazeutika | Medizinprodukte und Diagnostik |
|---|---|---|
| Stichprobengröße | Große RCTs (Hunderte–Tausende) | Oft klein (Dutzende–Hunderte) |
| Heterogenität | Relativ kontrolliert | Hoch: Modelle, Techniken, Anwendererfahrung |
| Lerneffekt | Minimal | Kritisch für Interpretation |
| Ökonomische Synthese | Zusätzliche Analyse | In Validierung integriert |
Umgang mit heterogenen Daten und kleinen Stichproben
Studien zu Medizinprodukten weisen häufig kleinere Stichprobengrößen auf als pharmazeutische Studien. Dies schafft statistische Herausforderungen für Meta-Analysen und Evidenzsynthese.
Die Abhängigkeit der Ergebnisse vom Anwender fügt eine zusätzliche Ebene der Variabilität hinzu. Qualitative Evidenzsynthese wird kritisch, wenn quantitative Meta-Analysen aufgrund hoher Heterogenität nicht möglich sind.
Datenheterogenität in Medizinproduktstudien ist kein Hindernis, sondern die Norm. Die Methodik muss dies berücksichtigen, nicht ignorieren.
- Bayesianische Ansätze für den Umgang mit kleinen Stichproben anwenden
- Netzwerk-Meta-Analyse-Methoden zur Integration indirekter Vergleiche nutzen
- Qualitative Synthese durchführen, wenn quantitative Analyse begrenzt ist
- Lerneffekte und prozedurale Abhängigkeiten dokumentieren
- Ergebnisse nach Anwendererfahrung und Produktmodell stratifizieren
Klinische Validierung und regulatorische Anforderungen: von EU MDR bis zur Marktüberwachung
EU MDR und IVDR haben die Spielregeln für Medizinprodukte und Diagnostika neu geschrieben. Die Verordnungen etablierten strenge Anforderungen an die Sicherheitsberichterstattung gegenüber Benannten Stellen (Notified Bodies) und schufen ein umfassendes Vigilanzsystem.
Die Marktzulassung ist nicht die Ziellinie, sondern die Startlinie. NICE-Leitlinien und HTA-Bewertungen beeinflussen maßgeblich die praktische Anwendung von Medizinprodukten in der Klinik.
Anforderungen von EU MDR und IVDR an die Evidenzbasis
Die Verordnungen verlangen systematische Berichterstattung über unerwünschte Ereignisse und Sicherheitsvorfälle. Klinische Validierung ist nun kein einmaliges Ereignis mehr, sondern ein kontinuierlicher Prozess zur Sicherstellung von Qualität, Sicherheit und Wirksamkeit über den gesamten Produktlebenszyklus.
| Anforderung | EU MDR | IVDR |
|---|---|---|
| Klinische Nachweise | Entsprechend Risikoklasse; klinische Studien für Hochrisikoprodukte | Strenge Bewertung analytischer und klinischer Validität, insbesondere für kritische Entscheidungen |
| Risikoklassifizierung | Vier Klassen (I–IV) | Vier Kategorien mit verschärften Anforderungen für Diagnostika |
| Marktüberwachung | Verpflichtend für alle Klassen | Verpflichtend; Register aus der Versorgungsrealität erwünscht |
Marktüberwachung und Variabilität der Implementierung
Nach Erhalt der Marktzulassung zeigt sich eine erhebliche Variabilität bei der Technologieadoption. Dieses Phänomen unterstreicht die kritische Rolle der Marktüberwachung und Datenerhebung aus der Versorgungsrealität.
- Organisatorische Barrieren: Inkompatibilität mit bestehender Infrastruktur, Anforderungen an Personalschulung.
- Klinische Integration: Anpassung des Produkts an routinemäßige klinische Pfade und Arbeitsabläufe.
- Ökonomische Faktoren: Kostenerstattung, Budgetrestriktionen, Kosten-Nutzen-Analysen unter Realbedingungen.
- Evidenzgenerierung: Datenerhebung zu Langzeitsicherheit und -wirksamkeit außerhalb kontrollierter Studien.
Die frühe Implementierung medizinischer Innovationen stößt auf Barrieren im Zusammenhang mit Evidenzgenerierung, Kostenerstattung und klinischer Integration. Studien nach Markteinführung und Register aus der Versorgungsrealität werden entscheidend für den Nachweis von Langzeitsicherheit, Wirksamkeit und ökonomischem Wert von Medizinprodukten unter diversen klinischen Bedingungen.
Evidenz für die Implementierung in die Routineversorgung erfordert die Berücksichtigung praktischer Faktoren, die über klinische Studien hinausgehen: organisatorische Barrieren, Personalschulung, Integration in bestehende klinische Pfade.
Gesundheitsökonomische Bewertung diagnostischer Technologien: von klinischer Wirksamkeit zu Budgetauswirkungen
Modelle der ökonomischen Auswirkungen für Diagnostikgeräte
Die Bewertung medizinischer Technologien erfordert den Nachweis eines Nutzens, der über die klinische Wirksamkeit hinausgeht. Gesundheitsökonomische Modelle für Diagnostikgeräte müssen Kaskadeneffekte berücksichtigen: wie Testergebnisse therapeutische Entscheidungen beeinflussen, Behandlungsverläufe verändern und kostspielige Komplikationen verhindern.
Die Analyse der ökonomischen Auswirkungen umfasst drei Komponenten: direkte Testkosten, indirekte Kosten für die nachfolgende Patientenversorgung und potenzielle Einsparungen durch Früherkennung oder Vermeidung ineffektiver Behandlungen.
| Methodischer Ansatz | Wirksamkeitseinheit | Anwendung |
|---|---|---|
| Kosten-Wirksamkeit | Korrekt gestellte Diagnosen, vermiedene Outcomes | Vergleich diagnostischer Technologien |
| Kosten-Nutzen | QALY (qualitätsadjustierte Lebensjahre) | Bewertung der Auswirkungen auf die Lebensqualität des Patienten |
Systematische Literaturübersichten etablieren klinische und ökonomische Evidenz für In-vitro-Diagnostikgeräte. Die Anforderungen an Health Technology Assessment variieren je nach Jurisdiktion, mit wachsender Anerkennung der Notwendigkeit spezialisierter Kriterien für Geräte und Diagnostik.
Budgetauswirkungsanalyse und Preisgestaltung
Die Budgetauswirkungsanalyse ergänzt die Kosten-Wirksamkeits-Analyse um die Perspektive der finanziellen Tragbarkeit für das Gesundheitssystem. Sie bewertet die gesamten finanziellen Konsequenzen der Einführung einer neuen diagnostischen Technologie in einer definierten Population über einen spezifischen Zeithorizont.
- Bestimmen Sie die Nutzungsvolumina der Technologie in der Zielpopulation
- Berechnen Sie direkte Kosten pro Testeinheit und indirekte Kosten für das Ergebnismanagement
- Bewerten Sie die Substitution bestehender Diagnosemethoden und Ressourcenfreisetzung
- Modellieren Sie die finanziellen Auswirkungen auf das Gesundheitssystembudget über 3–5 Jahre
- Verknüpfen Sie die Ergebnisse mit klinischer Evidenz zur Begründung der Preispositionierung
Die Preisgestaltung medizinischer Geräte erfordert eine Balance zwischen Erstattung der Entwicklungskosten, Marktwettbewerbsfähigkeit und Wertnachweis für Kostenträger. Ohne diese Balance ist die Technologie entweder für Patienten unzugänglich oder ökonomisch nicht tragfähig.
Strategische Preisgestaltung verknüpft das Finanzmodell mit klinischer Evidenz und schafft eine Grundlage für Verhandlungen mit Regulierungsbehörden und Gesundheitssystemen.
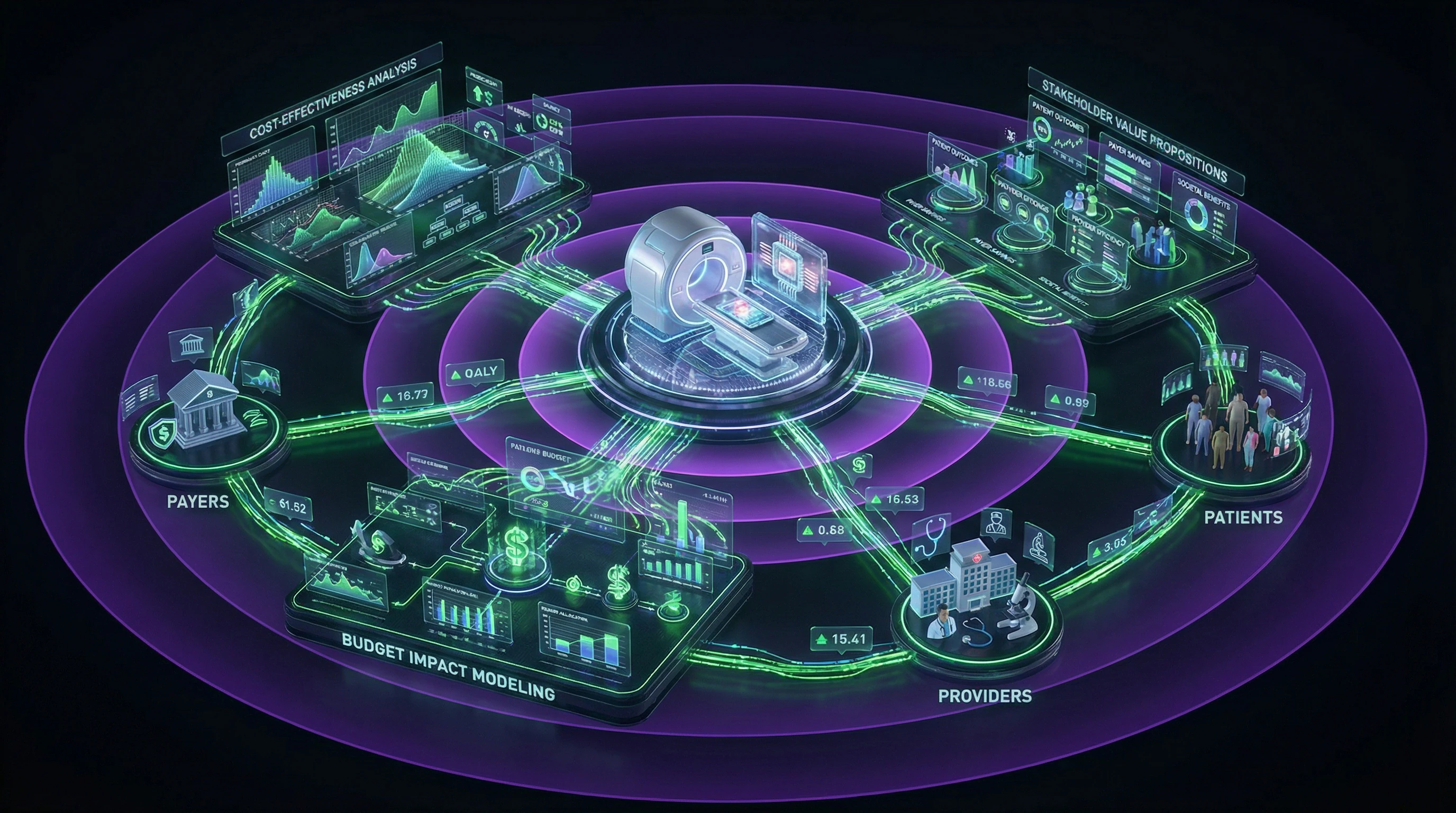
Marktzugangswege und Kostenerstattung: Navigation in der regulatorischen Landschaft
NICE Medical Technologies Guidance und spezialisierte Bewertungswege
Das Medical Technologies Advisory Committee (MTAC) im Rahmen von NICE bestimmt die geeigneten Bewertungswege für Medizinprodukte und Diagnostika. Die Marktzulassung allein garantiert keine Implementierung — NICE-Leitlinien und HTA-Bewertungen beeinflussen die praktische Umsetzung im Gesundheitssystem erheblich.
Die regulatorische Landschaft der EU (MDR und IVDR) hat Anforderungen zur Sicherheitsberichterstattung gegenüber benannten Stellen etabliert. Innovatoren müssen einen Mehrwert nachweisen, der über die klinische Wirksamkeit hinausgeht: ökonomische Auswirkungen und Effektivität unter Realbedingungen.
- Evidenzgenerierung in frühen Entwicklungsphasen beginnen
- HTA-Anforderungen in Zielmärkten untersuchen
- Jurisdiktionsspezifische Bewertungskriterien für Medizinprodukte und Diagnostika präzisieren
- Gesundheitsökonomische Begründung parallel zu klinischen Daten vorbereiten
Implementierungsvariabilität nach regulatorischer Zulassung
Nach Marktzulassung und positiven NICE-Empfehlungen zeigt sich eine erhebliche Variabilität in der Technologieadoption. Die Lücke zwischen regulatorischer Zulassung und breiter klinischer Anwendung entsteht durch Barrieren in der Evidenzgenerierung, Kostenerstattung und klinischen Integration.
Organisatorische Bereitschaft, Verfügbarkeit von Personalschulungen, Kompatibilität mit bestehenden klinischen Pfaden und lokale Budgetbeschränkungen bestimmen Geschwindigkeit und Umfang der Innovationsimplementierung, nicht nur ihr regulatorischer Status.
Erfolgreiche Implementierung erfordert zusätzliche Wertdemonstration und gezielte Unterstützung auf Ebene der Gesundheitsorganisationen. Die Strategie sollte lokale Schulungen, Anpassung an bestehende Arbeitsabläufe und transparente Kostenbegründung für Entscheidungsträger umfassen.
Generierung von Real-World-Evidence: von kontrollierten Studien zur Routineanwendung
Studiendesign für Medizinprodukte und Diagnostik
Klinische Validierung bedeutet nachzuweisen, dass ein Medizinprodukt oder diagnostisches Instrument unter klinischen Bedingungen bestimmungsgemäß funktioniert. Das Studiendesign muss iterative Verbesserungen, Lernkurven der Anwender und die Abhängigkeit der Ergebnisse von prozeduralen Faktoren berücksichtigen.
Systematische Reviews für Medizinprodukte werden an kleinere Stichprobengrößen, Heterogenität der Interventionen und anwenderabhängige Outcomes angepasst. Komplexe diagnostische Szenarien — Koinfektionen, Multiorganschäden — erfordern Metagenomik und Multiplex-Plattformen.
- Evidenz für die Routinepraxis muss organisatorische Barrieren und Personalschulung einbeziehen
- Integration in bestehende klinische Pfade ist ein obligatorisches Validierungskriterium
- Fortgeschrittene Methodologien kompensieren Limitationen traditioneller RCTs
Monitoring der Wirksamkeit in der klinischen Routinepraxis
Post-Market-Studien und Real-World-Register demonstrieren Langzeitsicherheit, Wirksamkeit und ökonomischen Wert unter diversen klinischen Bedingungen. Monitoring-Systeme erfassen Daten zu klinischen Outcomes, Nutzungsmustern, unerwünschten Ereignissen und ökonomischen Kennzahlen.
Die regulatorischen Anforderungen der MDR und IVDR schaffen einen strukturierten Rahmen für systematische Datenerfassung zu Sicherheit und Wirksamkeit unter realen Anwendungsbedingungen — das ist keine Bürokratie, sondern ein Feedback-Mechanismus für iterative Verbesserung.
Die Integration von Real-World-Daten mit traditionellen klinischen Studien erzeugt ein vollständiges Bild von Wirksamkeit und Sicherheit. Machine Learning und künstliche Intelligenz identifizieren Muster, die unter kontrollierten Bedingungen nicht offensichtlich sind.
| Evidenzquelle | Vorteile | Limitationen |
|---|---|---|
| Kontrollierte RCTs | Hohe interne Validität, Minimierung von Bias | Enge Einschlusskriterien, artifizielle Bedingungen |
| Real-World-Register | Repräsentativität, Langzeitdaten, Patientendiversität | Confounding, unvollständige Daten, Selektionsbias |
| Big-Data-Analyse + ML | Identifikation verborgener Muster, Skalierbarkeit | Validierung erforderlich, Overfitting-Risiko |

Knowledge Access Protocol
FAQ
Häufig gestellte Fragen
Medizinprodukte erfordern spezialisierte HTA-Ansätze, die sich von pharmazeutischen unterscheiden. Wesentliche Unterschiede umfassen iterative Designverbesserungen, Abhängigkeit von Anwenderfähigkeiten, Lernkurven und prozedurale Faktoren, die bei Arzneimitteln nicht auftreten. Standardmethoden zur Arzneimittelbewertung berücksichtigen diese Besonderheiten von Medizinprodukten und Diagnostika nicht.
Es handelt sich um einen methodischen Prozess zur Sammlung, kritischen Bewertung und Synthese klinischer und ökonomischer Daten zu Medizintechnologien. Reviews sind notwendig, um die Evidenzbasis für IVD-Produkte und andere Medizintechnologien zu etablieren. Die Methodik wird an die Spezifika von Medizinprodukten und die Heterogenität verfügbarer Daten angepasst.
In der EU gelten die Verordnungen MDR (für Medizinprodukte) und IVDR (für In-vitro-Diagnostika). Sie legen Anforderungen zur Sicherheitsberichterstattung gegenüber benannten Stellen und zur klinischen Validierung fest. Diese Verordnungen gewährleisten die Marktüberwachung über den gesamten Produktlebenszyklus.
Nein, die regulatorische Zulassung garantiert keinen Markterfolg. Nach Erhalt der Genehmigung und NICE-Empfehlungen zeigt sich erhebliche Variabilität bei Implementierung und Verbreitung von Technologien. Es bedarf zusätzlicher Wertdemonstration, ökonomischer Nachweise und Unterstützung der praktischen Implementierung für echten Erfolg.
Die Bewertung umfasst die Analyse der ökonomischen Auswirkungen auf das Gesundheitssystem und Budgetfolgenabschätzungen. Für diagnostische Technologien werden spezialisierte Modelle entwickelt, die Änderungen in klinischen Pfaden, diagnostische Genauigkeit und nachfolgende therapeutische Entscheidungen berücksichtigen. Kosten- und Preisanalysen sind für die HTA-Bewertung entscheidend.
Es ist der Prozess zur Bestätigung, dass ein Produkt unter klinischen Bedingungen bestimmungsgemäß funktioniert. Die Validierung gewährleistet Qualität, Sicherheit und Wirksamkeit der Technologie. Es handelt sich um einen kontinuierlichen Prozess über den gesamten Produktlebenszyklus, besonders wichtig für iterativ weiterentwickelte Produkte.
NICE bewertet das Wertversprechen von Medizintechnologien durch den spezialisierten Ausschuss MTAC und legt Bewertungswege fest. NICE-Empfehlungen beeinflussen die Implementierung von Technologien im NHS und dienen als Orientierung für Beschaffungen. Eine positive NICE-Bewertung erhöht die Chancen auf breite Anwendung des Produkts erheblich.
Die Variabilität der Implementierung hängt mit Barrieren bei Evidenzgenerierung, Kostenerstattung und klinischer Integration zusammen. Selbst nach Zulassung und positiven Empfehlungen benötigt es Zeit für Personalschulung, Prozessanpassung und Demonstration realer Wirksamkeit. Lokale Faktoren und Ressourcen beeinflussen ebenfalls die Implementierungsgeschwindigkeit.
Es bedarf spezieller Studiendesigns, die praktische Faktoren jenseits klinischer Studien berücksichtigen. Notwendig ist das Monitoring der Wirksamkeit in der Routineversorgung unter Berücksichtigung von Lernkurven, Anwendervariabilität und Anwendungsbedingungen. Post-Market-Register und Beobachtungsstudien ergänzen RCT-Daten.
Das ist ein Mythos – die ökonomische Bewertung ist für Medizinprodukte und Diagnostika entscheidend. Innovatoren müssen nicht nur klinische Wirksamkeit, sondern auch ökonomische Auswirkungen nachweisen. HTA-Anforderungen steigen in allen Jurisdiktionen, und ohne gesundheitsökonomische Begründung ist eine Kostenerstattung unwahrscheinlich.
Nein, diagnostische Technologien erfordern spezifische Bewertungsmethoden. Es müssen Auswirkungen auf klinische Entscheidungen, Änderungen in therapeutischen Pfaden und Kaskadeneffekte der diagnostischen Genauigkeit berücksichtigt werden. Die direkte Übertragung von Bewertungsmethoden für Arzneimittel ignoriert die einzigartigen Eigenschaften diagnostischer Technologien und führt zu unvollständigen Bewertungen.
IVD (in vitro diagnostic) sind Medizinprodukte zur Analyse von Biomaterialproben (Blut, Gewebe, Urin) außerhalb des Körpers. Sie erfordern systematische Literaturübersichten zur Etablierung der klinischen Evidenzbasis und unterliegen der IVDR-Verordnung in der EU. Die Bewertung umfasst analytische und klinische Validierung sowie Wirtschaftlichkeitsanalysen.
Kontinuierliche Verbesserungen der Gerätekonstruktion stellen eine Herausforderung für traditionelle HTA-Methoden dar, die für statische Technologien konzipiert sind. Es werden adaptive Bewertungsansätze benötigt, die die Evolution des Geräts und die Akkumulation von Daten berücksichtigen. Die klinische Validierung wird zu einem kontinuierlichen Prozess und nicht zu einem einmaligen Ereignis vor der Markteinführung.
Hauptbarrieren umfassen mangelnde Evidenzbasis in frühen Phasen, Unsicherheit bei der Kostenerstattung und Schwierigkeiten bei der klinischen Integration. Frühe Innovatoren stehen vor der Anforderung, Daten unter Bedingungen begrenzter Anwendungserfahrung zu generieren. Regulatorische und HTA-Prozesse sind oft nicht für die Bewertung disruptiver Technologien mit limitierten Daten angepasst.
Metagenomik stellt eine fortschrittliche Lösung für die Identifizierung komplexer diagnostischer Szenarien mit multiplen Pathogenen dar. Die Technologie ermöglicht die gleichzeitige Identifizierung verschiedener Erreger ohne vorherige Hypothesen. Für die Implementierung metagenomischer Diagnostik werden neue Methoden der klinischen und ökonomischen Bewertung benötigt, die die Komplexität der Ergebnisinterpretation berücksichtigen.
Post-Market-Surveillance gewährleistet kontinuierliches Monitoring von Sicherheit und Wirksamkeit unter realen Anwendungsbedingungen. Die MDR- und IVDR-Verordnungen erfordern systematische Berichterstattung über unerwünschte Ereignisse und Qualitätsprobleme. Dies ermöglicht die Identifizierung seltener Komplikationen, die Bewertung langfristiger Ergebnisse und die Anpassung von Anwendungsempfehlungen basierend auf akkumulierter Erfahrung.
