 🧠 Neurowissenschaften
🧠 NeurowissenschaftenNeurowissenschaften: Erforschung von Gehirn und Nervensystemλ
Interdisziplinäre Wissenschaft, die Struktur, Funktion und Entwicklung des Nervensystems erforscht – von molekularen Mechanismen bis hin zu menschlichem Verhalten und Kognition.
Overview
Neurowissenschaft vereint Biologie, Physik, Chemie und Informatik, um die 🧠 Funktionsweise des Gehirns zu entschlüsseln — von molekularen Mechanismen bis zum Bewusstsein. Moderne Technologien (fMRT, PET-Scanning) ermöglichen die Beobachtung neuronaler Netzwerkaktivität in Echtzeit und das Verständnis, wie Gedächtnis, Emotionen und Entscheidungen entstehen. Die Erkenntnisse finden Anwendung in Medizin, Bildung, KI-Entwicklung und kognitiver Therapie.
🛡️
Laplace-Protokoll: Neurowissenschaft basiert auf strengen experimentellen Methoden und reproduzierbaren Ergebnissen, die wissenschaftlich fundiertes Wissen über das Gehirn von populären Mythen und pseudowissenschaftlichen Behauptungen über seine Funktionsweise trennen.
Reference Protocol
Wissenschaftliche Grundlage
Evidenzbasierter Rahmen für kritische Analyse
Protocol: Evaluation
Teste Dich
Quiz zu diesem Thema kommt bald
Sector L1
Artikel
Forschungsmaterialien, Essays und tiefe Einblicke in die Mechanismen des kritischen Denkens.
 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften 🧠 Neurowissenschaften
🧠 Neurowissenschaften⚡
Vertiefung
Architektur des Nervensystems: von molekularen Maschinen zu globalen Netzwerken
Das Nervensystem ist eine hierarchische Struktur, in der Milliarden spezialisierter Zellen alle Prozesse des Organismus koordinieren – von automatischen Reflexen bis zum abstrakten Denken. Neuronen übertragen Informationen über Distanzen von Mikrometern bis zu Metern mit Geschwindigkeiten bis zu 120 m/s dank ihrer einzigartigen Morphologie und elektrochemischen Eigenschaften.
Das menschliche Gehirn enthält etwa 86 Milliarden Neuronen, von denen jedes durchschnittlich 7000 synaptische Kontakte bildet. Dieses Netzwerk bildet die Grundlage für alle kognitiven Prozesse.
Neuronen und synaptische Übertragung: molekulare Logik der Kommunikation
Ein Neuron besteht aus dem Soma (Zellkörper), Dendriten (Signalempfang) und dem Axon (Übertragung). Information wird durch Aktionspotenziale kodiert – stereotypische elektrische Impulse mit einer Amplitude von etwa 100 mV und einer Dauer von 1–2 ms, die bei Depolarisation der Membran über den Schwellenwert von −55 mV entstehen.
Die Generierung des Aktionspotenzials wird durch kaskadenartiges Öffnen spannungsabhängiger Natriumkanäle gewährleistet, die bis zu 10⁷ Na⁺-Ionen pro Sekunde durch einen Kanal leiten. Die Myelinscheide erhöht die Leitungsgeschwindigkeit um das 5- bis 50-fache durch den saltatorischen Mechanismus – die sprunghafte Ausbreitung der Erregung zwischen den Ranvier-Schnürringen.
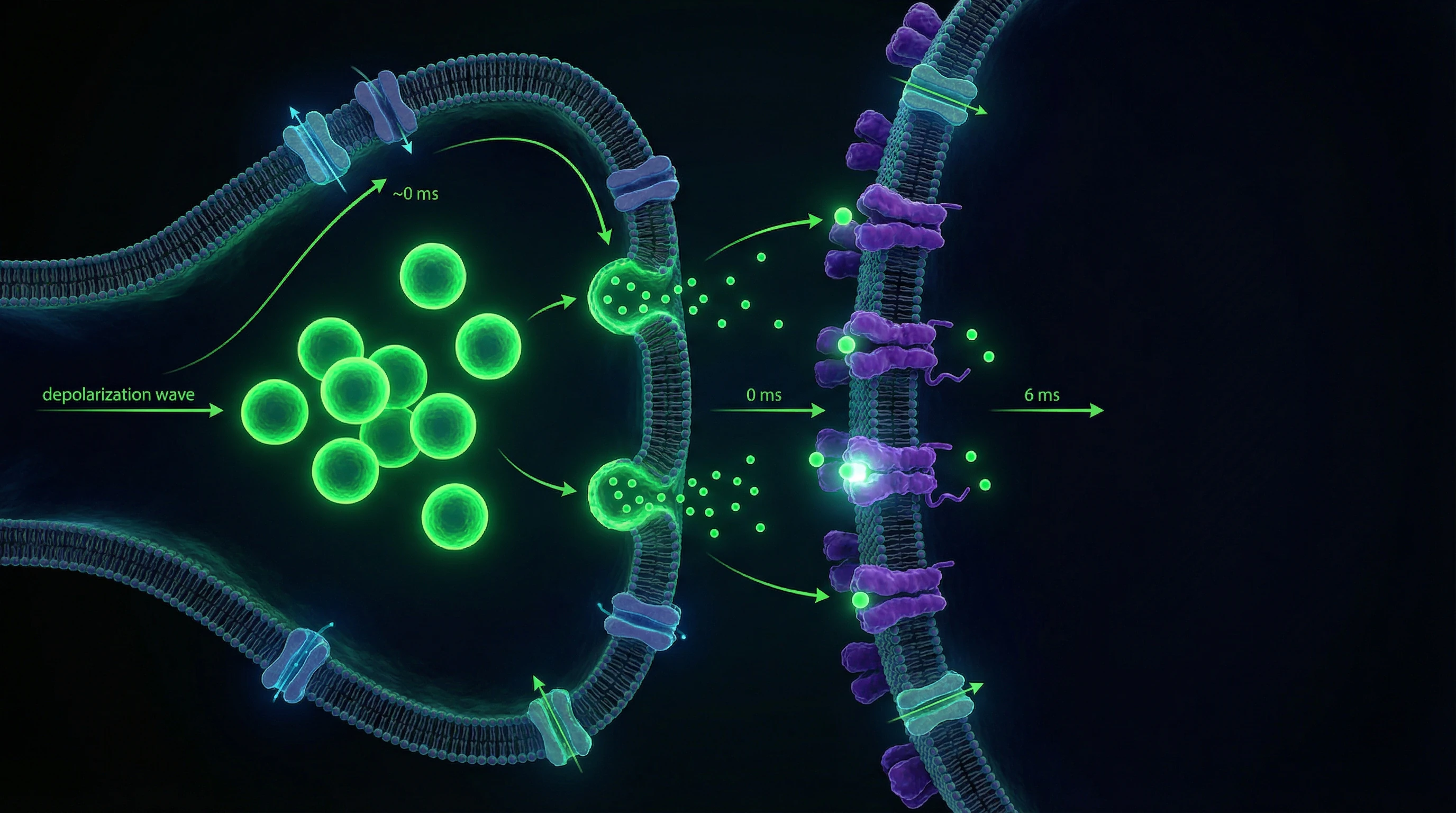
Die synaptische Übertragung erfolgt überwiegend chemisch durch Freisetzung von Neurotransmittern in den synaptischen Spalt mit einer Breite von 20–40 nm. Das Eintreffen des Aktionspotenzials an der präsynaptischen Endigung öffnet spannungsabhängige Calciumkanäle; der Ca²⁺-Einstrom löst die Exozytose synaptischer Vesikel innerhalb von 0,2–0,5 ms aus.
- Transmitterquantum
- Inhalt eines synaptischen Vesikels; eine typische Synapse setzt 1–5 Quanten pro Impuls mit einer Wahrscheinlichkeit von 0,1–0,9 frei.
- Glutamat
- Wichtigster exzitatorischer Transmitter (80–90% der ZNS-Synapsen); sein Gleichgewicht mit GABA bestimmt die Erregbarkeit neuronaler Netzwerke.
- GABA
- Wichtigster inhibitorischer Transmitter (10–20% der Synapsen); entscheidend zur Verhinderung von Hyperexzitabilität.
Zentrales und peripheres Nervensystem: funktionelle Arbeitsteilung
Das ZNS umfasst das Gehirn (Masse 1300–1400 g) und das Rückenmark (Länge 40–45 cm, 31 Segmente), geschützt durch knöcherne Strukturen und drei Hirnhäute. Die Großhirnrinde enthält 16–20 Milliarden Neuronen, organisiert in sechs Schichten mit einer Dicke von 1,5–4,5 mm; die Gesamtfläche der Rinde beträgt bei Glättung 1800–2300 cm².
| Struktur | Funktion | Mechanismus |
|---|---|---|
| Basalganglien | Bewegungskontrolle | Auswahl und Initiierung motorischer Programme |
| Hippocampus | Gedächtniskonsolidierung | Kodierung episodischer Ereignisse |
| Amygdala | Emotionale Reaktionen | Bewertung von Bedrohung und Belohnung |
| Rückenmark | Reflexe und Motorik | Latenz 30–50 ms über 31 Nervenpaare |
Das PNS besteht aus 12 Hirnnervenpaaren und 31 Spinalnervenpaaren und gliedert sich in das somatische System (willkürliche Kontrolle der Skelettmuskulatur) und das autonome System (unwillkürliche Regulation innerer Organe).
- Sympathikus (Noradrenalin): „Kampf-oder-Flucht"-Reaktion – erhöht die Herzfrequenz von 60–80 auf 120–180 Schläge/min, verteilt Blutfluss zu den Muskeln (bis zu 80% des Herzzeitvolumens), mobilisiert Energiereserven.
- Parasympathikus (Acetylcholin): „Ruhe-und-Verdauung"-Modus – stimuliert die Verdauung, senkt die Herzfrequenz, aktiviert anabole Prozesse.
- Enterisches Nervensystem: 200–600 Millionen Neuronen im Darm funktionieren autonom und interagieren bidirektional mit dem ZNS über den Vagusnerv.
Methoden der Hirnforschung: von Elektroden bis zu molekularen Markern
Die moderne Neurowissenschaft nutzt einen multimodalen Ansatz, der Methoden mit unterschiedlicher räumlicher (von Nanometern bis Zentimetern) und zeitlicher (von Mikrosekunden bis Jahren) Auflösung kombiniert. Durchbrüche der letzten Jahrzehnte — funktionelle MRT (1990er), Optogenetik (2005), Zwei-Photonen-Mikroskopie in vivo (2000er), Konnektomik (2010er) — ermöglichten den Übergang von korrelativen Beobachtungen zur kausalen Analyse neuronaler Mechanismen.
Die Integration von Daten verschiedener Maßstäbe durch computergestützte Modellierung schafft mehrstufige Hirnkarten von Molekülen bis zum Verhalten.
Neuroimaging und Elektrophysiologie: Beobachtung des lebenden Gehirns
Die funktionelle MRT (fMRT) detektiert Veränderungen des Blutflusses über das BOLD-Signal (blood oxygen level dependent) mit einer räumlichen Auflösung von 1–3 mm und einer zeitlichen von 1–2 s, was eine nichtinvasive Kartierung der Aktivität des gesamten Gehirns ermöglicht. Die Aktivierung von Neuronen erhöht den lokalen Blutfluss um 20–40% mit einer Verzögerung von 4–6 s, was den Sauerstoffbedarf übersteigt (neurovaskuläre Kopplung) und einen Kontrast zwischen aktiven und inaktiven Zonen erzeugt.
Die Positronen-Emissions-Tomographie (PET) verwendet radioaktive Tracer zur Visualisierung des Glukosestoffwechsels (¹⁸F-FDG), von Neurotransmittersystemen (¹¹C-Racloprid für Dopamin), von Amyloid-Plaques bei Alzheimer-Krankheit mit einer Empfindlichkeit bis zu pikomolaren Konzentrationen.
| Methode | Räumliche Auflösung | Zeitliche Auflösung | Vorteil |
|---|---|---|---|
| fMRT | 1–3 mm | 1–2 s | Gesamtes Gehirn, nichtinvasiv |
| PET | 2–4 mm | Minuten | Molekulare Marker (Stoffwechsel, Rezeptoren) |
| MEG | 2–5 mm | 1 ms | Hohe zeitliche Auflösung, nichtinvasiv |
| EEG | 5–10 cm | 1 ms | Portabilität, geringe Kosten |
Die Magnetenzephalographie (MEG) registriert Magnetfelder von 10–100 Femtotesla, die durch synchrone Aktivität von 10⁴–10⁵ Neuronen erzeugt werden, mit einer zeitlichen Auflösung von 1 ms und einer Lokalisierung der Quellen mit einer Genauigkeit von 2–5 mm.
Die Elektroenzephalographie (EEG) misst die summierte elektrische Aktivität über 19–256 Elektroden auf der Kopfhaut und erfasst Rhythmen: Delta (0,5–4 Hz, Tiefschlaf), Theta (4–8 Hz, Meditation), Alpha (8–13 Hz, entspanntes Wachsein), Beta (13–30 Hz, aktives Denken), Gamma (30–100 Hz, kognitive Integration).
Die Patch-Clamp-Technik erreicht eine Auflösung einzelner Ionenkanäle (Leitfähigkeit 1–100 Pikosiemens) und ermöglicht die Analyse synaptischer Ströme mit einer Amplitude von 5–50 pA mit Mikrosekundengenauigkeit — dies ist die Grenze zwischen Makroskopie und molekularer Physik.
Multikanal-Elektrodenmatrizen (bis zu 1024 Kanäle) registrieren die Aktivität von Hunderten von Neuronen gleichzeitig in vivo und enthüllen Muster der Populationskodierung und neuronale Ensembles, die mit Verhalten korrelieren.
Molekulare und genetische Ansätze: Manipulation neuronaler Schaltkreise
Die Optogenetik nutzt lichtempfindliche Proteine (Channelrhodopsin-2 wird durch blaues Licht bei 470 nm aktiviert, Halorhodopsin durch gelbes bei 580 nm) zur Kontrolle der Aktivität genetisch definierter Neuronenpopulationen mit Millisekundengenauigkeit. Die Expression von Opsinen unter Promotoren spezifischer Gene (z. B. CaMKIIα für exzitatorische Neuronen, GAD67 für inhibitorische) ermöglicht die selektive Aktivierung oder Hemmung von Zelltypen und beweist ihre kausale Rolle im Verhalten.
Die Chemogenetik (DREADD — designer receptors exclusively activated by designer drugs) bietet pharmakologische Kontrolle neuronaler Aktivität: der synthetische Ligand Clozapin-N-Oxid (CNO, 1–10 mg/kg) aktiviert inerte Rezeptoren und moduliert die Aktivität der Zielneuronen über Stunden. Virale Vektoren (AAV, Lentivirus) liefern genetische Konstrukte mit einer Transduktionseffizienz von 60–90% in ein Zielgebiet mit einem Volumen von 0,5–2 mm³.
- Optogenetik: Licht → Opsin → Ionenkanal → Neuron aktiv/inaktiv (Millisekunden)
- Chemogenetik: CNO → synthetischer Rezeptor → Modulation der Aktivität (Stunden)
- CRISPR/Cas9: Genombearbeitung → Gen-Knockout → Krankheitsmodellierung (dauerhaft)
- Virale Vektoren: Lieferung des Konstrukts in das Zielgebiet (60–90% Effizienz)
Die CRISPR/Cas9-Genombearbeitung ermöglicht die Erzeugung von Knockouts spezifischer Gene in Neuronen mit einer Effizienz von 40–80% und modelliert genetische Varianten, die mit neurologischen Erkrankungen assoziiert sind.
Die Einzelzell-Transkriptomik (scRNA-seq) hat mehr als 100 molekular unterschiedliche Neuronentypen in der Hirnrinde identifiziert, jeder mit einem einzigartigen Expressionsprofil von 15.000–20.000 Genen, was die Klassifizierung von Hirnzellen neu definiert.
Die Konnektomik rekonstruiert vollständige Karten synaptischer Verbindungen: das Konnektom von C. elegans (302 Neuronen, 7.000 Synapsen) wurde 1986 fertiggestellt, ein kortikaler Würfel von 1 mm³ der Maus (100.000 Neuronen, 10⁹ Synapsen) im Jahr 2021 unter Verwendung serieller Elektronenmikroskopie und maschinellen Lernens. Dies ist der Übergang von der Beschreibung zur vollständigen Topographie.
Die Kalzium-Bildgebung mit GCaMP6-Indikatoren (ΔF/F bis zu 1000% bei Aktivität) ermöglicht die Registrierung der Aktivität von 1.000–10.000 Neuronen gleichzeitig in vivo über implantierte Mikroskope (1–2 g) oder Zwei-Photonen-Mikroskopie durch ein Schädelfenster.
Kognitive Neurowissenschaft: Neuronale Codes des Geistes
Die kognitive Neurowissenschaft untersucht die neuronalen Mechanismen höherer psychischer Funktionen — Wahrnehmung, Aufmerksamkeit, Gedächtnis, Sprache, Entscheidungsfindung, Bewusstsein. Das Schlüsselkonzept ist die neuronale Kodierung: Information wird durch Aktivitätsmuster von Neuronenpopulationen repräsentiert, wobei die Bedeutung nicht durch einzelne Zellen, sondern durch die verteilte Aktivität von Ensembles aus 10²-10⁴ Neuronen bestimmt wird.
Die zeitliche Dynamik ist nicht weniger wichtig als die Feuerrate: Information wird im präzisen Timing der Spikes relativ zum Theta-Rhythmus (4-8 Hz) des Hippocampus mit einer Genauigkeit von 10-20 ms kodiert.
Mechanismen von Gedächtnis und Lernen: Von Synapsen zu Systemen
Langzeitpotenzierung (LTP) — eine anhaltende Verstärkung der synaptischen Übertragung um 100-400% nach hochfrequenter Stimulation (100 Hz, 1 s) — gilt als zellulärer Mechanismus des Gedächtnisses. LTP im Hippocampus erfordert die Aktivierung von NMDA-Rezeptoren, die Ca²⁺ nur bei gleichzeitiger Depolarisation und Glutamatbindung durchlassen (Hebb'scher Koinzidenzdetektor).
Aktivierungskaskade: CaMKII → Phosphorylierung von AMPA-Rezeptoren → Erhöhung ihrer Anzahl in der Synapse (von 20 auf 80 Rezeptoren innerhalb von 15-30 min). Die späte Phase der LTP (L-LTP, >3 h) erfordert de novo Proteinsynthese durch Aktivierung CREB-abhängiger Transkription, vergrößert dendritische Dornen um 30-60% und stabilisiert Veränderungen über Tage bis Monate.
| Prozess | Stimulation | Effekt | Funktion |
|---|---|---|---|
| LTP | 100 Hz, 1 s | Verstärkung um 100-400% | Lernen, Einprägen |
| LTD | 1 Hz, 15 min | Abschwächung um 30-50% | Vergessen, Verfeinerung |
Langzeitdepression (LTD) — der entgegengesetzte Prozess der Synapsenschwächung bei niederfrequenter Stimulation — ermöglicht Vergessen und Verfeinerung neuronaler Schaltkreise.
Gedächtniskonsolidierung überträgt Information vom Hippocampus zum Neokortex über Wochen bis Monate durch Reaktivierung neuronaler Muster während des Schlafs. Während des Tiefschlafs reproduzieren hippocampale „Replays" Tagesaktivitätssequenzen in komprimierter Zeit (Kompression um Faktor 6-20), synchronisiert mit kortikalen Spindeln (12-15 Hz, 0,5-2 s) für den Informationstransfer.
Schlafstörungen in den ersten 6 h nach dem Lernen reduzieren die Konsolidierung um 30-50%, während optogenetische Verstärkung der Reaktivierung das Gedächtnis um 20-40% verbessert.
Das Arbeitsgedächtnis hält 4±1 Elemente im präfrontalen Kortex durch anhaltende neuronale Aktivität (10-30 Hz) während Verzögerungen von Sekunden bis Minuten, moduliert durch Dopamin (Optimum bei moderaten Spiegeln, invertierte U-Kurve). Das episodische Gedächtnis wird durch „Ortszellen" des Hippocampus (aktiv in spezifischen Lokationen, Feld 20-50 cm) und „Zeitzellen" (kodieren Zeitintervalle von 1-30 s) kodiert und bildet eine kognitive Karte von Raum und Zeit.
Neuronale Grundlagen des Bewusstseins: Integration und globaler Arbeitsraum
Die Theorie des globalen neuronalen Arbeitsraums (Dehaene, Changeux) postuliert, dass bewusste Wahrnehmung entsteht, wenn ein verteiltes Netzwerk aus präfrontalen, parietalen und temporalen Arealen „entzündet" wird und Information über weitreichende kortiko-kortikale Verbindungen überträgt. Bewusste Stimuli erzeugen späte Aktivität (>300 ms) mit globaler Synchronisation im Gamma-Bereich (30-80 Hz).
Unterschwellige Stimuli generieren nur lokale frühe Aktivität (<200 ms) ohne Ausbreitung. Schädigungen des präfrontalen Kortex oder thalamischer Kerne (intralaminare Kerne) beeinträchtigen das Bewusstsein und bestätigen ihre Rolle in der globalen Integration.
- Bewusster Stimulus → späte globale Entzündung (>300 ms)
- Unterschwelliger Stimulus → lokale frühe Aktivität (<200 ms)
- Schädigung des präfrontalen Kortex → Integrationsstörung
- Schädigung thalamischer Kerne → Bewusstseinsverlust
Die Theorie der integrierten Information (Tononi) definiert Bewusstsein quantitativ durch Φ (Phi) — ein Maß für die kausale Integration eines Systems: Hohes Φ erfordert ein Gleichgewicht zwischen funktionaler Spezialisierung der Module und ihrer Integration, maximiert im thalamo-kortikalen System.
Neuronale Korrelate des Bewusstseins (NCC) — minimale neuronale Mechanismen, die für eine spezifische bewusste Erfahrung ausreichen — sind in posterioren kortikalen „Hot Zones" lokalisiert: extrastriärer visueller Kortex (V2-V4) für visuelles Bewusstsein, temporo-parietaler Kortex für körperliches Selbstbewusstsein.
Binokulare Rivalität zeigt, dass V1-Aktivität mit dem physischen Stimulus korreliert, während V4 und inferotemporaler Kortex mit der subjektiven Wahrnehmung korrelieren, was V4 als kritische Zone für visuelles Bewusstsein ausweist.
Anästhetika (Propofol, Sevofluran) unterdrücken das Bewusstsein, indem sie thalamo-kortikale Konnektivität stören und die EEG-Komplexität reduzieren (Perturbational Complexity Index PCI von 0,5 im Wachzustand auf 0,2 unter Anästhesie), ohne lokale Aktivität zu beeinträchtigen.
Der vegetative Zustand ist durch erhaltene metabolische Aktivität (50-60% der Norm laut PET) gekennzeichnet, aber fragmentierte funktionale Konnektivität, während der Zustand minimalen Bewusstseins teilweise Wiederherstellung weitreichender Verbindungen und Reaktionen auf Befehle in 20-40% der Fälle zeigt.
Neuroplastizität und Entwicklung — Wie sich das Gehirn im Laufe des Lebens umstrukturiert
Bildung neuronaler Verbindungen durch Synaptogenese und Pruning
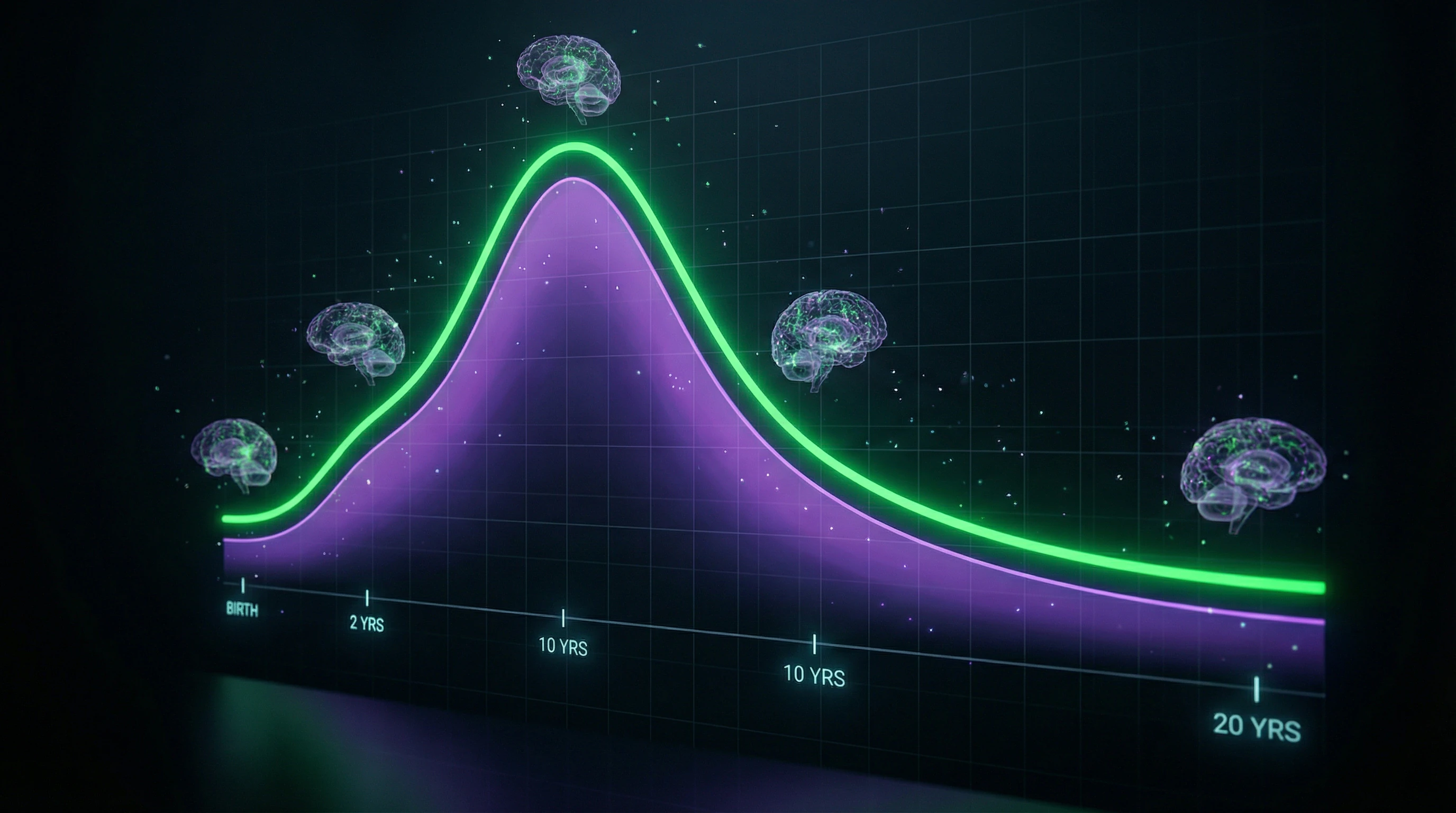
Die Synaptogenese erreicht in verschiedenen Bereichen zu unterschiedlichen Zeitpunkten ihren Höhepunkt: visueller Kortex — 3–4 Monate (Synapsendichte bis zu 150% des Erwachsenenniveaus), präfrontaler Kortex — 1–2 Jahre, mit anschließendem Pruning, das bis zum Jugendalter bis zu 40% der Synapsen entfernt.
Der Mechanismus ist aktivitätsabhängig: häufig genutzte Synapsen werden durch Expression von BDNF und TrkB-Rezeptoren stabilisiert, inaktive werden durch Komplement C1q markiert und von Mikroglia eliminiert.
- Langzeitpotenzierung (LTP)
- Erfordert Aktivierung von NMDA-Rezeptoren, Ca²⁺-Einstrom und Phosphorylierung von AMPA-Rezeptoren, wodurch die synaptische Stärke innerhalb von Minuten um 200–400% erhöht wird, mit Konsolidierung durch Proteinsynthese innerhalb von 1–3 Stunden.
- Angereicherte Umgebung
- Bei Nagetieren erhöht sich die Dichte dendritischer Dornen um 25%, das Hippocampusvolumen um 15% und die Neurogenese im Gyrus dentatus um 50% im Vergleich zu Standardbedingungen.
Kritische Perioden der Gehirnentwicklung und ihre molekularen Mechanismen
Die kritische Periode für binokulares Sehen beim Menschen liegt zwischen 3–8 Jahren, wenn monokulare Deprivation (Schielen, Katarakt) aufgrund der Dominanz des offenen Auges im visuellen Kortex irreversible Amblyopie verursacht.
Öffnung und Schließung kritischer Perioden werden durch die Balance von Erregung/Hemmung reguliert: die Reifung Parvalbumin-positiver Interneurone und perineuronaler Netze beendet die Plastizität, während deren Abbau durch Chondroitinase ABC bei erwachsenen Ratten jugendliche Plastizität wiederherstellt.
Die Sprachentwicklung zeigt eine kritische Periode bis 7 Jahre für Phonologie (Unterscheidung von Lauten der Muttersprache) und bis 15 Jahre für Syntax, mit progressivem Rückgang der Fähigkeit zum akzentfreien Erwerb einer Zweitsprache um 0,7 Punkte auf der Kompetenzskala für jedes Jahr Verzögerung nach dem 7. Lebensjahr.
Die adulte Neurogenese bleibt in der subgranulären Zone des Hippocampus erhalten (700 neue Neuronen/Tag bei jungen Menschen, abnehmend auf 200/Tag bis zum 70. Lebensjahr) und in der subventrikulären Zone, mit Integration neuer Neuronen in bestehende Netzwerke innerhalb von 4–6 Wochen.
Klinische Neurowissenschaft — Hirnpathologien und ihre neurobiologischen Grundlagen
Neurodegenerative Erkrankungen und Mechanismen der Proteinaggregation
Die Alzheimer-Krankheit basiert auf zwei pathologischen Säulen: extrazellulären β-Amyloid-Plaques (Aβ42, Oligomerisierung bei Konzentrationen >100 nM) und intrazellulären neurofibrillären Bündeln aus hyperphosphoryliertem Tau-Protein (Phosphorylierung an 40+ Stellen statt 2-3 im Normalzustand). Im Demenzstadium gehen 30-40% der Neuronen im Hippocampus und entorhinalen Kortex verloren.
Die Pathologie breitet sich nach dem Braak-Schema aus: Stadien I-II (entorhinaler Kortex, symptomfrei) → III-IV (Hippocampus, leichte kognitive Beeinträchtigungen) → V-VI (Neokortex, schwere Demenz). Die Korrelation der Tau-Pathologie mit kognitivem Abbau (r=0,7-0,8) ist deutlich stärker als bei Amyloid (r=0,3-0,4).
| Erkrankung | Primärer Mechanismus | Schlüsselprotein | Neuronenverlust |
|---|---|---|---|
| Parkinson-Krankheit | Untergang dopaminerger Neuronen der Substantia nigra | α-Synuclein (Lewy-Körperchen) | 60-80% bis zum Auftreten motorischer Symptome |
| ALS | Selektive Degeneration motorischer Neuronen | TDP-43 (97%) oder SOD1 (20% familiäre Fälle) | 2-3% motorische Einheiten pro Monat; Überlebenszeit 3-5 Jahre |
Die Parkinson-Krankheit breitet sich nach der Braak-Hypothese aus: vom Bulbus olfactorius und dorsalen Vaguskern zum Mittelhirn und Kortex. Die Amyotrophe Lateralsklerose (ALS) schreitet mit einem Verlust von 2-3% motorischer Einheiten pro Monat fort, die mediane Überlebenszeit beträgt 3-5 Jahre ab Symptombeginn.
Psychische Störungen und ihre Neurobiologie auf Netzwerkebene
Die Major Depression ist ein Ungleichgewicht der Aktivität im präfrontal-limbischen Netzwerk. Der dorsolaterale präfrontale Kortex ist hypoaktiv (Stoffwechselreduktion um 15-25% im PET), der subgenuale anteriore cinguläre Kortex ist hyperaktiv (Brodmann-Areal 25, +30-40%), der Hippocampus verkleinert sich bei chronischer Depression um 8-10% aufgrund Glukokortikoid-induzierter Atrophie.
Die Monoamin-Hypothese erklärt die Wirkung von SSRIs: Sie erhöhen das synaptische Serotonin um das 3-5-fache, aber der therapeutische Effekt zeigt sich erst nach 2-4 Wochen, da neuroplastische Veränderungen erforderlich sind (BDNF-Erhöhung, Neurogenese).
Schizophrenie zeigt ein dopaminerges Ungleichgewicht: Der mesolimbische Pfad ist hyperaktiv (D2-Rezeptoren, +40-60% Dopaminfreisetzung → Positivsymptome), der mesokortikale Pfad ist hypoaktiv (präfrontaler Kortex → Negativsymptome und kognitives Defizit). Die graue Substanz nimmt um 2-3% ab, die Ventrikel erweitern sich um 20-30%.
Die Zwangsstörung (OCD) ist durch Hyperaktivität der orbitofrontal-striato-thalamo-kortikalen Schleife gekennzeichnet: Stoffwechsel im orbitofrontalen Kortex +25-35%, im Nucleus caudatus +15-20%. Nach erfolgreicher Therapie (SSRIs oder kognitive Verhaltenstherapie) normalisiert sich die Aktivität.
Neurotechnologien und Zukunft — Schnittstellen und Modulation der Gehirnaktivität
Gehirn-Computer-Schnittstellen und Dekodierung neuronaler Aktivität
Invasive BCI mit Mikroelektroden-Arrays (Utah Array, 96–128 Elektroden) registrieren Aktionspotenziale einzelner Neuronen des motorischen Kortex mit einer Auflösung von 30 kHz. Dies ermöglicht die Dekodierung von Bewegungsabsichten mit einer Genauigkeit von 90–95% und die Steuerung robotischer Gliedmaßen mit 7–10 Freiheitsgraden in Echtzeit (Latenz <100 ms).
Algorithmen des maschinellen Lernens (rekurrente neuronale Netze, Kalman-Filter) transformieren Aktivitätsmuster von 50–200 Neuronen in Bewegungstrajektorien. Ko-adaptive Decoder lernen durch Verstärkung und passen sich an Signalveränderungen an.
- Nicht-invasive BCI auf EEG-Basis nutzen P300 (Potenzial 300 ms nach Zielreiz, Amplitude 5–10 µV) oder motorische Vorstellungen (Desynchronisation des μ-Rhythmus 8–12 Hz im kontralateralen motorischen Kortex).
- Die Steuerung von Cursor oder Speller erreicht Geschwindigkeiten von 5–25 Zeichen/Minute mit einer Genauigkeit von 70–90%.
- Elektrokortikographie (ECoG) mit subduralen Elektroden bietet eine mittlere Auflösung (1–2 cm, 1 kHz) und dekodiert Sprache mit einer Genauigkeit von 75–90% für begrenztes Vokabular und 40–60% für freie Sprache.
Neuromodulation und therapeutische Anwendungen der Hirnstimulation
Tiefe Hirnstimulation (DBS) des Nucleus subthalamicus bei Parkinson-Krankheit (130–185 Hz, 2–4 V, 60–90 µs) verbessert motorische Symptome um 40–70% nach UPDRS-Skala und reduziert den Levodopa-Bedarf um 50–60%. Die Wirksamkeit bleibt bei 70% der Patienten über >10 Jahre erhalten.
Mechanismus: Unterdrückung pathologischer β-Oszillationen (13–30 Hz) in den Basalganglien und Normalisierung thalamo-kortikaler Aktivität. Adaptive DBS, die die Stimulation anhand lokaler Feldpotenziale (LFP) reguliert, erhöht die Wirksamkeit um 20–30%.
Transkranielle Magnetstimulation (TMS) des dorsolateralen präfrontalen Kortex (10 Hz, 3000 Impulse/Sitzung, 20–30 Sitzungen) zeigt Remission der Depression bei 30–40% der Patienten, die resistent gegen Antidepressiva sind. Der Mechanismus umfasst LTP-ähnliche Plastizität und eine Erhöhung von BDNF um 20–35%.
| Methode | Parameter | Effekt |
|---|---|---|
| tDCS (anodal) | 1–2 mA, 20–30 min | Erhöht kortikale Erregbarkeit um 30–40% |
| tDCS (kathodal) | 1–2 mA, 20–30 min | Senkt Erregbarkeit um 20–30% |
| tDCS + Arbeitsgedächtnis | Stimulation entsprechender Areale | Verbesserung um 10–20% |
| tDCS + motorisches Lernen | Stimulation entsprechender Areale | Beschleunigung um 15–25% |

Knowledge Access Protocol
FAQ
Häufig gestellte Fragen
Neurowissenschaft ist ein interdisziplinäres Forschungsgebiet, das Struktur, Funktion und Entwicklung des Nervensystems untersucht. Sie vereint Biologie, Psychologie, Chemie und Physik, um die Funktionsweise des Gehirns, Verhaltensmechanismen und kognitive Prozesse zu verstehen. Die Forschung umfasst Ebenen von Molekülen bis hin zu ganzen neuronalen Netzwerken.
Neuronen übertragen Informationen durch elektrische Impulse und chemische Signale an Synapsen. Wenn ein Impuls das Ende eines Neurons erreicht, werden Neurotransmitter freigesetzt, die sich an Rezeptoren der nächsten Zelle binden. Dieser Prozess dauert Millisekunden und bildet die Grundlage aller Gehirnfunktionen.
Neuroplastizität ist die Fähigkeit des Gehirns, seine Struktur und Funktion als Reaktion auf Erfahrung und Lernen zu verändern. Neuronale Verbindungen können sich ein Leben lang verstärken, abschwächen oder neu bilden. Diese Eigenschaft ermöglicht es dem Gehirn, sich nach Schädigungen zu erholen und sich an neue Bedingungen anzupassen.
Nein, das ist ein weit verbreiteter Mythos, der durch Neuroimaging widerlegt wurde. Studien zeigen, dass alle Gehirnregionen aktiv sind und bestimmte Funktionen erfüllen, selbst im Ruhezustand. Verschiedene Aufgaben aktivieren unterschiedliche Bereiche, aber im Laufe des Tages wird das gesamte Gehirn genutzt.
MRT zeigt die Aktivität von Gehirnregionen, kann aber keine konkreten Gedanken „lesen
Chronischer Alkoholmissbrauch kann irreversible Schäden an Neuronen verursachen, insbesondere im Hippocampus und präfrontalen Kortex. Bei mäßigem Konsum und Abstinenz kann sich das Gehirn jedoch dank Neuroplastizität teilweise erholen. Das Ausmaß der Erholung hängt von Dauer und Schwere des Konsums ab.
Wirksam sind regelmäßige körperliche Bewegung, qualitativ hochwertiger Schlaf und wiederholtes Lernen in Intervallen. Aerobe Belastungen stimulieren die Neurogenese im Hippocampus, während Schlaf Erinnerungen konsolidiert. Auch Mnemotechniken, soziale Aktivität und das Erlernen neuer Fähigkeiten helfen, neuronale Verbindungen zu stärken.
Neurotransmitter sind chemische Substanzen, die Signale zwischen Neuronen über Synapsen übertragen. Dopamin reguliert Motivation und Belohnung, Serotonin die Stimmung, GABA die Hemmung neuronaler Aktivität. Ein Ungleichgewicht der Neurotransmitter steht in Verbindung mit Depression, Angststörungen und anderen Erkrankungen.
Schnittstellen registrieren die elektrische Aktivität des Gehirns über Elektroden und wandeln sie in Befehle für Geräte um. Die Technologie nutzt EEG oder implantierte Sensoren zur Dekodierung der Absichten des Nutzers. Sie wird zur Steuerung von Prothesen, zur Kommunikation gelähmter Patienten und zur Rehabilitation nach Schlaganfall eingesetzt.
Ja, kritische Phasen sind Zeitfenster maximaler Empfindlichkeit des Gehirns für bestimmte Reize. Beispielsweise ist die Entwicklung des Sehvermögens in den ersten Lebensjahren am aktivsten, während Sprachfähigkeiten am besten vor dem Jugendalter erworben werden. Nach dem Schließen dieser Fenster ist Lernen möglich, aber weniger effektiv.
Dies ist eine Vereinfachung, die die Realität nicht widerspiegelt. Beide Hemisphären sind an den meisten kognitiven Prozessen beteiligt, obwohl sie eine gewisse Spezialisierung aufweisen. Beispielsweise ist die linke Hemisphäre häufiger mit Sprache verbunden, aber Kreativität erfordert die Interaktion beider Hemisphären. Neuroimaging zeigt komplexe Aktivität bei allen Aufgaben.
Die Alzheimer-Krankheit ist durch die Ansammlung von Beta-Amyloid-Plaques und Tau-Protein im Gehirn gekennzeichnet, was zum Absterben von Neuronen führt. Betroffen sind Bereiche, die für Gedächtnis und Denken zuständig sind, insbesondere der Hippocampus und die Großhirnrinde. Der Prozess beginnt Jahrzehnte vor dem Auftreten von Symptomen und ist derzeit irreversibel.
Die Wirksamkeit der meisten „Gehirntrainer
Chronischer Stress verursacht eine Atrophie des Hippocampus, was das Gedächtnis beeinträchtigt, und vergrößert die Amygdala, was Ängstlichkeit verstärkt. Erhöhtes Cortisol schädigt Neuronen und unterdrückt die Neurogenese. Diese Veränderungen sind jedoch teilweise reversibel durch Stressreduktion, Meditation und Therapie.
Bewusstsein ist die integrierte Informationsverarbeitung durch verteilte neuronale Netzwerke, insbesondere in der Großhirnrinde und im Thalamus. Theorien umfassen den globalen Arbeitsraum und integrierte Information, aber es gibt kein vollständiges Verständnis. Forschungen untersuchen neuronale Korrelate des Bewusstseins bei Wahrnehmung, Aufmerksamkeit und Selbstbewusstsein.
Dies ist ein theoretisches Konzept, das aufgrund der Komplexität des Gehirns und des mangelnden Verständnisses der Natur des Bewusstseins weit von der Realisierung entfernt ist. Es erfordert eine vollständige Kartierung von 86 Milliarden Neuronen und Billionen von Synapsen sowie die Reproduktion ihrer Dynamik. Philosophische Fragen zur Identität der Person und zur subjektiven Erfahrung bleiben ungelöst.
